Содержание
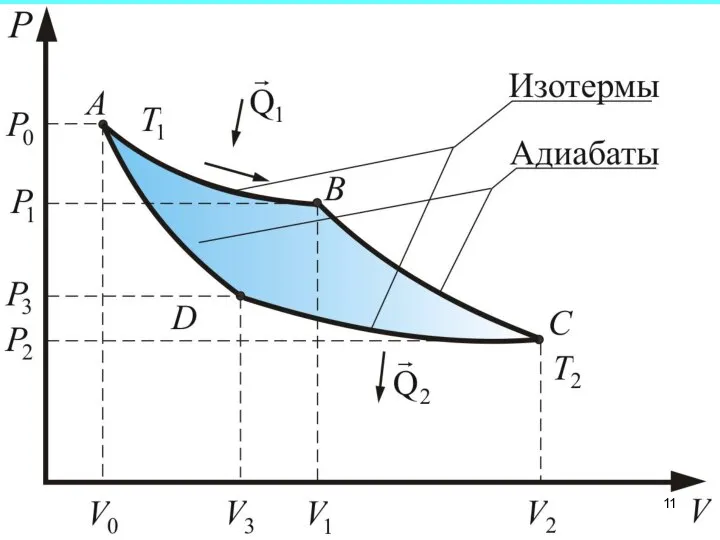
- 2. Процесс А-В – изотермическое расширение Процесс В-С – адиабатическое расширение. γ – коэффициент Пуассона.
- 3. Процесс С-D – изотермическое сжатие Процесс D-A – адиабатическое сжатие.
- 5. КПД цикла Карно η Если Т2 = 0, то η = 1, что невозможно, т.к. абсолютный
- 6. Теоремы Карно. К.п.д. η обратимой идеальной тепловой машины Карно не зависит от рабочего вещества. 2. К.п.д.
- 7. МОЛЕКУЛЯРНАЯ ФИЗИКА ТЕРМОДИНАМИКА Энтропия
- 8. Вопросы Приведенная теплота. Энтропия Изменение энтропии 3. Поведение энтропии в процессах изменения агрегатного состояния
- 9. 1. Приведенная теплота. Энтропия Из рассмотренного цикла Карно видно, что равны между собой отношения теплот к
- 10. Отношение теплоты Q в изотермическом процессе к температуре, при которой происходила передача теплоты, называется приведенной теплотой
- 12. Суммируя приведенную теплоту на всех участках процесса, получим: Тогда в обратимом цикле Карно имеем:
- 13. Этот результат справедлив для любого обратимого процесса. Таким образом, для процесса, происходящего по замкнутому циклу (2)
- 14. Это позволяет ввести новую функцию состояния S: (3) Функция состояния, полный дифференциал которой равен , называется
- 15. Понятие энтропии было впервые введено Рудольфом Клаузиусом в 1865 г. Для обратимых процессов изменение энтропии: (4)
- 16. Клаузиус Рудольф Юлиус Эмануэль (1822 – 1888) – немецкий физик-теоретик, один из создателей термодинамики и кинетической
- 17. В 1850 г. получил общие соотношения между теплотой и механической работой (первое начало термодинамики) и разработал
- 18. 2. Изменение энтропии в изопроцессах Энтропия системы является функцией ее состояния, определенная с точностью до произвольной
- 19. Таким образом, по этой формуле можно определить энтропию лишь с точностью до аддитивной постоянной, т.е. начало
- 20. Так как, а то или (6)
- 21. т.е. изменение энтропии ΔS1→2 идеального газа при переходе его из состояния 1 в состояние 2 не
- 22. изобарический: т.к. Р1 = Р2, изотермический: т.к. адиабатический: адиабатический процесс называют изоэнтропийным процессом, т.к.
- 23. Изменение энтропии в изопроцессах:
- 24. 3. Поведение энтропии в процессах изменения агрегатного состояния Рассмотрим три агрегатных состояния: твердое, жидкое и газообразное
- 25. 1. Переход вещества из твердого состояния (фазы) в жидкое называется плавлением, а обратный – кристаллизация. 2.
- 26. 4. Закон плавления: количество тепла ∂Q, которое необходимо для плавления вещества массой dm, пропорционально этой массе:
- 27. Этот закон справедлив и для кристаллизации, правда, с одним отличием: ∂Q в этом случае – тепло
- 28. Изменение энтропии в процессе этого фазового перехода можно найти просто, если считать процесс равновесным. Это вполне
- 29. Тогда можно использовать термодинамический смысл энтропии: с точки зрения термодинамики энтропия – это такая функция состояния
- 30. или . Подставим сюда выражение для ∂Q, получим: .
- 31. Так как температура системы в данном фазовом переходе не меняется и равна температуре плавления, то подынтегральное
- 32. Из этой формулы следует, что при плавлении энтропия возрастает, а при кристаллизации уменьшается. Физический смысл этого
- 33. Поэтому при равной температуре энтропия твердого тела меньше энтропии жидкости. Это означает, что твердое тело представляет
- 34. Фазовый переход «жидкость – газ» Этот переход обладает всеми свойствами перехода «твердое тело – жидкость». Существует
- 35. 2: при испарении система поглощает тепло, при конденсации – теряет. 3: процессы испарения и конденсации протекают
- 36. В процессе фазового перехода «жидкость – газ» температура остается постоянной и равной температуре кипения до тех
- 37. Коэффициент пропорции r в этом выражении, есть константа, зависящая от вещества системы, называемая удельной теплотой испарения.
- 38. Изменение энтропии в этом процессе можно найти просто, считая процесс равновесным. И опять это вполне допустимое
- 39. Из формулы следует, что при испарении энтропия возрастает, а при конденсации уменьшается.
- 40. Физический смысл этого результата состоит в различии фазовой области молекулы в жидкости и газе. Хотя в
- 41. занятой жидкостью, но не имеет возможности «оторваться от коллектива» остальных молекул: стоит ей оторваться от одной
- 42. Молекулы газа ведут себя иначе. У них гораздо больше свободы, среднее расстояние между ними таково, что
- 44. Скачать презентацию








































 Творчий проект «Енергія»
Творчий проект «Енергія» Презентация по физике "Решение задач по теме "Закон Кулона"" - скачать
Презентация по физике "Решение задач по теме "Закон Кулона"" - скачать  Ходовая система трактора МТЗ - 82(80)
Ходовая система трактора МТЗ - 82(80) Постоянный электрический ток. Причины электрического тока
Постоянный электрический ток. Причины электрического тока Прямолинейное равномерное движение
Прямолинейное равномерное движение Приспособления к швейной машине
Приспособления к швейной машине Введение в космологию Наука о возникновении и развитии Вселенной
Введение в космологию Наука о возникновении и развитии Вселенной Презентация по физике "Вес и сила тяжести" - скачать бесплатно
Презентация по физике "Вес и сила тяжести" - скачать бесплатно Постоянные магниты
Постоянные магниты Термодинамика
Термодинамика Особенности поведения основного металла и сварных соединений при низких температурах
Особенности поведения основного металла и сварных соединений при низких температурах Презентация по физике "Зрительные иллюзии" - скачать бесплатно
Презентация по физике "Зрительные иллюзии" - скачать бесплатно Барометр-анероид
Барометр-анероид Вращение звезд. (Тема 17)
Вращение звезд. (Тема 17) Закон збереження механічної енергії
Закон збереження механічної енергії Динамометр. Взаимодействие тел. 7 класс
Динамометр. Взаимодействие тел. 7 класс Эксплуатация топливной системы главных двигателей судна проекта 428 - 2 ОТ - 2100
Эксплуатация топливной системы главных двигателей судна проекта 428 - 2 ОТ - 2100 Покрытия материалов
Покрытия материалов Механическое движение - Презентация по физике_
Механическое движение - Презентация по физике_ Степени свободы. Четвертая задача динамики
Степени свободы. Четвертая задача динамики Лекция 10.7. Фазовые диаграммы
Лекция 10.7. Фазовые диаграммы Электростатика. Работа поля над зарядом. Потенциал. Разность потенциалов
Электростатика. Работа поля над зарядом. Потенциал. Разность потенциалов Архімедова сила. Плавання тіл. Виштовхування тіла
Архімедова сила. Плавання тіл. Виштовхування тіла Открытие и исследования электромагнетизма
Открытие и исследования электромагнетизма Градуировка спектроскопа определение длины волны спектральных линий
Градуировка спектроскопа определение длины волны спектральных линий Пленочные наноматериалы и технологии их получения
Пленочные наноматериалы и технологии их получения Отличия идеального газа от реального. Идеальный газ
Отличия идеального газа от реального. Идеальный газ Жолио Кюри Ирен
Жолио Кюри Ирен