Содержание
- 2. Люминесценция (англ. luminescence) – - свечение. Термин введен Видеманом в 1889 году.
- 3. Выдающуюся роль в разви-тии учения о люминесцен-ции сыграла советская школа физиков, созданная С.И. Вавиловым (президент АН
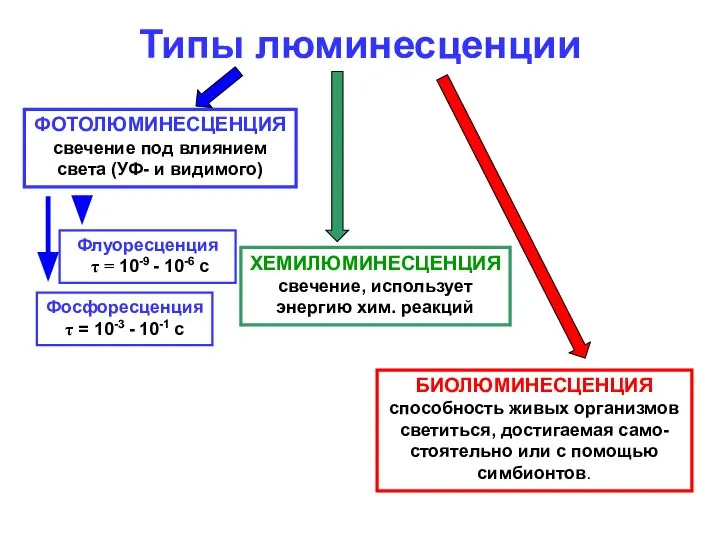
- 4. Типы люминесценции ФОТОЛЮМИНЕСЦЕНЦИЯ свечение под влиянием света (УФ- и видимого) Флуоресценция τ = 10-9 - 10-6
- 5. Другие типы люминесценции РАДИОЛЮМИНЕСЦЕНЦИЯ - при возбуждении веще- ства ионизирующим излучением. ЭЛЕКТРОЛЮМИНЕСЦЕНЦИЯ - возникает при про-
- 6. ХЕМИЛЮМИНЕСЦЕНЦИЯ Многие химические реакции протекают с выделе-нием энергии в форме тепла (экзотермические реак-ции). Существуют химические реакции,
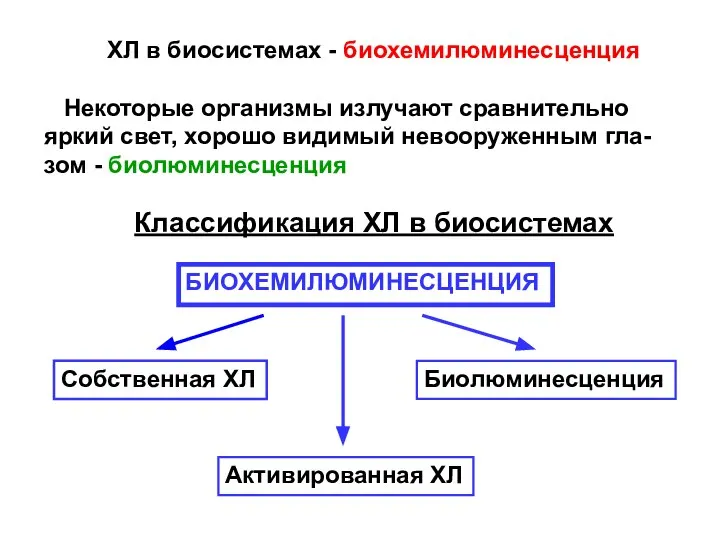
- 7. ХЛ в биосистемах - биохемилюминесценция Некоторые организмы излучают сравнительно яркий свет, хорошо видимый невооруженным гла- зом
- 8. В основе био-ХЛ (собственного или сверхслабого свечения) лежат реакции взаимодействия между свободными радикалами (СР): радикалами липидов,
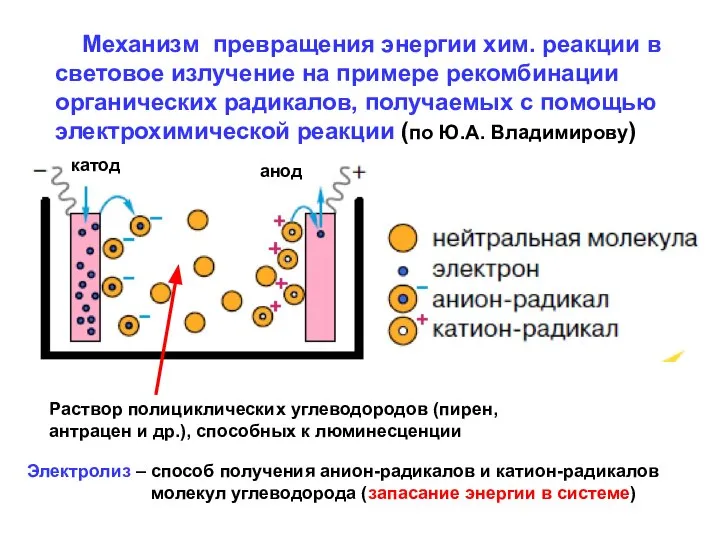
- 9. Механизм превращения энергии хим. реакции в световое излучение на примере рекомбинации органических радикалов, получаемых с помощью
- 10. Образование радикалов: с катода на нейтральную молекулу переходят электроны, образуя анион-ради-кал (q-); на аноде нейтральная молекула
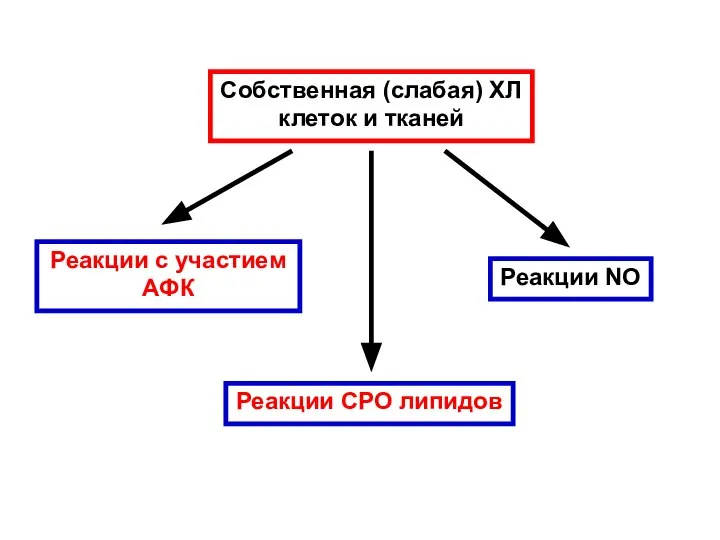
- 11. Собственная (слабая) ХЛ клеток и тканей Реакции с участием АФК Реакции СРО липидов Реакции NO
- 12. I тип реакций: Собственное свечение клеток и тканей с участием активных форм кислорода Активные формы кислорода
- 13. В мембранах макрофагов содержится НАДФН-ок-сидазный комплекс, с помощью которого НАДФН окисляется в результате восстановления двух моле-
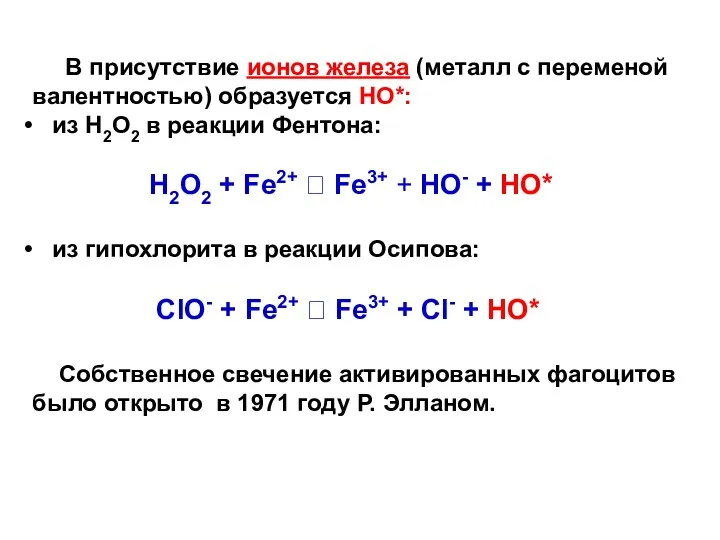
- 14. В присутствие ионов железа (металл с переменой валентностью) образуется НО*: из Н2О2 в реакции Фентона: H2O2
- 15. Полагают, что свечение обусловлено образовани- ем синглетного кислорода (1О2 – одна из форм воз- бужденного состояния
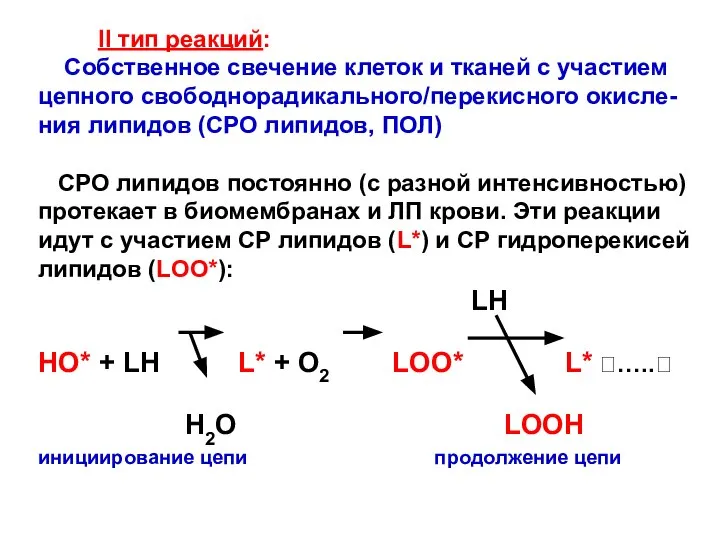
- 16. II тип реакций: Собственное свечение клеток и тканей с участием цепного свободнорадикального/перекисного окисле-ния липидов (СРО липидов,
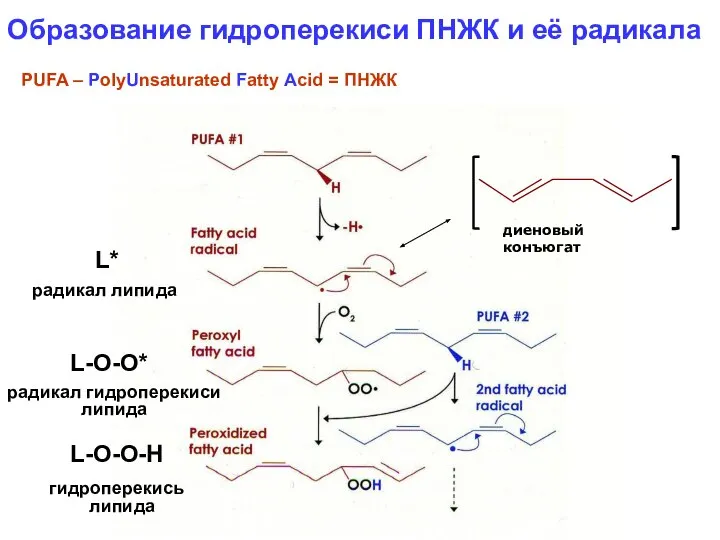
- 17. Образование гидроперекиси ПНЖК и её радикала PUFA – PolyUnsaturated Fatty Acid = ПНЖК диеновый конъюгат L-O-O*
- 18. LOO* - СР, которые ведут цепь СРО липида. Их взаи-модействие приводит к образованию продуктов, которые находятся
- 19. III тип реакций: Собственное свечение клеток и тканей с участием оксида азота (NO) Оксид азота –
- 20. Причины чрезвычайно низкой интенсивности собственной ХЛ клеток и тканей («сверхслабое свечение») 1. [СР] в биологических системах
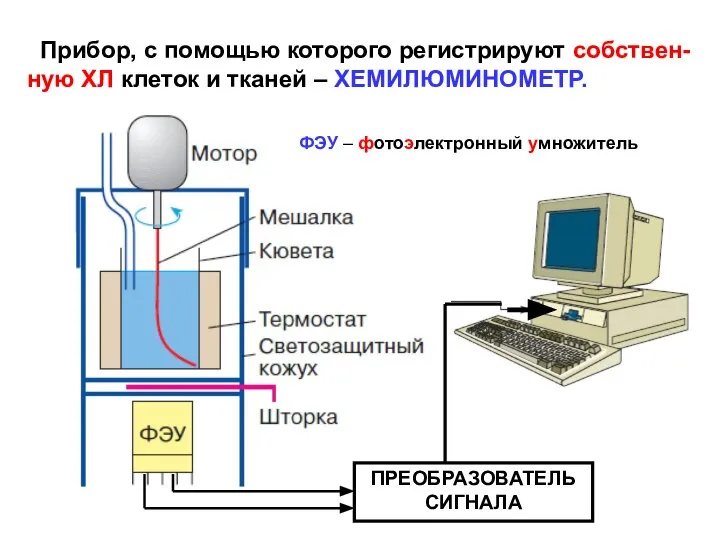
- 21. Прибор, с помощью которого регистрируют собствен- ную ХЛ клеток и тканей – ХЕМИЛЮМИНОМЕТР. ПРЕОБРАЗОВАТЕЛЬ СИГНАЛА ФЭУ
- 22. Что измеряем с помощью хемилюминометра? Главные участники реакций, лежащих в основе ХЛ клеток и тканей –
- 23. Интенсивность ХЛ при СРО липидов равна скорости образования фотонов (квантов светового излучения) в реакции: LOO* +
- 24. Т.о., интенсивность свечения (интенсивность ХЛ) отражает [СР], которые ведут (продолжают) цепи реакций ПОЛ, в каждый момент
- 25. Для чего используют измерение собственной (неактивированной) ХЛ Изучение фундаментальных механизмов проте-кания реакций ПОЛ в живых системах,
- 26. 2. Показатель активности процессов СРО липидов в тканях организма (сыворотка, плазма и клетки крови) при патологии
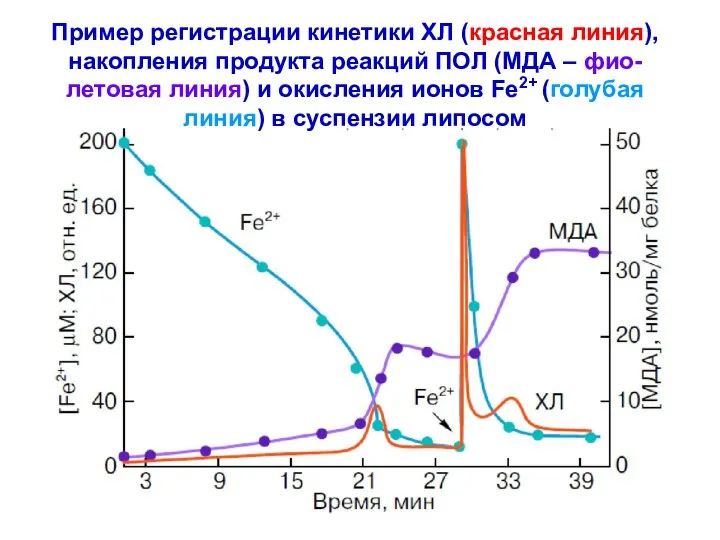
- 27. Пример регистрации кинетики ХЛ (красная линия), накопления продукта реакций ПОЛ (МДА – фио-летовая линия) и окисления
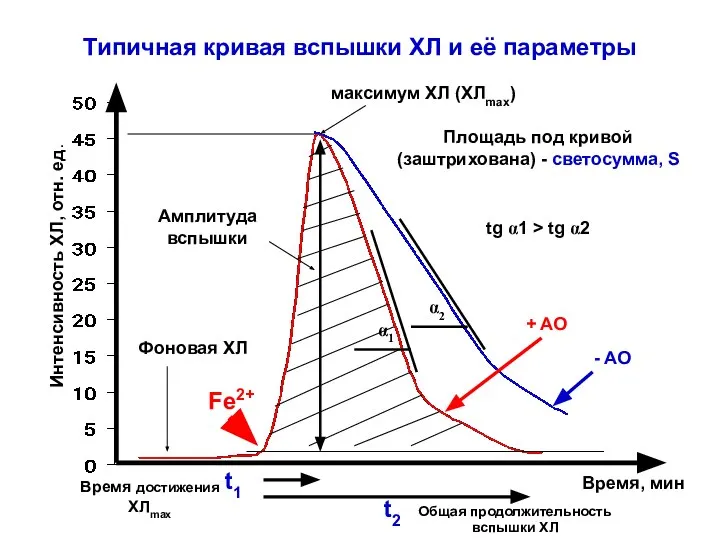
- 28. Типичная кривая вспышки ХЛ и её параметры Интенсивность ХЛ, отн. ед. Время, мин Fe2+ t1 t2
- 29. Активированная ХЛ Активированная ХЛ Химические активаторы ХЛ Физические активаторы ХЛ 1. Химические активаторы ХЛ (хемилюминогенные зонды).
- 30. Благодаря этому, увеличивается доля возбужден-ных молекул по отношению к общему числу молекул. В результате свечение становится
- 31. Примеры химических активаторов ХЛ (хемилюми-ногенных зондов): Люминол (3-аминофталевый гидразид) – обеспечи-вает интенсивное свечение в присутствие НО*
- 32. 2. Физические активаторы Эти молекулы не вступают в химические реакции со СР. В основе усиления ими
- 33. Примеры физических активаторов ХЛ (для реак- ций СРО липидов, т.е. детекция СР липидов – L*, LO*
- 34. Для чего используют измерение активированной ХЛ Обнаружение веществ – катализаторов, разлага-ющих Н2О2 с образованием СР. Н2О2
- 35. 1.1. Обнаружение миоглобина в биологических жидкостях. При инфаркте миокарда в моче больного появля-ется миоглобин (выходит из
- 36. 1.2. ХЛ раневого экссудата. Реакция воспаления обеспечивает присутствие в экссудате Н2О2, гемсодержащих белков и других СР.
- 37. 1.3. ХЛ клеток – фагоцитов. Фагоцитирующие клетки (гранулоциты, моноциты, тканевые макрофаги) продуцируют АФК, с помощью которых
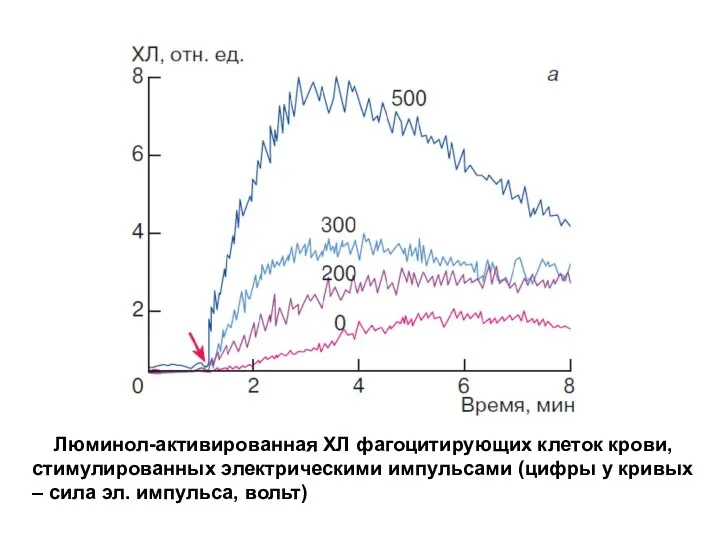
- 38. Люминол-активированная ХЛ фагоцитирующих клеток крови, стимулированных электрическими импульсами (цифры у кривых – сила эл. импульса, вольт)
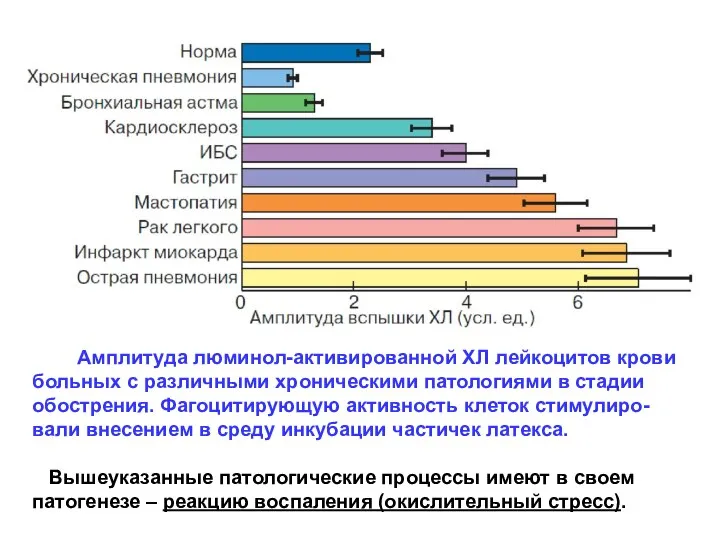
- 39. Амплитуда люминол-активированной ХЛ лейкоцитов крови больных с различными хроническими патологиями в стадии обострения. Фагоцитирующую активность клеток
- 41. Скачать презентацию














![Т.о., интенсивность свечения (интенсивность ХЛ) отражает [СР], которые ведут (продолжают) цепи](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/649402/slide-23.jpg)










 Закон всемирного тяготения. Искусственные спутники Земли. Решение задач
Закон всемирного тяготения. Искусственные спутники Земли. Решение задач Плоская система сил
Плоская система сил Гамма – излучение
Гамма – излучение Скорость прямолинейного равноускоренного движения. График скорости
Скорость прямолинейного равноускоренного движения. График скорости Устройство подвески Лада Веста
Устройство подвески Лада Веста Пространственная система сил
Пространственная система сил Эллиптическое движение
Эллиптическое движение Радиоактивные батарейки
Радиоактивные батарейки Что изучает физика
Что изучает физика Магнитное поле. Его свойства
Магнитное поле. Его свойства Смачивание и капиллярность в природе и технике
Смачивание и капиллярность в природе и технике Лазер и его применение
Лазер и его применение Основы кинематики
Основы кинематики Ядерный магнитный резонанс
Ядерный магнитный резонанс Электрический ток. (лекция 2)
Электрический ток. (лекция 2) Теория переноса ионизирующего излучения
Теория переноса ионизирующего излучения Телескопы: линзовые, зеркальные, зеркально-линзовые
Телескопы: линзовые, зеркальные, зеркально-линзовые Методика подготовки к ЕГЭ, специфика преподавания физики. Примеры
Методика подготовки к ЕГЭ, специфика преподавания физики. Примеры Магнитное поле. Магниты естественные и искусственные
Магнитное поле. Магниты естественные и искусственные Агрегатное состояние вещества Приготовила:Верхозина Анастасия
Агрегатное состояние вещества Приготовила:Верхозина Анастасия  Аттестационная работа. Методическая разработка по выполнению проекта Невидимые оковы тяжести. Земное притяжение
Аттестационная работа. Методическая разработка по выполнению проекта Невидимые оковы тяжести. Земное притяжение Термодинамика – табиғатта жүретін жылулық қозғалыс туралы ғылым
Термодинамика – табиғатта жүретін жылулық қозғалыс туралы ғылым Схемы многокорпусных выпарных установок
Схемы многокорпусных выпарных установок Замена маслосъёмных колпачков автомобиля ВАЗ2110
Замена маслосъёмных колпачков автомобиля ВАЗ2110 Закон сохранения энергии
Закон сохранения энергии Термомеханические испытания. Методы и средства механических испытаний
Термомеханические испытания. Методы и средства механических испытаний Модельный ряд двигателей ЗМЗ
Модельный ряд двигателей ЗМЗ Биофизика дыхания. Объемы и емкости легких
Биофизика дыхания. Объемы и емкости легких