Содержание
- 2. Основы мкт Молекулярно-кинетическая теория Масса и размеры молекул Количество вещества Строение газов, жидкостей и твердых тел
- 3. Молекулярно-кинетическая теория МКТ объясняет свойства макроскопических тел и тепловых процессов, на основе представлений о том, что
- 4. Основные положения мкт Вещество состоит из частиц Частицы непрерывно и хаотически движутся Частицы взаимодействуют друг с
- 5. Масса и размеры молекул
- 6. Масса и размеры молекул Массы молекул в макроскопических масштабах чрезвычайно малы.
- 7. Количество вещества В 1 моле любого вещества содержится одно и то же число атомов или молекул.
- 8. Количество вещества Молярной массой вещества называют массу вещества, взятого в количестве 1 моль. m0 - масса
- 9. Количество вещества m – масса вещества
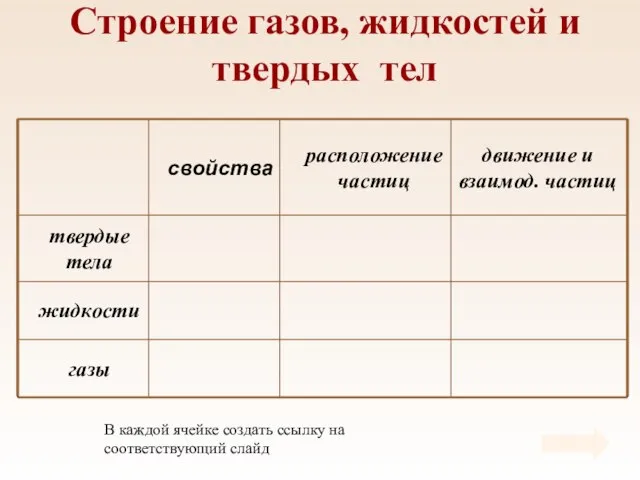
- 10. Таблица Свойства газов, жидкостей и твердых тел
- 11. Строение газов, жидкостей и твердых тел В каждой ячейке создать ссылку на соответствующий слайд
- 12. Свойства Твердые тела сохраняют объем и форму.
- 13. Свойства Жидкости сохраняют объем и принимают форму сосуда. Обладают текучестью.
- 14. Свойства Газы не имеют формы, занимают весь предоставленный объем.
- 15. Расположение частиц Частицы расположены в строгом порядке вплотную друг к другу. Кристаллическая решетка.
- 16. Расположение частиц Частицы расположены вплотную друг к другу, образуют только ближний порядок.
- 17. Расположение частиц Частицы расположены на значительных расстояниях (расстояния между частицами во много раз больше размеров самих
- 18. Движение и взаимодействие частиц Частицы совершают колебательные движения около положения равновесия Силы притяжения и отталкивания значительны
- 19. Движение и взаимодействие частиц Частицы совершают колебательные движения около положения равновесия, изредка совершая скачки на новое
- 20. Движение и взаимодействие частиц Частицы свободно перемещаются по всему объему, двигаясь поступательно Силы притяжения почти отсутствуют,
- 21. Идеальный газ Идеальный газ – это газ, в котором Частицы – материальные точки Частицы взаимодействуют только
- 22. Среднее значение квадрата скорости молекул Скорость – величина векторная, поэтому средняя скорость движения частиц в газе
- 23. Среднее значение квадрата скорости молекул
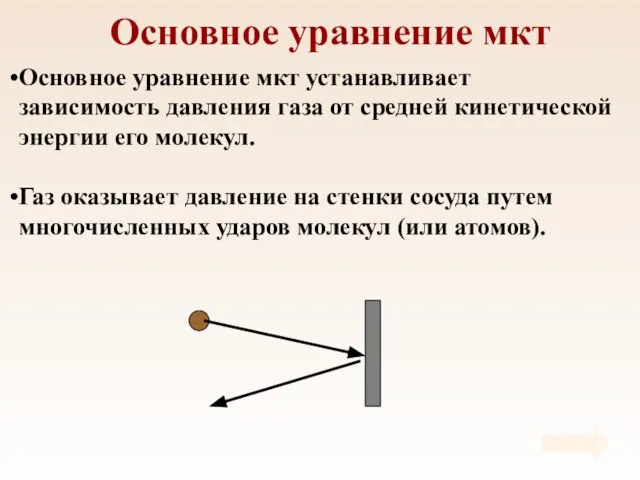
- 24. Основное уравнение мкт Основное уравнение мкт устанавливает зависимость давления газа от средней кинетической энергии его молекул.
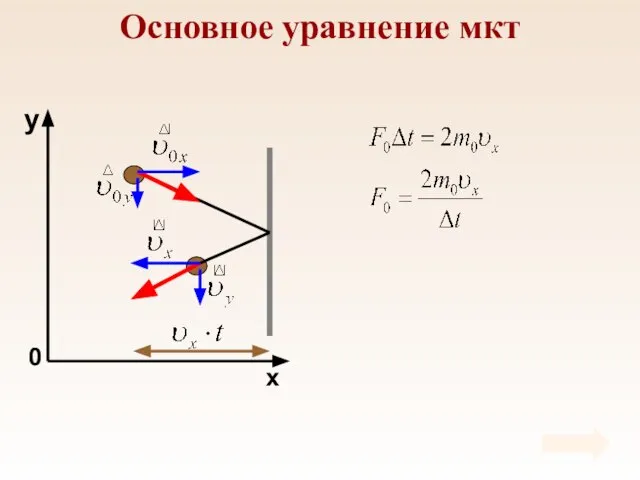
- 25. Основное уравнение мкт
- 26. Число ударов и общая сила
- 27. Основное уравнение мкт
- 28. Воспользуйтесь таблицей Менделеева и определите молярную массу ацетилена С2H2. Чему равна масса одной молекулы ацетилена в
- 29. Сколько молекул содержится в 10 г углекислого газа?
- 39. Скачать презентацию

































 Принцип работы лазера и основные свойства лазерного излучения
Принцип работы лазера и основные свойства лазерного излучения Уравнения Шредингера. Движение свободной частицы
Уравнения Шредингера. Движение свободной частицы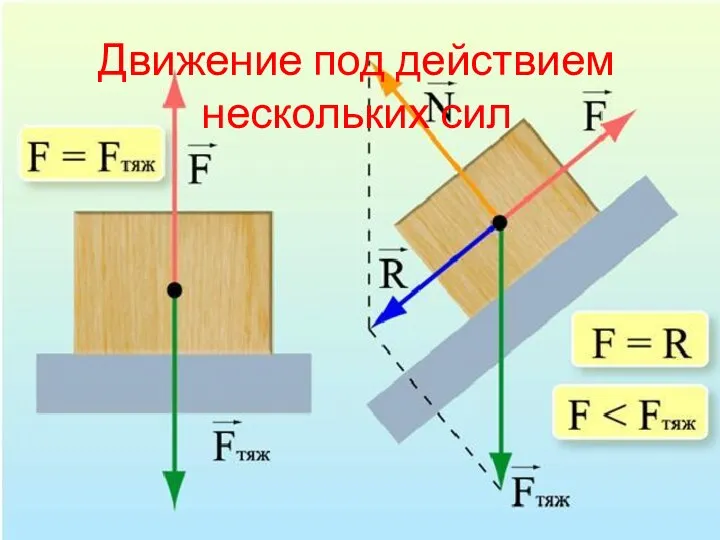 Презентация Движение под действием нескольких сил
Презентация Движение под действием нескольких сил Машинная игла
Машинная игла Презентация Закон Ома Как связаны между собой I и U
Презентация Закон Ома Как связаны между собой I и U  Модель с силами сцепления у вершины трещины. Модель Дагдейла
Модель с силами сцепления у вершины трещины. Модель Дагдейла Закони Ньютона
Закони Ньютона Презентация по физике "Виды спектров. Спектральный анализ." - скачать бесплатно
Презентация по физике "Виды спектров. Спектральный анализ." - скачать бесплатно Свободное падение тел
Свободное падение тел Естественные и искусственные освещения
Естественные и искусственные освещения Классификация и основные виды антенн. Антенно-фидерные устройства и распространение радиоволн
Классификация и основные виды антенн. Антенно-фидерные устройства и распространение радиоволн Рентгеновское излучение
Рентгеновское излучение Колебательные движения
Колебательные движения Механическое движение
Механическое движение Смазка автомобиля
Смазка автомобиля Продольные и поперечные магнитооптические эффекты. Распространение электромагнитной волны в среде. Уравнения Максвелла
Продольные и поперечные магнитооптические эффекты. Распространение электромагнитной волны в среде. Уравнения Максвелла Презентация на тему «Метод толстослойных фотоэмульсий» Подготовила Живулько Елена.
Презентация на тему «Метод толстослойных фотоэмульсий» Подготовила Живулько Елена. Сила трения
Сила трения Перенапряжения в отключении малых индуктивных токов. (Лекция 2.3)
Перенапряжения в отключении малых индуктивных токов. (Лекция 2.3) Чистые вещества и смеси
Чистые вещества и смеси Агрегатные состояния вещества
Агрегатные состояния вещества Задача стационарной теплопередачи на примере полуограниченной пластины и длинного цилиндра
Задача стационарной теплопередачи на примере полуограниченной пластины и длинного цилиндра Электротехника. Методы расчёта электрических цепей. (лекция 5)
Электротехника. Методы расчёта электрических цепей. (лекция 5)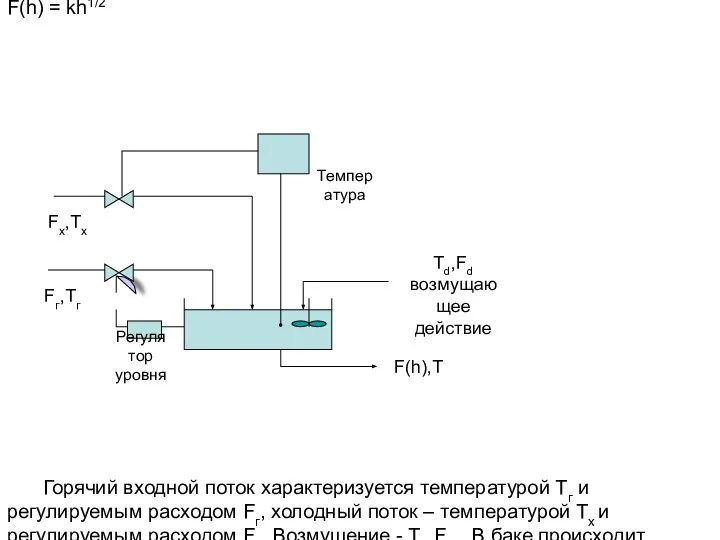 Смесительный бак с регулированием уровня и температуры. Пример
Смесительный бак с регулированием уровня и температуры. Пример Лазеры (или идеал, который создал человек)
Лазеры (или идеал, который создал человек) Аттестационная работа. Методическая разработка индивидуальной исследовательской работы - из опыта работы учителя
Аттестационная работа. Методическая разработка индивидуальной исследовательской работы - из опыта работы учителя Левитация проводящего кольца в переменном магнитном поле
Левитация проводящего кольца в переменном магнитном поле Механика материалов. Теории прочности и разрушения. (Лекция 23)
Механика материалов. Теории прочности и разрушения. (Лекция 23)