Содержание
- 2. 1.1 Статистический и термодинамический методы исследования. Статистический метод используется в молекулярной физике. На основе рассмотрения движения
- 3. Макроскопическим параметром называется физическая величина, характеризующая какое-либо свойство системы частиц как целого , например, температура, давление,
- 4. Пример : Как можно получить среднее значение микропараметра. Пусть N раз измеряли скорость молекул газа: Если
- 5. Термодинамический метод исследования не рассматривает внутреннее строение вещества и характер движения отдельных частиц. Термодинамика : --
- 6. 1.2 Состояние системы. Процесс. Макросостояние системы задается набором значений макропараметров (для газов это P,V,T). Микросостояние системы
- 7. Переход системы из одного макроскопического состояния в другое называется процессом, что обязательно связано с нарушением равновесия,
- 8. Равновесный процесс всегда обратим, т.е. может проходить в обратном направлении через те же состояния, что и
- 9. 2. Элементы молекулярно-кинетической теории Основная физическая модель, с которой работает МКТ – идеальный газ. Идеальным газом
- 10. В молекулярной физике естественно при измерении количества вещества исходить из массы одной молекулы -- .
- 11. Уравнение Менделеева – Клапейрона (1) для 1-го моля газа: PV=RT. Универсальная газовая постоянная постоянная Больцмана. Запишем
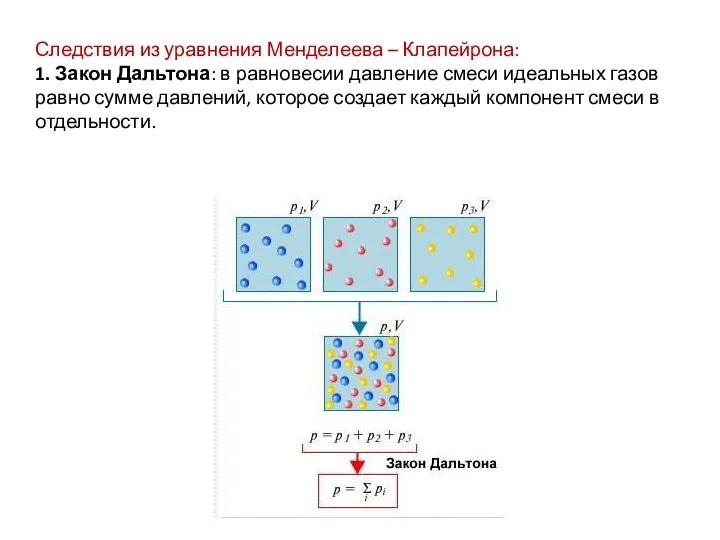
- 12. Следствия из уравнения Менделеева – Клапейрона: 1. Закон Дальтона: в равновесии давление смеси идеальных газов равно
- 13. 2. Закон Авогадро: различные газы, находящиеся в одинаковых объемах при равных температурах и давлениях, содержат одинаковое
- 14. 2.2 Основное уравнение МКТ для давления идеального газа Найдем связь давления газа и среднего значения кинетической
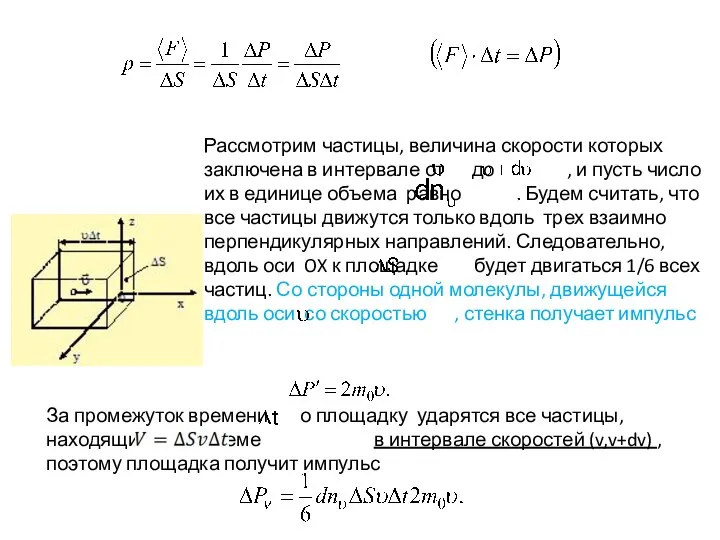
- 15. Рассмотрим частицы, величина скорости которых заключена в интервале от до , и пусть число их в
- 16. Т.к. , то Или: (3) – это основное уравнение МКТ для давления идеального газа. Рассмотрение более
- 17. 2.3 Закон равномерного распределения энергии молекул по степеням свободы Приравняв правые части (1) и (2), получим:
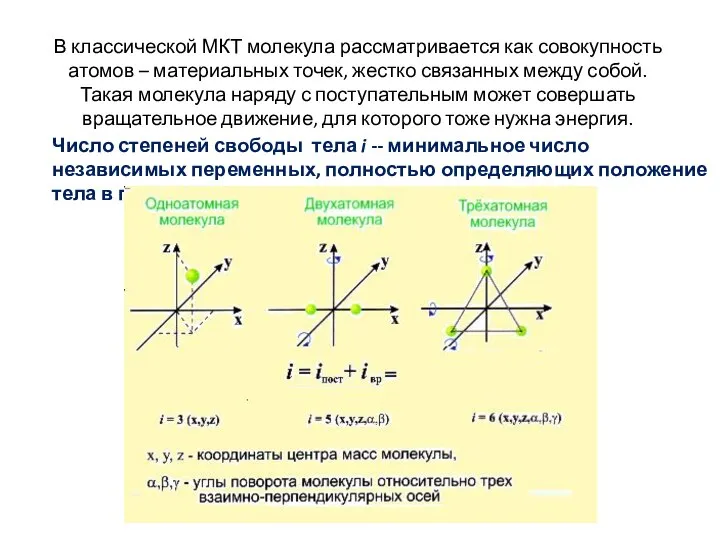
- 18. В классической МКТ молекула рассматривается как совокупность атомов – материальных точек, жестко связанных между собой. Такая
- 19. В статической физике доказывается положение о равномерном распределении энергии по степеням свободы молекулы. На каждую степень
- 20. 3. Статистические законы распределения в МКТ. Статистические законы принципиально отличаются от законов классической механики. Так, закон
- 21. 2. Вероятностью случайного события, дающего результат со значением рi , называется отношение числа испытаний Ni ,
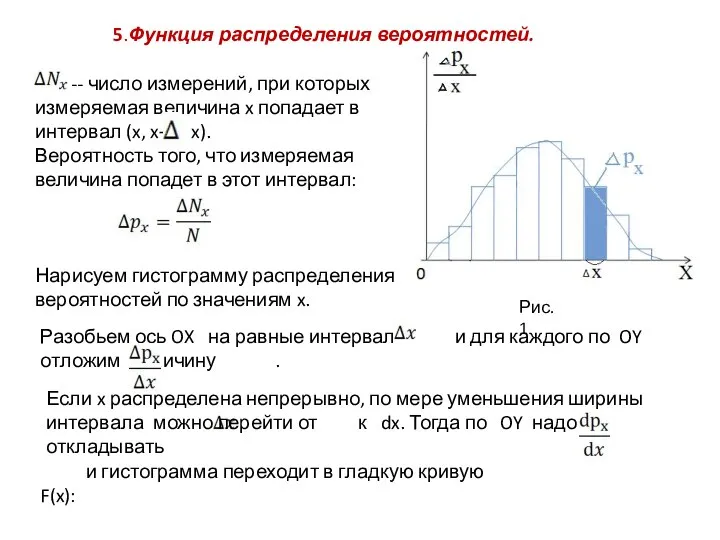
- 22. -- число измерений, при которых измеряемая величина x попадает в интервал (x, x+ x). Вероятность того,
- 23. ) Отсюда -- функция распределения вероятностей появления величины x. Она численно равна относительному числу измерений, которые
- 24. 8. Согласно , среднее значение непрерывно распределенной величины Теперь ее можно выразить через функцию распределения вероятностей:
- 25. Нормальное распределение, также называемое гауссовым распределением или распределением Гаусса — распределение вероятностей, которое играет важнейшую роль
- 26. При приеме в аспирантуру на экзамене часто ставились неразрешимые задачи. Д.Г.Стокс (1819-1903) поставил задачу Максвеллу о
- 27. 3.2 Закон Максвелла для распределения молекул идеального газа по скоростям Поставим задачу об отыскании функции распределения
- 28. Обозначим -- вероятность попадания измеренной скорости молекулы в объем (см. рис.2): Найдем коэффициент пропорциональности из следующих
- 29. В силу равноправия всех направлений в пространстве вид функций должен быть одинаков и отличаться только значениями
- 30. N/j/ aeyrwbz hfcghtltktybz Vfrcdtkkf gj rjvgjytynt crjhjcnb Т.о. функция распределения Максвелла по компоненте скорости имеет экспоненциальный
- 31. Параметр α найдем из следующих соображений. Согласно закону равнораспределения энергии молекулы по степеням свободы , доля
- 32. Подставляя (6) и (7) в (1), получим явный вид распределения Максвелла по компоненте скорости: (8) Такой
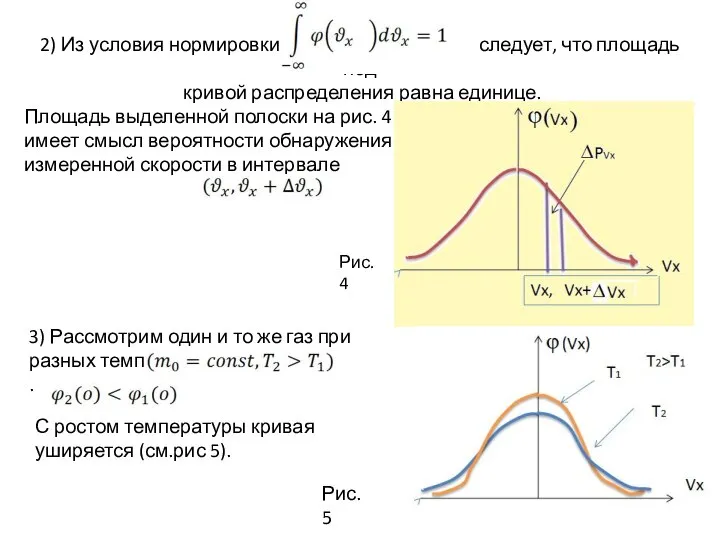
- 33. 2) Из условия нормировки следует, что площадь под кривой распределения равна единице. Площадь выделенной полоски на
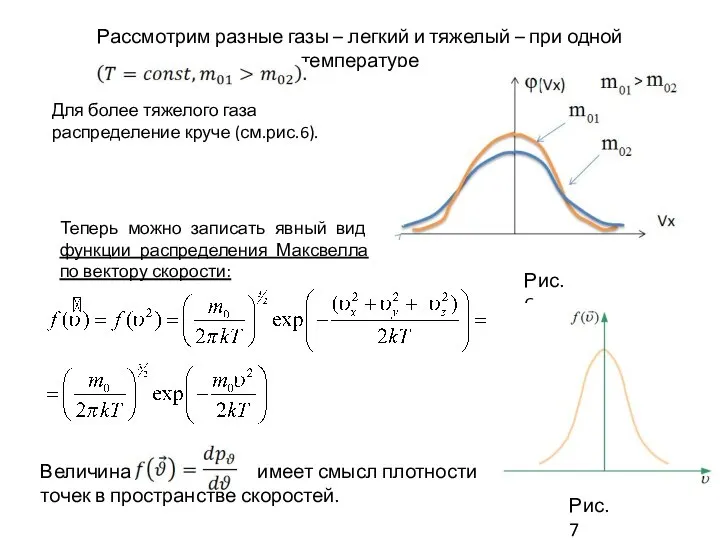
- 34. Рассмотрим разные газы – легкий и тяжелый – при одной температуре Рис.6 Для более тяжелого газа
- 35. 3.2.2 Распределение Максвелла по абсолютному значению скорости В пространстве скоростей (рис.8) концы всех векторов, имеющих одно
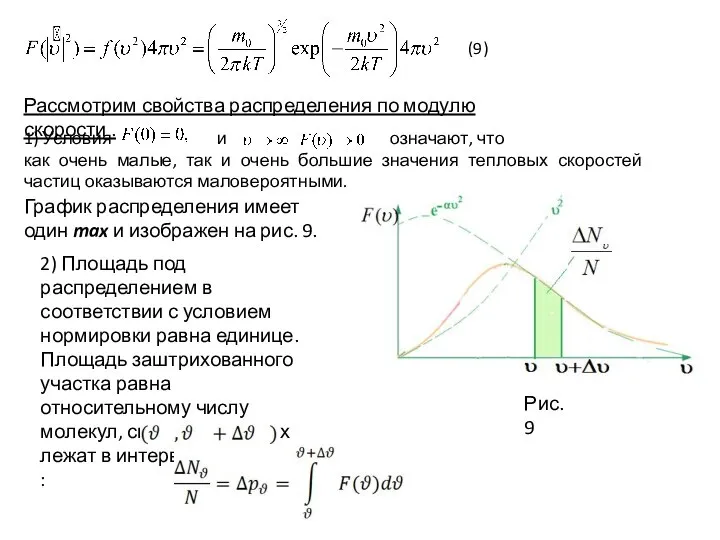
- 36. Рассмотрим свойства распределения по модулю скорости . 1) Условия и означают, что как очень малые, так
- 37. 3) Характерные скорости молекул газа. Наиболее вероятная скорость соответствует максимуму распределения по модулю скорости (см.рис.10) и
- 38. Средняя арифметическая скорость 4)
- 40. Распределение Максвелла по модулю скорости можно преобразовать в распределение частиц по значениям кинетической энергии поступательного движения
- 41. 3.3.1 Барометрическая формула 3.3 Газы в силовом поле В состоянии равновесия при отсутствии внешних силовых полей
- 42. Выражая плотность из уравнения Менделеева-Клапейрона и подставляя её в (1), получим (2). Интегрирование приводит к соотношению
- 43. Барометрическую формулу (5) можно записать в другом виде, используя связь , где - масса одной молекулы
- 44. 3.3.2 РАСПРЕДЕЛЕНИЕ БОЛЬЦМАНА Нетрудно заметить, что в соотношении (6) выражение в показателе экспоненты является потенциальной энергией
- 45. Cледует, однако, помнить, что размеры элементарного объема не могут быть сколь угодно малыми. Этот объем должен
- 47. Поскольку распределения Максвелла и Больцмана статистически независимы, то вероятность обнаружить частицу, обладающую скоростью из интервала .
- 49. Скачать презентацию







































 Квантовая природа электромагнитного излучения. Элементы квантовой механики
Квантовая природа электромагнитного излучения. Элементы квантовой механики Конкурс «Интерактивная мозаика» Pedsovet.su Журун Татьяна Юрьевна Интерактивная презентация сопровождения игры по физике и химии
Конкурс «Интерактивная мозаика» Pedsovet.su Журун Татьяна Юрьевна Интерактивная презентация сопровождения игры по физике и химии  Кристаллические тела и их применение
Кристаллические тела и их применение Теория линейных электрических цепей
Теория линейных электрических цепей Кристаллизация. Ликвация. Метод Бринелля. Метод Роквелла
Кристаллизация. Ликвация. Метод Бринелля. Метод Роквелла Презентация по физике "Источники электрического тока" - скачать _
Презентация по физике "Источники электрического тока" - скачать _ Механиканың физикалық негіздері. Физикалық шамалардың өлшем бірліктері
Механиканың физикалық негіздері. Физикалық шамалардың өлшем бірліктері Выбор мощности компенсирующих устройств
Выбор мощности компенсирующих устройств Специальная теория относительности
Специальная теория относительности Механические колебания и волны. Звук
Механические колебания и волны. Звук Деформация и механические свойства материалов
Деформация и механические свойства материалов Силы в природе
Силы в природе Выполнила Выполнила ученица 11 «А» класса Степаненко Лина
Выполнила Выполнила ученица 11 «А» класса Степаненко Лина  Измерительные приборы.
Измерительные приборы. Закон сохранения импульса Из законов Ньютона можно получить некоторые общие следствия применительно к движению системы тел. М
Закон сохранения импульса Из законов Ньютона можно получить некоторые общие следствия применительно к движению системы тел. М Аттестационная работа. Программа курса по выбору «Мои открытия». (7 класс)
Аттестационная работа. Программа курса по выбору «Мои открытия». (7 класс) Тепловое движение. Температура. Внутренняя энергия
Тепловое движение. Температура. Внутренняя энергия Аттестационная работа. Технология исследовательской деятельности в преподавании физики в рамках реализации ФГОС
Аттестационная работа. Технология исследовательской деятельности в преподавании физики в рамках реализации ФГОС Гидравлический домкрат в быту
Гидравлический домкрат в быту Разрушение. Теоретический предел прочности
Разрушение. Теоретический предел прочности Геометрические характеристики плоских сечений. Лекция 4
Геометрические характеристики плоских сечений. Лекция 4 Физический эксперимент. Статистическая обработка результатов физического эксперимента
Физический эксперимент. Статистическая обработка результатов физического эксперимента Физикалық және химиялық құбылыстар
Физикалық және химиялық құбылыстар Модели радиолокационных сигналов
Модели радиолокационных сигналов Плоское потенциальное движение. Использование вихревой теории в расчетах турбомашин
Плоское потенциальное движение. Использование вихревой теории в расчетах турбомашин Виды излучений
Виды излучений Заготовительные операции ювелирного производства
Заготовительные операции ювелирного производства Презентация по физике "«Последовательное соединение проводников»" - скачать
Презентация по физике "«Последовательное соединение проводников»" - скачать