Содержание
- 2. Основное уравнение молекулярно-кинетической теории идеальных газов Получим уравнение состояния идеального газа, исходя из молекулярно-кинетических представлений. Рассмотрим
- 3. Если n – концентрация молекул в газе, то число молекул в цилиндре равно nΔSvΔt, а импульс,
- 4. здесь - средний квадрат модуля скорости, равный где N – число молекул внутри сосуда, vi –
- 5. Здесь - среднее значение кинетической энергии поступательного движения молекул. Формула (10.3.1) раскрывает физический смысл давления –
- 6. Элементы теории вероятностей При статистическом описании свойств термодинамических систем используются понятия теории вероятностей. Рассмотрим некоторые положения
- 7. Рассмотрим сложное событие, состоящее в том, что в нем обнаруживаются два значения xi и xk в
- 8. Зная результаты измерений случайной величины можно найти ее среднее значение (10.4.4) Пусть теперь случайная величина x
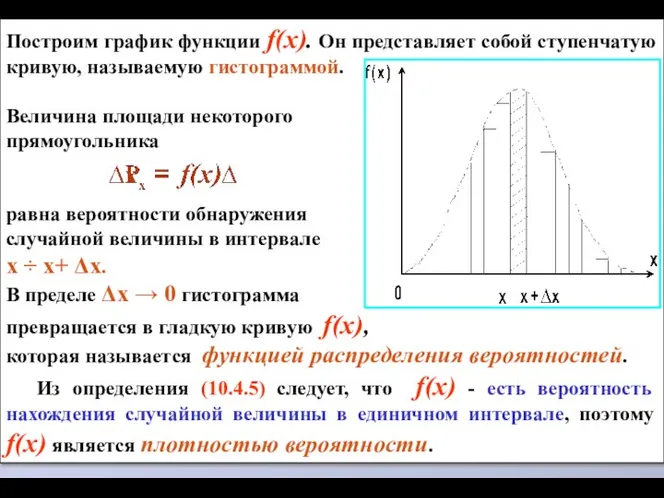
- 9. Построим график функции f(x). Он представляет собой ступенчатую кривую, называемую гистограммой. Величина площади некоторого прямоугольника равна
- 10. Полная вероятность нахождения случайной величины должна равняться 1. Ей отвечает площадь под всей кривой f(x), отсюда
- 11. Рассмотрим идеальный газ. В результате соударений его молекулы находятся в хаотическом движении и беспрерывно меняют направление
- 12. Обозначим плотность точек через f(v) - она равна вероятности того, что модуль скорости молекулы равен значению
- 13. Малый объем dvxdvydvz находится между сферами с радиусами v и v+dv. Объем сферического слоя равен 4πv2dv,
- 14. Разделив dP(v) на dv, находим dP(v)/dv = f(v)4πv2 = F(v) (10.5.3) Функция F(v) - дает вероятность
- 15. Кроме того, проекции скоростей vх, vy, vz являются статистически независимыми друг от друга событиями. Поэтому по
- 16. Возьмем частные производные от последнего выражения. Сначала продифференцируем по vх поскольку то В последнем выражении слева
- 17. Обозначая эту константу через - α , получаем Данное соотношение является дифференциальным уравнением первого порядка, интегрируем
- 18. Аналогичные выкладки дают выражения для других функций Поэтому
- 19. Константу интегрирования С найдем из условия нормировки
- 20. Константу α найдем из расчета средних значений квадратов проекций скорости Такие же значения имеют и ,
- 21. Но ранее, (10.3.2) было получено поэтому Подставляя α в функцию , а последнюю в , получаем
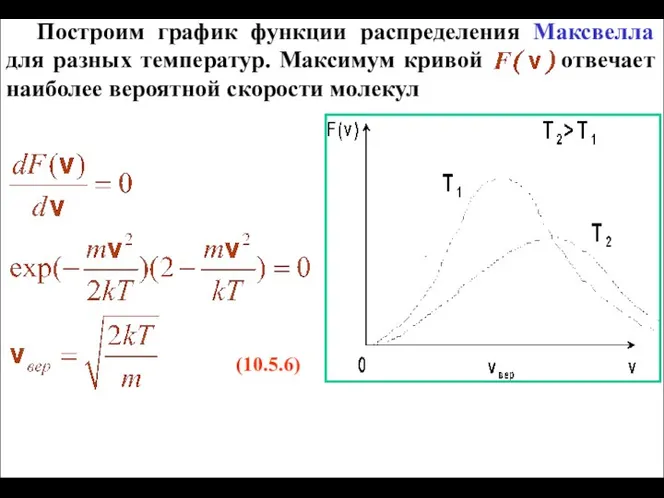
- 22. Построим график функции распределения Максвелла для разных температур. Максимум кривой отвечает наиболее вероятной скорости молекул (10.5.6)
- 23. Определим среднеквадратичную скорость молекулы (10.5.7) и среднюю скорость молекулы (10.5.8) Между этими тремя скоростями имеет место
- 24. Согласно (10.5.2) и (10.5.3) число молекул в сферическом слое с радиусом v и толщиной dv равно
- 26. Скачать презентацию





















 Умники и умницы
Умники и умницы Теория решения изобретательских задач. Законы кинематики
Теория решения изобретательских задач. Законы кинематики Механический резонанс
Механический резонанс электродинамика Лекция 10
электродинамика Лекция 10  Твердотельные лазеры
Твердотельные лазеры Werkstoffkunde
Werkstoffkunde Электрические свойства 2
Электрические свойства 2 Kernfusion in der sonne
Kernfusion in der sonne Электромагнитные взаимодействия, размеры и форма ядер
Электромагнитные взаимодействия, размеры и форма ядер Методы наблюдения и регистрации элементарных частиц
Методы наблюдения и регистрации элементарных частиц Рентгеновское излучение
Рентгеновское излучение Работа и внутренняя энергия
Работа и внутренняя энергия Плавание судов
Плавание судов Механические волны. Звук
Механические волны. Звук Парогенераторы АЭС. Место и роль ПГ в схеме АЭС. (Тема 1)
Парогенераторы АЭС. Место и роль ПГ в схеме АЭС. (Тема 1) Швидкість як фізична якість
Швидкість як фізична якість Методы и режимы интенсивной пластической деформации
Методы и режимы интенсивной пластической деформации Критический диаметр изоляции. Передача теплоты через шаровую стенку
Критический диаметр изоляции. Передача теплоты через шаровую стенку Презентация по физике "Источники звука" - скачать
Презентация по физике "Источники звука" - скачать  Презентация по физике "Метрическая система длин" - скачать
Презентация по физике "Метрическая система длин" - скачать  Газотурбинные установки
Газотурбинные установки Презентация по физике "Электризация тел. Два рода зарядов Лауреат" - скачать
Презентация по физике "Электризация тел. Два рода зарядов Лауреат" - скачать  Презентация Общие принципы и методы научного познания
Презентация Общие принципы и методы научного познания Зависимость ускорения свободного падения от длины нити маятника
Зависимость ускорения свободного падения от длины нити маятника Законы электромагнетизма
Законы электромагнетизма Характеристики атмосферы
Характеристики атмосферы Основи гемодинаміки
Основи гемодинаміки Научно - исследовательская работа «Испарение жидкости. Факторы, влияющие на испарение жидкости»
Научно - исследовательская работа «Испарение жидкости. Факторы, влияющие на испарение жидкости»