Содержание
- 2. 1.1 Внутренняя энергия термодинамической системы. Полная энергия любой т.-д. системы складывается из кинетической энергии движения системы
- 3. 3) Внутренняя энергия является функцией состояния системы. (Функция состояния – это функция, приращение которой не зависит
- 4. Подставив в это выражение , получим: (1.1) Как видно из (1.1), внутренняя энергия идеального газа для
- 5. 1.2 Работа идеального газа при изменении его объема Обмен энергией между т.-д. системой и внешними телами
- 6. dx s P0 F P>P0 Увеличение объема dV=Sdx. Работа положительная, δА>0, так как изменение объёма системы
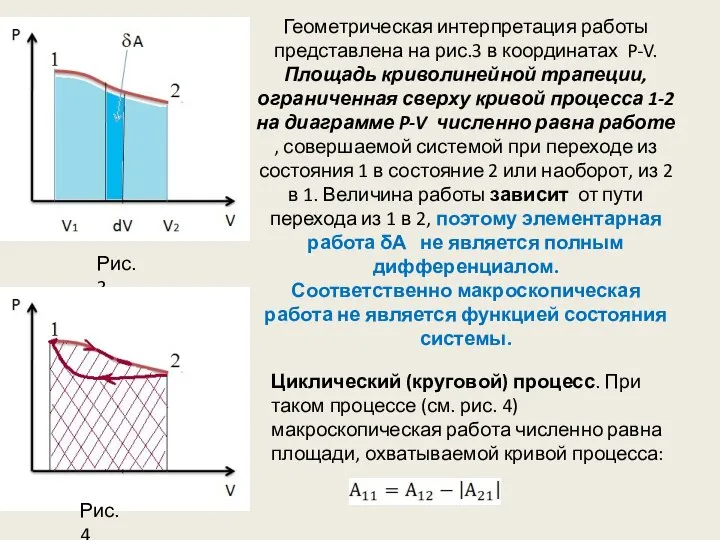
- 7. Геометрическая интерпретация работы представлена на рис.3 в координатах P-V. Площадь криволинейной трапеции, ограниченная сверху кривой процесса
- 8. Рассмотрим работу при некоторых процессах в идеальном газе, при неизменной массе газа (ν=const). 1. Изобарный процесс
- 9. 1.3. Количество теплоты. Обмен энергией между системой и внешней средой может быть не связан с перемещением
- 10. 1.4.. Первое начало термодинамики (Закон сохранения и превращения энергии применительно к тепловым процессам). Количество теплоты, переданное
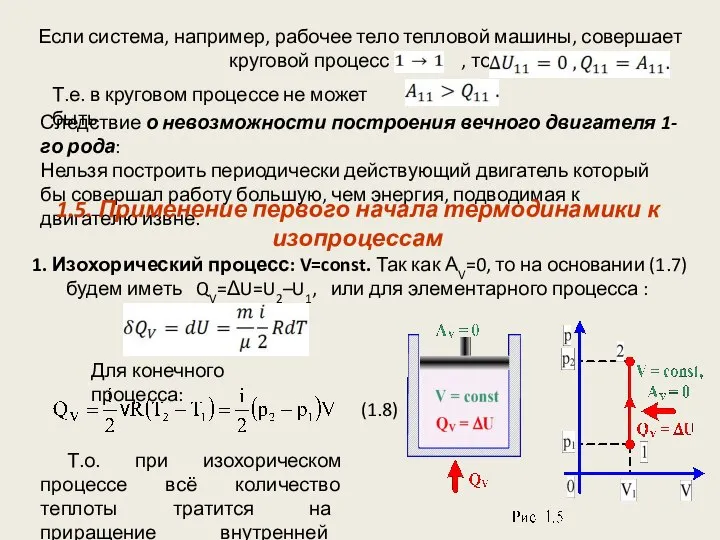
- 11. Если система, например, рабочее тело тепловой машины, совершает круговой процесс , то Т.е. в круговом процессе
- 12. 2. Изобарический процесс: p = const. При изобарическом процессе изменяется и температура и объем газа. Следовательно
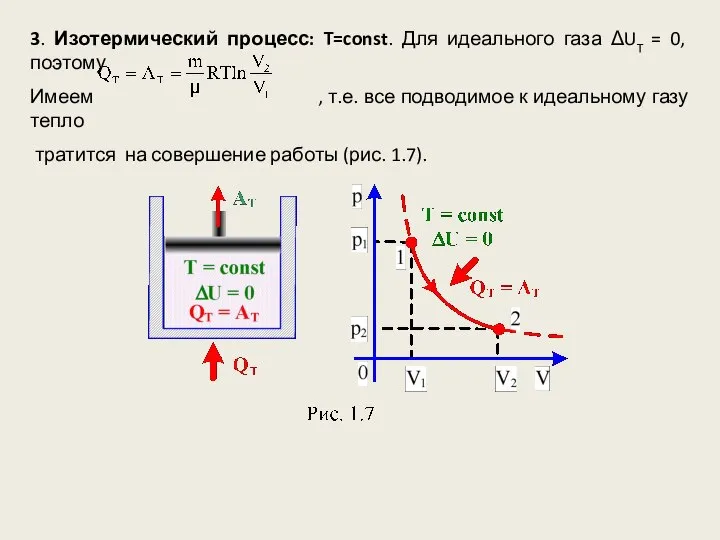
- 13. 3. Изотермический процесс: T=const. Для идеального газа ΔUT = 0, поэтому Имеем , т.е. все подводимое
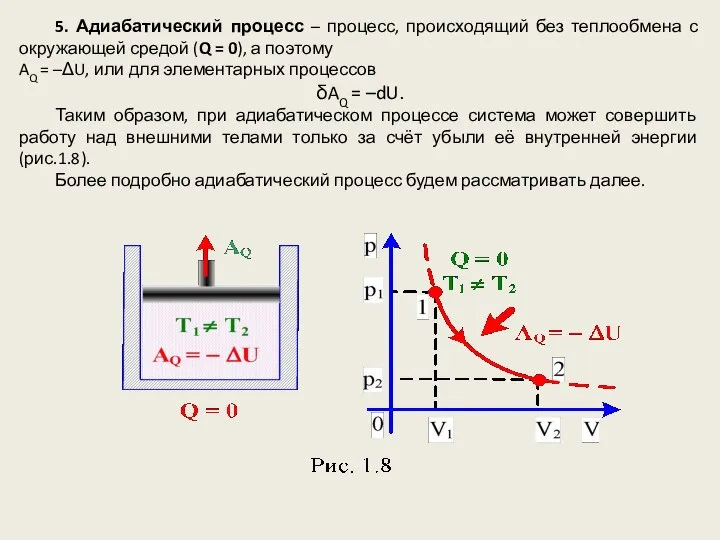
- 14. 5. Адиабатический процесс – процесс, происходящий без теплообмена с окружающей средой (Q = 0), а поэтому
- 15. 1.6 Теплоемкость системы. Классическая теория теплоемкости и ее ограниченность. Теплоемкостью системы называется величина, равная количеству теплоты
- 16. Из (1.11) и (1.12) следует Учитывая, что , из последнего выражения получим связь удельной и молярной
- 17. 3) Изобарический процесс. P=const. (1.15) Это соотношение называется уравнением Майера. Из него видно что всегда на
- 18. Итак, согласно изложенной классической теории теплоемкости, молярная теплоемкость идеального газа при V=const независимо от природы газа
- 19. При низких температурах для поведения молекул характерно поступательное движение (участок I), по мере роста температуры (нормальные
- 20. Энергетические уровни, соответствующие определенному виду движения, возбуждаются в среднем при температурах не ниже: которые находятся в
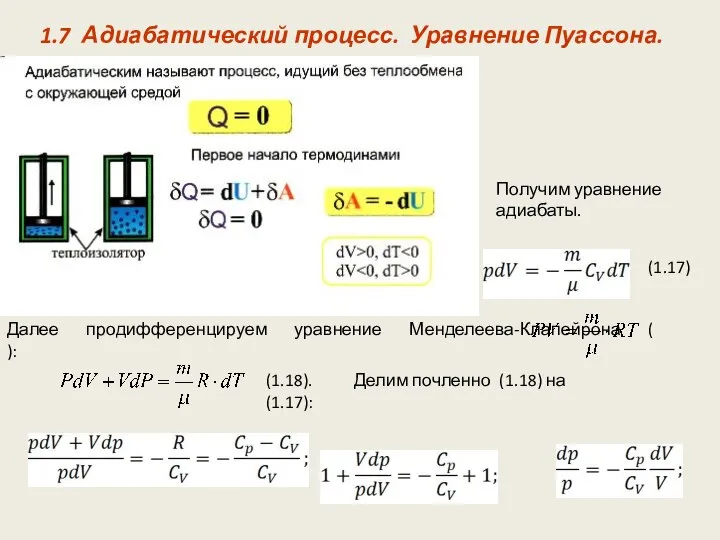
- 21. 1.7 Адиабатический процесс. Уравнение Пуассона. Далее продифференцируем уравнение Менделеева-Клапейрона ( ): (1.17) (1.18). Делим почленно (1.18)
- 22. Отношение теплоемкостей (1.19) называется показателем адиабаты, характерной для каждого газа величиной, зависящей только от числа степеней
- 23. Уравнению (1.20 )можно придать другой вид, используя уравнение Менделеева-Клапейрона. Выразим из уравнения М.-К. давление и подставим
- 24. PS. Применять уравнение Пуассона к реальным процессам надо с осторожностью, так как необходимо здесь выполнение двух
- 26. Скачать презентацию


















 КПД тепловой машины
КПД тепловой машины Молекулярная физика
Молекулярная физика Лампы накаливания и электрические нагревательные приборы
Лампы накаливания и электрические нагревательные приборы  Статическое электричество
Статическое электричество Колебательные процессы. Лекция 16
Колебательные процессы. Лекция 16 Простые механизмы
Простые механизмы Три состояния вещества. Различие в молекулярном строении твердых тел, жидкостей и газов. Учитель физики ГБОУ СОШ № 128 г.Санкт-Пете
Три состояния вещества. Различие в молекулярном строении твердых тел, жидкостей и газов. Учитель физики ГБОУ СОШ № 128 г.Санкт-Пете Переменный ток. Метод симметричных составляющих
Переменный ток. Метод симметричных составляющих Законы сохранения энергии и импульса
Законы сохранения энергии и импульса Энергия. Кинетическая и потенциальная энергия. Вывод закона сохранения механической энергии
Энергия. Кинетическая и потенциальная энергия. Вывод закона сохранения механической энергии Транспортные системы ОФ. Расчет ленточного питателя
Транспортные системы ОФ. Расчет ленточного питателя ПРЕЗЕНТАЦИЯ по теме: «Фотоэффект»
ПРЕЗЕНТАЦИЯ по теме: «Фотоэффект»  Электростатические спектрометры заряженных частиц
Электростатические спектрометры заряженных частиц Магнитные подшипники
Магнитные подшипники Способи охолоджування приміщень
Способи охолоджування приміщень Расчет электрических сетей напряжением до 1 кВ
Расчет электрических сетей напряжением до 1 кВ Мирное применение ядерной энергии
Мирное применение ядерной энергии Аттестационная работа. Проектно - исследовательская работа Радуга цвета. Явление радуги
Аттестационная работа. Проектно - исследовательская работа Радуга цвета. Явление радуги Законы сохранения в механике
Законы сохранения в механике Применение производной в физике
Применение производной в физике Сварочное производство
Сварочное производство  Artificial communication satellites
Artificial communication satellites Электроны. История открытия.
Электроны. История открытия. Проекция силы на ось
Проекция силы на ось Презентация по физике "Измерение высоты здания разными способами" - скачать
Презентация по физике "Измерение высоты здания разными способами" - скачать  Потенциальная энергия
Потенциальная энергия Автоматизация процесса регулировки манометров
Автоматизация процесса регулировки манометров Приёмники оптического излучения
Приёмники оптического излучения