Содержание
- 2. МОЛЕКУЛЯРНАЯ ФИЗИКА ТЕРМОДИНАМИКА Сегодня *
- 3. Тема 4 ПЕРВОЕ НАЧАЛО ТЕРМОДИНАМИКИ 4.1. Внутренняя энергия. Работа и теплота 4.2. Теплоёмкость идеального газа Уравнение
- 4. 4.1. Внутренняя энергия. Работа и теплота Наряду с механической энергией любое тело (или система) обладает внутренней
- 5. В термодинамических процессах изменяется только кинетическая энергия движущихся молекул (тепловой энергии недостаточно, чтобы изменить строение атома,
- 6. Внутренняя энергия U одного моля идеального газа равна: или Таким образом, внутренняя энергия зависит только от
- 7. Понятно, что в общем случае термодинамическая система может обладать как внутренней, так и механической энергией и
- 8. Например, зимой вы бросили в снег горячий камень. За счёт запаса потенциальной энергии совершена механическая работа
- 9. Итак, работа и теплота не есть особые формы энергии. Нельзя говорить о запасе теплоты или работы.
- 10. Можно найти ещё массу примеров диссипации или превращения одной формы энергии в другую. Опыт показывает, что
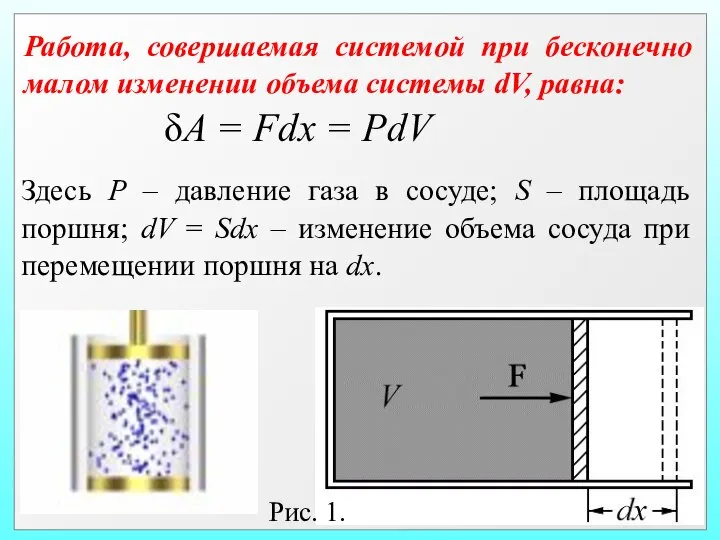
- 11. Количество теплоты, сообщаемой телу, идёт на увеличение внутренней энергии и на совершение телом работы: (4.1.1) –
- 12. Правило знаков: если тепло передаётся от окружающей среды данной системе, и если система производит работу над
- 14. Закон сохранения энергии для малого изменения состояния системы будет иметь вид: (4.1.2) U – функция состояния
- 15. В каждом состоянии система обладает определенным и только таким значением внутренней энергии, поэтому можно записать Так
- 16. Теплота Q и работа А зависят от того, каким образом совершен переход из состояния 1 в
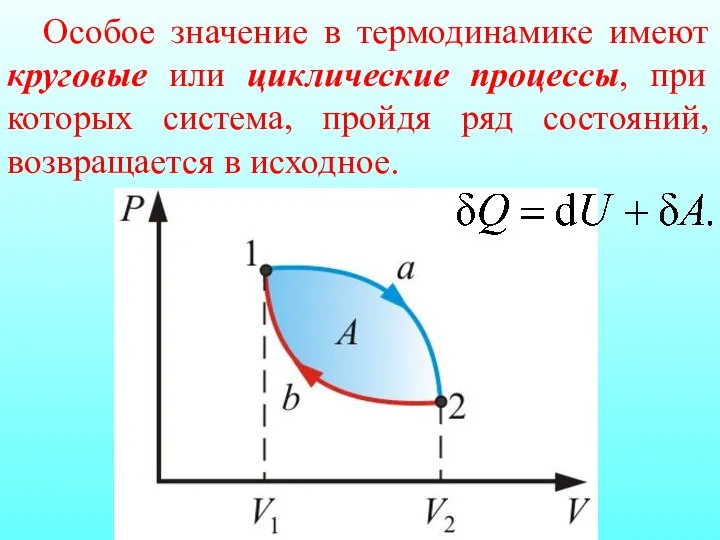
- 17. Особое значение в термодинамике имеют круговые или циклические процессы, при которых система, пройдя ряд состояний, возвращается
- 18. Если то согласно первому началу термодинамики т.е. нельзя построить периодически действующий двигатель, который совершал бы бóльшую
- 19. К недостаткам первого начала следует отнести то, что: первое начало термодинамики не указывает, в каком направлении
- 20. 4.2. Теплоёмкость идеального газа. Теплоёмкость тела характеризуется количеством теплоты, необходимой для нагревания этого тела на один
- 21. Удельная теплоёмкость Суд – есть количество теплоты, необходимое для нагревания единицы массы вещества на 1 градус
- 22. Молярная масса – масса одного моля: где А – атомная масса; mед − атомная единица массы;
- 23. Теплоёмкость термодинамической системы зависит от того, как изменяется состояние системы при нагревании. Если газ нагревать при
- 24. СР – теплоемкость при постоянном давлении. Если нагревать газ при постоянном давлении Р в сосуде с
- 26. Следовательно, проводимое тепло затрачивается и на нагревание и на совершение работы. Отсюда ясно, что Итак, проводимое
- 27. Пусть мы нагреваем один моль идеального газа при постоянном объёме. Тогда, первое начало термодинамики, запишем в
- 28. В общем случае (4.2.4) так как U может зависеть не только от температуры. В случае идеального
- 29. Внутренняя энергия идеального газа является только функцией температуры (и не зависит от V, Р и тому
- 30. При изобарическом процессе кроме увеличения внутренней энергии происходит совершение работы газом: (4.2.7) Из основного уравнения молекулярно-кинетической
- 31. Это уравнение Майера для одного моля газа. Из него следует, что физический смысл универсальной газовой постоянной
- 32. Отсюда получим формулу Майера для удельных теплоёмкостей: (4.2.9) Т.к.
- 33. 4.3. Теплоёмкости одноатомных и многоатомных газов Внутренняя энергия одного моля идеального газа равна (4.3.1)
- 34. Теплоёмкости одноатомных газов теплоемкость при постоянном объеме СV – величина постоянная, от температуры не зависит.
- 35. Учитывая физический смысл R для изобарических процессов можно записать: (4.3.3) (для одного моля). Отсюда Тогда, теплоемкость
- 36. - постоянная адиабаты (коэффициент Пуассона)
- 37. Так как Тогда Из этого следует, что (4.3.5) Кроме того , где i – число степеней
- 38. Подставив в выражение для внутренней энергии, получим: а так как , то внутреннюю энергию можно найти
- 39. То, что , хорошо подтверждается на опыте с Ne, He, Ar, Kr, парами одноатомных металлов.
- 40. Теплоемкости многоатомных газов Опыты с двухатомными газами такими как азот, кислород и др. показали, что Для
- 41. Необходимо учитывать вращательное движение молекул и число степеней свободы этих молекул. Молекулы многоатомных газов нельзя рассматривать
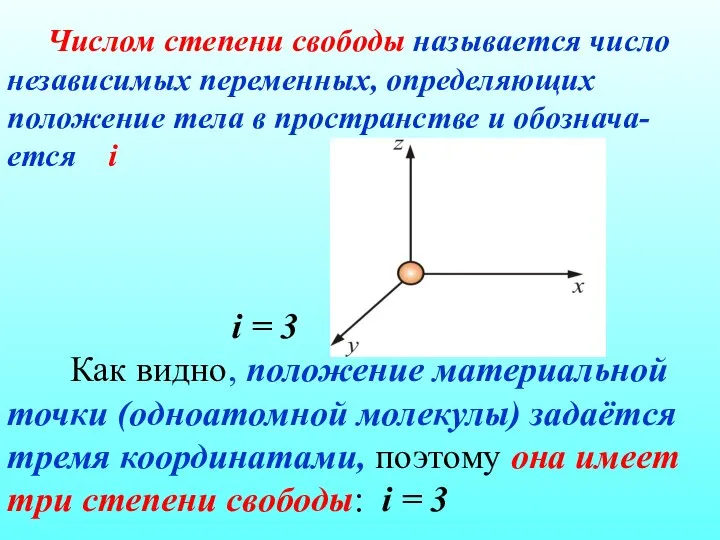
- 42. Числом степени свободы называется число независимых переменных, определяющих положение тела в пространстве и обознача-ется i i
- 43. Многоатомная молекула может ещё и вращаться. Например, у двухатомных молекул вращательное движение можно разложить на два
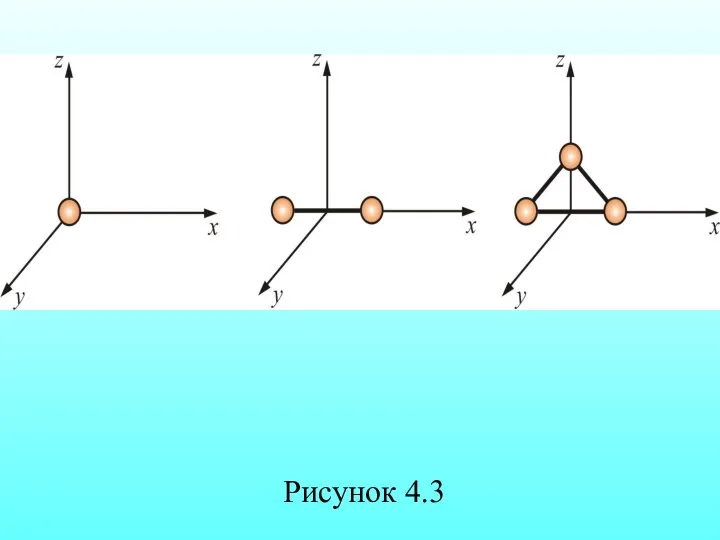
- 44. Рисунок 4.3
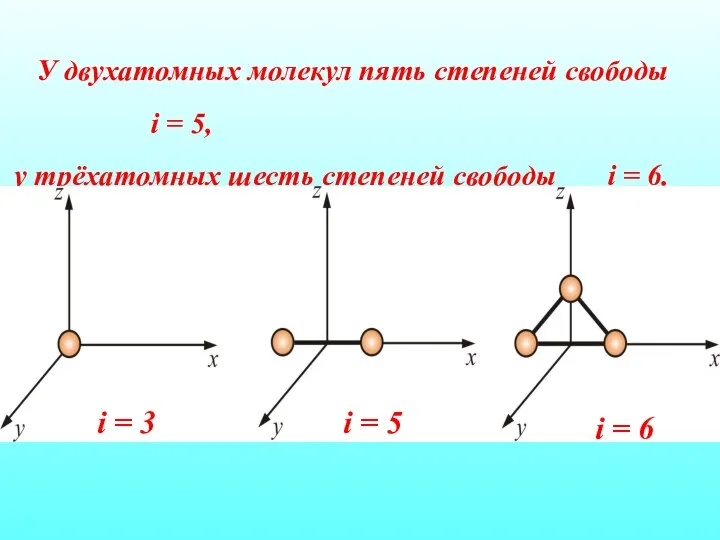
- 47. У двухатомных молекул пять степеней свободы i = 5, у трёхатомных шесть степеней свободы i =
- 48. При взаимных столкновениях молекул возможен обмен их энергиями и превращение энергии вращательного движения в энергию поступательного
- 49. Больцман доказал, что, средняя энергия приходящаяся на одну степень свободы равна 4.4. Закон о равномерном распределении
- 50. Итак, средняя энергия приходящаяся на одну степень свободы: (4.4.1)
- 51. У одноатомной молекулы i = 3, тогда (4.4.2) для двухатомных молекул i = 5 (4.4.3) для
- 52. На среднюю кинетическую энергию молекулы, имеющей i-степеней свободы приходится (4.4.5) Это и есть закон Больцмана о
- 54. для трехатомных молекул: . При этом: для двухатомных молекул:
- 55. В общем случае, для молярной массы газа (4.4.6) (4.4.7)
- 56. Для произвольного количества газов: , (4.4.9) (4.4.10) Из теории также следует, что СV не зависит от
- 57. Рисунок 4.4
- 58. Для одноатомных газов это выполняется в очень широких пределах, а для двухатомных газов только в интервале
- 59. Одна колебательная степень свободы несет энергии, так как при этом есть и кинетическая и потенциальная энергия,
- 60. 4.5. Применение первого начала термодинамики к изопроцессам идеальных газов В таблице (4.1) приводятся сводные данные о
- 61. Таблица 4.1 δQ = 0 Закон Шарля Закон Гей-Люссака Закон Бойля – Мариотта
- 65. Здесь уместно рассмотреть еще и политропный процесс – такой процесс, при котором изменяются все основные параметры
- 66. С помощью показателя n можно легко описать любой изопроцесс: 1. Изобарный процесс Р = const, n
- 67. 4. Адиабатический процесс ΔQ = 0, n = γ, Сад = 0. Во всех этих процессах
- 68. Рис. 1.
- 72. Скачать презентацию
































































 Конвективный теплообмен
Конвективный теплообмен Презентация по физике "Производство, передача и потребление электроэнергии" - скачать
Презентация по физике "Производство, передача и потребление электроэнергии" - скачать  Воздух, какой он
Воздух, какой он Посвящение в юные физики
Посвящение в юные физики Воздействие лазерного излучения на мишени
Воздействие лазерного излучения на мишени Составитель: Гринякин Станислав Александрович Руководитель: Талалай Ольга Георгиевна, учитель физики
Составитель: Гринякин Станислав Александрович Руководитель: Талалай Ольга Георгиевна, учитель физики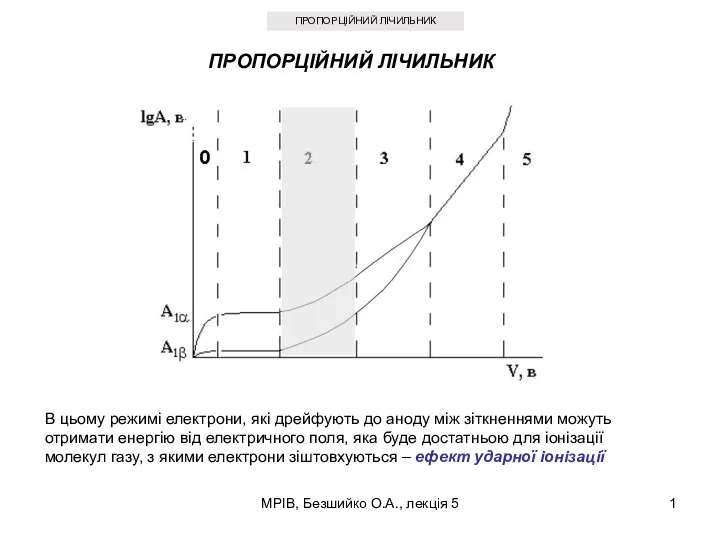 Пропорційний лічильник
Пропорційний лічильник Медициналық интроскопияның негізгі техникалық құралдары. Фотоэлектрлік түрлендіргіштер
Медициналық интроскопияның негізгі техникалық құралдары. Фотоэлектрлік түрлендіргіштер Обзор доказательств ложности утверждений о возможности самосовершенствования
Обзор доказательств ложности утверждений о возможности самосовершенствования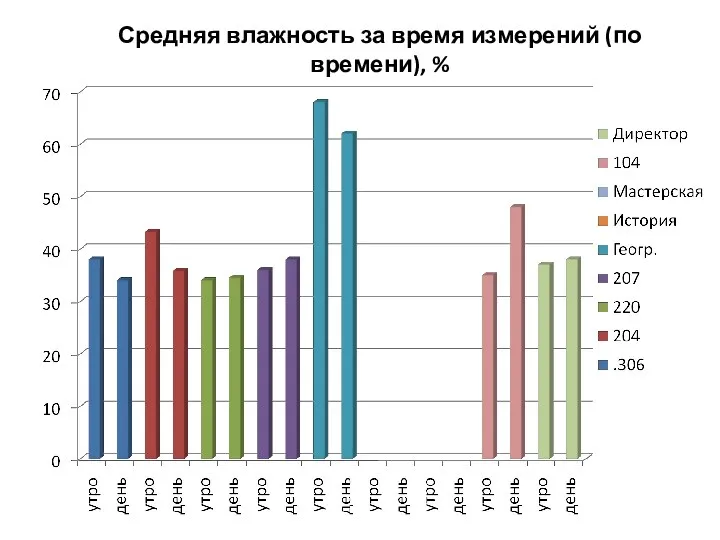 Таблицы. Средняя влажность за время измерений (по времени), %
Таблицы. Средняя влажность за время измерений (по времени), % Плоское движение капсулы в атмосфере
Плоское движение капсулы в атмосфере Гипотеза де Бройля. Дифракция электронов. Микрочастица в двухщелевом интерферометре. Соотношение неопределенностей Гейзенберга
Гипотеза де Бройля. Дифракция электронов. Микрочастица в двухщелевом интерферометре. Соотношение неопределенностей Гейзенберга Электрический ток в газах
Электрический ток в газах Сложение сил. Равнодействующая сил. Физика 7 класс
Сложение сил. Равнодействующая сил. Физика 7 класс Приведение системы сил к данному центру
Приведение системы сил к данному центру История русской философии Западники
История русской философии Западники Проект: Вычисление реагентов расходуемых за год. год.
Проект: Вычисление реагентов расходуемых за год. год.  Прямолинейные колебания точки
Прямолинейные колебания точки Общие указания к построению эпюр поперечных сил и изгибающих моментов
Общие указания к построению эпюр поперечных сил и изгибающих моментов Как можно избежать действия электрического тока при случайном прикосновении к электроприбору, которое оказалось под напряжением?
Как можно избежать действия электрического тока при случайном прикосновении к электроприбору, которое оказалось под напряжением? Исследование гиратора на основе слоистой структуры феррит никеля–метглас–цирконат-титанат свинца
Исследование гиратора на основе слоистой структуры феррит никеля–метглас–цирконат-титанат свинца Сила упругости. Закон Гука
Сила упругости. Закон Гука Тректі мембраналарды алу: иондардың зат арқылы жүруі
Тректі мембраналарды алу: иондардың зат арқылы жүруі Модели атомов. Опыт Резерфорда. Презентация по физике
Модели атомов. Опыт Резерфорда. Презентация по физике История развития телевидения
История развития телевидения Презентация Тепловые электростанции
Презентация Тепловые электростанции  Ортогональное частотное разделение со многими поднесущими (OFDM)
Ортогональное частотное разделение со многими поднесущими (OFDM) Структурный анализ и синтез механизмов
Структурный анализ и синтез механизмов