Содержание
- 2. Тема: « Первый закон термодинамики. Применение первого закона термодинамики к различным процессам». У него особая история
- 3. 1736 год - паровая лодка
- 4. 1770 год – паровая повозка
- 5. 1775 год - отказ Парижской Академии наук принимать проекты вечных двигателей
- 6. 1807 год - пароход Фултона
- 7. 1824 год – паровоз Стефенсона
- 8. 1842 год - статья Роберта Майера “Замечания о силах неживой природы”
- 9. Формула закона сложна, но будет понятна на простых примерах. Когда человек болеет у него поднимается температура,
- 10. И это будет ещё более логично, если учесть, что этот закон открыл ученый, по образованию врач.
- 11. Первый закон термодинамики – закон сохранения энергии, связанный с тепловыми явлениями. Этот закон показывает от чего
- 12. N: Кузнец ударяет молотом по куску железа – железо нагревается N: Искры от забивания гвоздя N:
- 13. Закон сохранения энергии. Количество энергии неизменно, она не возникает из ничего и не исчезает, она только
- 14. Этот закон был открыт в середине XIX в. немецким учёным, врачом по образованию Юлиусом Робертом фон
- 15. Изменение внутренней энергии системы при переходе её из одного состояния в другое равно сумме работы внешних
- 16. Изолированная система: А = 0 Q = 0 ΔU = U2 - U1 = 0, или
- 17. Вид работы в термодинамике А - работы внешних тел над системой А' - работу системы над
- 18. Q = ΔU + А' Количество теплоты, переданной системе, идёт на изменение её внутренней энергии и
- 19. Отсюда вытекает невозможность создания вечного двигателя, т.к. если к системе не поступает тепло (Q = 0),
- 20. Работа и количество теплоты характеристики процесса изменения внутренней энергии В данном состоянии система всегда обладает определённой
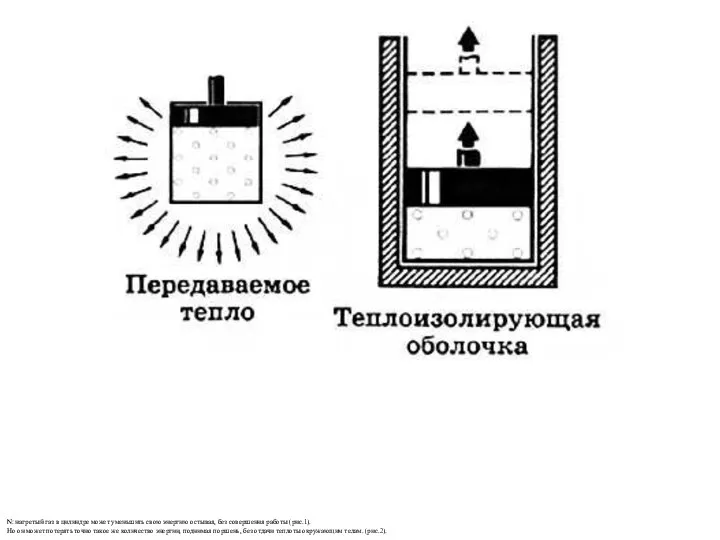
- 21. N: нагретый газ в цилиндре может уменьшить свою энергию остывая, без совершения работы (рис.1). Но он
- 22. Изохорный процесс Рассмотрим и запишем различные процессы, при которых одна из физических величин, характеризующих состояние газа,
- 23. Изохорный процесс нагревание ΔU = Q Q > 0 и ΔU > 0 U ↑ Объём
- 24. Изохорный процесс охлаждение Q ΔU = U2 - U1 U ↓ При охлаждении газа Q
- 25. Изотермический процесс Получение тепла Q = А' Q > 0, то А' > 0 (Т =
- 26. Изотермический процесс отдача тепла Q Если, напротив, газ отдаёт тепло окружающей среде (термостату), то Q Работа
- 27. Изобарный процесс Q = ΔU + А' = ΔU + pΔV. При изобарном процессе передаваемое газу
- 28. Адиабатный процесс процесс, происходящий без теплообмена с окружающей средой. ΔU = А При адиабатном процессе изменение
- 29. Задачи. Закон термодинамики 1. Идеальный газ получил количество теплоты, равное 300 Дж, и совершил работу, равную
- 30. Задачи. Закон термодинамики 2. Идеальный газ совершил работу, равную 100 Дж, и отдал количество теплоты, равное
- 31. Задачи. Закон термодинамики 3. Идеальный газ совершил работу, равную 300 Дж. При этом внутренняя энергия уменьшилась
- 32. Задачи. Закон термодинамики 4. При изотермическом расширении идеальным газом совершена работа 15 кДж. Какое количество теплоты
- 33. Задачи. Закон термодинамики 5. В закрытом баллоне находится газ. При охлаждении его внутренняя энергия уменьшилась на
- 34. Первый закон термодинамики Изменение внутренней энергии системы при переходе её из одного состояния в другое равно
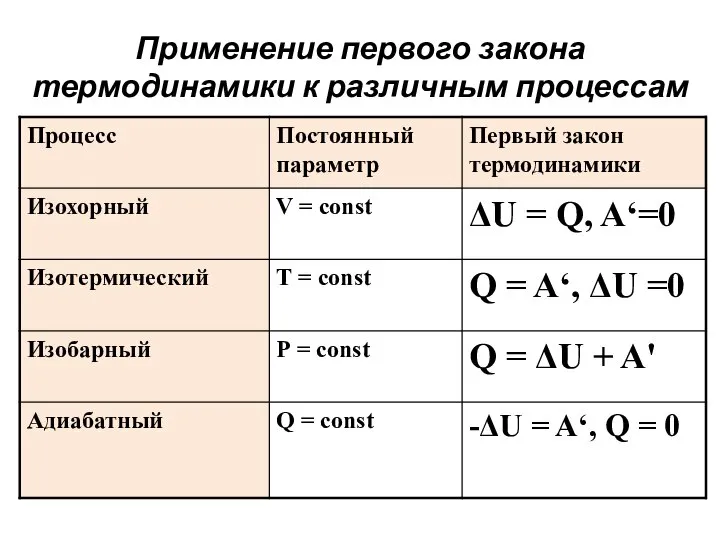
- 35. Применение первого закона термодинамики к различным процессам
- 36. Закрепление материала Для изобарного нагревания газа, количество вещества которого 800 моль, на 500 К ему сообщили
- 38. Скачать презентацию

































 Раздел физики - термодинамика
Раздел физики - термодинамика Закон сохранения импульса
Закон сохранения импульса Открытие электромагнитной индукции
Открытие электромагнитной индукции Почему шуршит пакетик
Почему шуршит пакетик Элементарные частицы. Материя. Бозон Хиггса. Переносчики взаимодействий
Элементарные частицы. Материя. Бозон Хиггса. Переносчики взаимодействий Магнитные подшипники
Магнитные подшипники Табиғи үдерістерді физика, химия, механика, тағы басқа жаратылыстану ғылымдары зерттейді
Табиғи үдерістерді физика, химия, механика, тағы басқа жаратылыстану ғылымдары зерттейді Источники электропитания
Источники электропитания Упругие свойства твёрдых тел. Гидродинамика
Упругие свойства твёрдых тел. Гидродинамика Многовибраторные проволочные антенны
Многовибраторные проволочные антенны Наноматеріали
Наноматеріали Электро-магнитные волны. Лекция 7
Электро-магнитные волны. Лекция 7 Внутренняя энергия. Первый закон термодинамики
Внутренняя энергия. Первый закон термодинамики Конденсаторы. Электроёмкость конденсатора. Энергия заряжённого конденсатора. Применение конденсаторов
Конденсаторы. Электроёмкость конденсатора. Энергия заряжённого конденсатора. Применение конденсаторов ЭЛЕКТРИЧЕСКИЕ ПРОВОДА
ЭЛЕКТРИЧЕСКИЕ ПРОВОДА Технические открытия и изобретения.
Технические открытия и изобретения. Характеристики спектров кристаллов
Характеристики спектров кристаллов Технологические и художественные особенности изготовления нагрудного украшения Танец стерхов
Технологические и художественные особенности изготовления нагрудного украшения Танец стерхов Презентация по физике "Измерение атмосферного давления 7 класс" - скачать
Презентация по физике "Измерение атмосферного давления 7 класс" - скачать  Теплотехника. Термодинамические основы работы тепловых машин
Теплотехника. Термодинамические основы работы тепловых машин Термодинамика. Основа термодинамики
Термодинамика. Основа термодинамики Презентация по физике "Никола Тесла" - скачать бесплатно
Презентация по физике "Никола Тесла" - скачать бесплатно Будова атома. Закріпити знання про будову атома. Узагальнити знання про стан електронів у атомі
Будова атома. Закріпити знання про будову атома. Узагальнити знання про стан електронів у атомі Тепловые двигатели и охрана окружающей среды
Тепловые двигатели и охрана окружающей среды Динамика твердого тела. Лекция 10: Метод кинетостатики
Динамика твердого тела. Лекция 10: Метод кинетостатики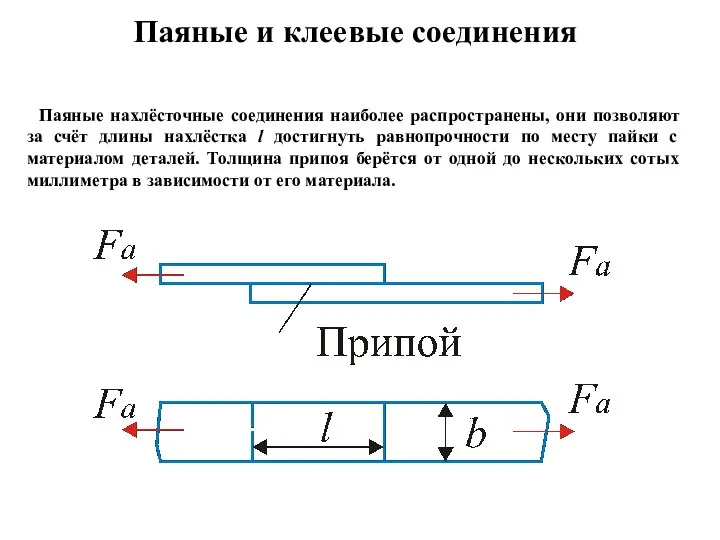 Паяные и клеевые соединения
Паяные и клеевые соединения Фотографический процесс в лучевой диагностике
Фотографический процесс в лучевой диагностике Запишите формулу
Запишите формулу