Содержание
- 2. Подумай… 1. Чем отличаются молекулы холодной и горячей воды? 2. Изменяется ли температура в процессе плавления?
- 3. Проверь себя: 1. Молекулы холодной и горячей воды отличаются только скоростью движения и расстоянием между ними.
- 4. Испарением называется парообразование, происходящее с поверхности жидкости. Кипением называется интенсивное парообразование, происходящее при температуре кипения жидкости.
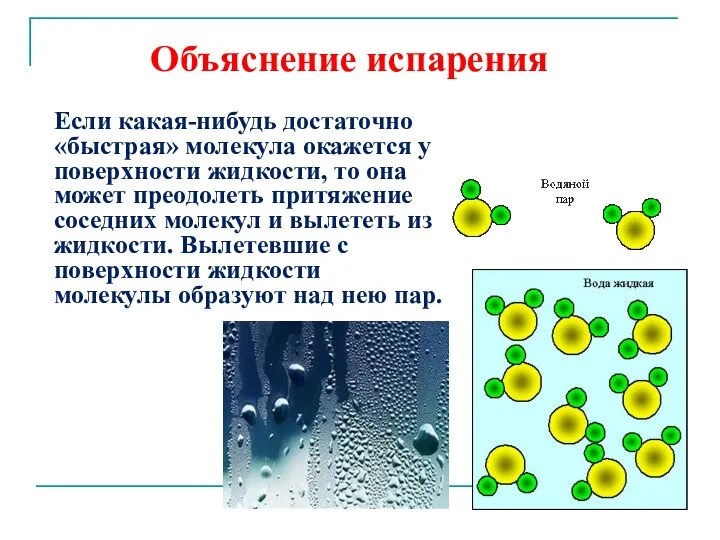
- 5. Объяснение испарения Если какая-нибудь достаточно «быстрая» молекула окажется у поверхности жидкости, то она может преодолеть притяжение
- 6. Испарение в природе
- 7. Объяснение кипения При нагревании в жидкости появляются мелкие пузырьки, количество которых быстро растёт. Это пузырьки воздуха,
- 8. Особенности кипения 1.Кипение всегда происходит при определенной для каждого вещества температуре – температуре кипения. 2.Во время
- 9. Расчёт количества теплоты Количество теплоты, необходимое для парообразования, зависит от рода вещества и его массы: Q
- 10. Какое количество теплоты требуется для испарения 200 г воды, взятой при температуре 200С? В задаче описано
- 12. Скачать презентацию








 Теплофизические основы высокотемпературных технологий
Теплофизические основы высокотемпературных технологий Квантовая физика. Фотоэффект. Теория фотоэффекта
Квантовая физика. Фотоэффект. Теория фотоэффекта ЭЛЕКТРОМАГНИТНАЯ ПРИРОДА СВЕТА
ЭЛЕКТРОМАГНИТНАЯ ПРИРОДА СВЕТА  Тепловое излучение и люминесценция
Тепловое излучение и люминесценция Равноускоренное движение. Ускорение
Равноускоренное движение. Ускорение Презентация по физике "Я познаю мир" - скачать
Презентация по физике "Я познаю мир" - скачать  Выполнила ученица 10 класса: Елагина М.В. Проверила: Васильева М.В.
Выполнила ученица 10 класса: Елагина М.В. Проверила: Васильева М.В. Фізика в побуті, в техніці, в виробництві
Фізика в побуті, в техніці, в виробництві Ремонт задвижной арматуры
Ремонт задвижной арматуры Основные положения молекулярно-кинетической теории
Основные положения молекулярно-кинетической теории Электромагнитные волны. Свойства электромагнитных волн. 11 класс
Электромагнитные волны. Свойства электромагнитных волн. 11 класс Физика пәнінде оптиканың орны және басқа пәндермен байланысы. Жарықтың электромагниттік табиғаты. Лекция 1
Физика пәнінде оптиканың орны және басқа пәндермен байланысы. Жарықтың электромагниттік табиғаты. Лекция 1 Роль физики в жизни кошки
Роль физики в жизни кошки Вопросы безопасности атомных электростанций с реакторами ВВЭР-1200
Вопросы безопасности атомных электростанций с реакторами ВВЭР-1200 Потенциальные течения
Потенциальные течения Количество теплоты
Количество теплоты Тема 3 -БИОЛОГИЧЕСКИЕ ЭФФЕКТЫ ВОЗДЕЙСТВИЯ ИОНИЗИРУЮЩИХ ИЗЛУЧЕНИЙ
Тема 3 -БИОЛОГИЧЕСКИЕ ЭФФЕКТЫ ВОЗДЕЙСТВИЯ ИОНИЗИРУЮЩИХ ИЗЛУЧЕНИЙ  Планетарная модель атома. Ядерная модель атома. Квантовые постулаты Бора
Планетарная модель атома. Ядерная модель атома. Квантовые постулаты Бора Ультрафиолетовое Излучение
Ультрафиолетовое Излучение Совет мудрецов
Совет мудрецов Тепловое излучение тел
Тепловое излучение тел Интерференция света
Интерференция света Презентация по физике Физика твердого тела
Презентация по физике Физика твердого тела  Генератор переменного тока, трансформатор
Генератор переменного тока, трансформатор Структура и взаимодействие адронов
Структура и взаимодействие адронов Молекулярная физика. Термодинамика
Молекулярная физика. Термодинамика Презентация по физике "Чудеса, имеющие реальную основу" - скачать
Презентация по физике "Чудеса, имеющие реальную основу" - скачать 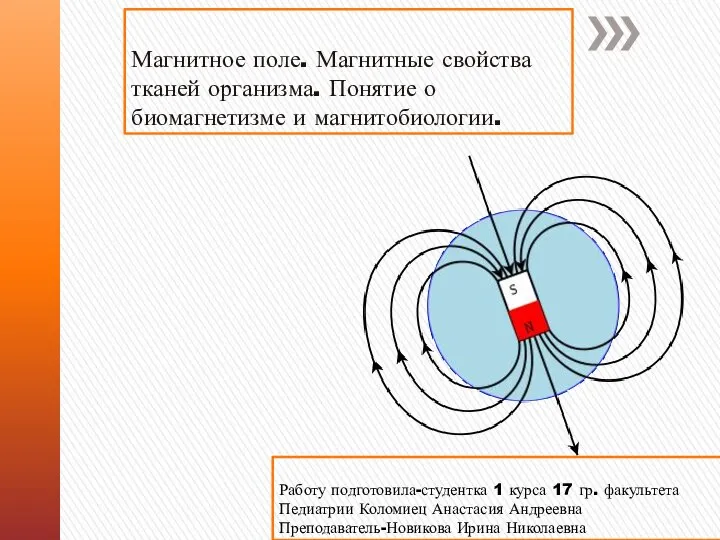 Магнитное поле. Магнитные свойства тканей организма. Понятие о биомагнетизме и магнитобиологии
Магнитное поле. Магнитные свойства тканей организма. Понятие о биомагнетизме и магнитобиологии