Содержание
- 2. 1. Газ Ван-дер-Ваальса Уравнение Клапейрона-Менделеева достаточно хорошо описывает газ при высоких температурах и низких давлениях, когда
- 3. Учет конечных размеров молекул приводит к тому, что объем, доступный для свободного движения молекул, оказывается меньше
- 4. Теперь учтем силы взаимного притяжения молекул. Давления, обусловленного силами молекулярного притяжения, давление газа на стенку будет
- 5. Величины а и b в этом уравнении для каждого газа могут быть измерены экспериментально. Так, если
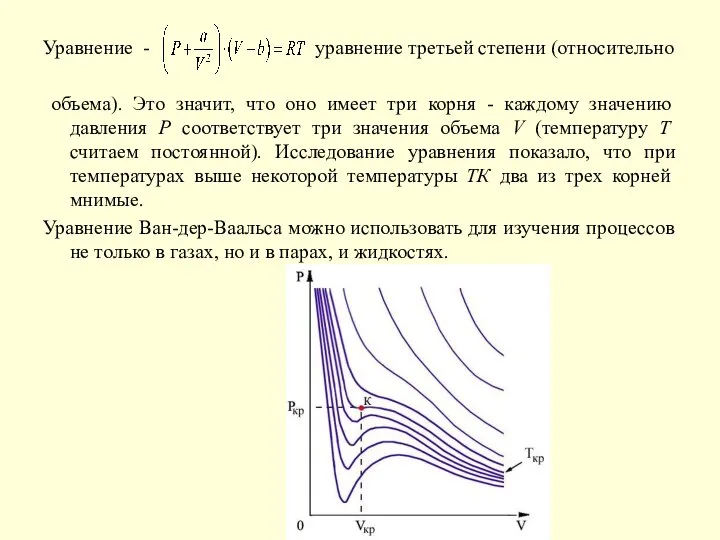
- 6. Уравнение - уравнение третьей степени (относительно объема). Это значит, что оно имеет три корня - каждому
- 7. Точка К называется критической точкой. Соответствующие критической точке значения давления РК и объема VК. называют критическим
- 8. Сравнивая коэффициенты у членов обоих уравнений, содержащих одинаковые степени V, можем написать три следующих соотношения: Используя
- 9. На рисунке показан вид экспериментально полученных изотерм, характерный для многих веществ. На этих кривых виден горизонтальный
- 10. Семейство изотерм для углекислого газа было построено Томасом Эндрюсом (1813 - 1885) во второй половине XIX
- 11. Для нахождения внутренней энергии газа Ван-дер-Ваальса, воспользуемся следующим приемом. Пусть над газом Ван-дер-Ваальса осуществляется адиабатический процесс.
- 12. Как следует из этого выражения, внутренняя энергия газа Ван-дер-Ваальса зависит не только от его температуры, как
- 13. На рисунке схематически изображен опыт Джоуля-Томсона. Внутри теплоизолированной трубки помешалась пористая перегородка, через которую осуществлялось медленное
- 14. 2.Экспериментальные изотермы реального газа. Фазовый переход газ-жидкость. При температурах ниже критической между изотермой Ван-дер-Ваальса и изотермой,
- 15. При некоторых условиях удается опытным путем получить состояния, соответствующие участкам сd и аf изотермы Ван-дер-Ваальса. Например,
- 16. Из рисунка видно, что с повышением температуры горизонтальный участок изотермы сокращается, стягиваясь в точку при критической
- 17. В критической точке переход вещества из газообразного состояния в жидкое происходит непрерывно. Выше критической температуры вещество
- 18. Испарение - непрерывный процесс вылета молекул с поверхности жидкости, обусловленный их тепловым движением. Для вылета с
- 19. Естественно, что при обратном процессе перехода из пара в жидкость (конденсация) теплота, затраченная на испарение, отдается
- 21. Скачать презентацию
1. Газ Ван-дер-Ваальса
Уравнение Клапейрона-Менделеева достаточно хорошо описывает газ при высоких температурах
1. Газ Ван-дер-Ваальса
Уравнение Клапейрона-Менделеева достаточно хорошо описывает газ при высоких температурах
Для описания свойств реального газа необходимо учитывать собственный объем молекул и силы притяжения между молекулами.
Учет конечных размеров молекул приводит к тому, что объем, доступный для
Учет конечных размеров молекул приводит к тому, что объем, доступный для
PV = RТ
вместо объема V надо написать объем , т. е.
P=RТ.
Это означает, что давление реального газа
P=
занимающего объем V при температуре Т, несколько больше давления идеального газа при тех же условиях.
Величину поправки b на собственный объем молекул можно вычислить. Обозначим через Vо объем одной молекулы. Если число молекул в газе N, то суммарный объем всех молекул равен (NVо).
Значит мы можем вести в уравнение состояния поправку b, учитывающую собственный объем молекул.
Теперь учтем силы взаимного притяжения молекул.
Давления, обусловленного силами молекулярного притяжения, давление
Теперь учтем силы взаимного притяжения молекул.
Давления, обусловленного силами молекулярного притяжения, давление
Можно лишь считать, что сила, действующая на молекулу, пропорциональна концентрации n молекул. Так как число молекул, расположенных у стенки сосуда, также пропорционально концентрации, то уменьшение давления можно считать пропорциональным n2. Учитывая, что n =N/V, ΔP ~ 1/V2,
т. е. обратно пропорционально квадрату объема газа. Если ввести некоторый коэффициент a, то поправку на давление можно записать в виде:
Имеем:
или
Это и есть уравнение Ван-дер-Ваальса.
Величины а и b в этом уравнении для каждого газа могут
Величины а и b в этом уравнении для каждого газа могут
По известным значениям параметров в двух состояниях можно вычислить коэффициенты a и b. Экспериментальная проверка уравнения Ван-дер-Ваальса показывает, что оно значительно лучше описывает свойства газов, чем уравнение Клапейрона - Менделеева.
Уравнение - уравнение третьей степени (относительно
объема). Это значит, что оно
Уравнение - уравнение третьей степени (относительно
объема). Это значит, что оно
Уравнение Ван-дер-Ваальса можно использовать для изучения процессов не только в газах, но и в парах, и жидкостях.
Точка К называется критической точкой. Соответствующие критической точке значения давления РК
Точка К называется критической точкой. Соответствующие критической точке значения давления РК
Критические значения давления, объема и температуры можно однозначно связать с постоянными a и b, входящими в уравнение Ван-дер-Ваальса. Для этого воспользуемся тем, что при критической температуре все три корня уравнения Ван-дер-Ваальса одинаковы и равны критическому объему. Поэтому уравнение Ван-дер-Ваальса, записанное в виде уравнения третьей степени
,
должно быть тождественно уравнению
Сравнивая коэффициенты у членов обоих уравнений, содержащих одинаковые степени V, можем
Сравнивая коэффициенты у членов обоих уравнений, содержащих одинаковые степени V, можем
Используя эти соотношения, нетрудно найти зависимость между критическими параметрами вещества и соответствующими значениями постоянных в уравнении Ван-дер-Ваальса:
На рисунке показан вид экспериментально полученных изотерм, характерный для многих веществ.
На
На рисунке показан вид экспериментально полученных изотерм, характерный для многих веществ.
На
Семейство изотерм для углекислого газа было построено Томасом Эндрюсом (1813 -
Семейство изотерм для углекислого газа было построено Томасом Эндрюсом (1813 -
В первой половине XIX века предполагали существование абсолютных газов, которые не могут быть сжижены ни при каких условиях. Однако опыт показал, что любое вещество может быть сжижено при достаточно высоком давлении и низкой температуре.
Совокупность участков изотерм реального газа, соответствующих двухфазным системам жидкость-газ, образуют колоколообразную фигуру, вершиной которой является критическая точка. При температурах выше критической вещество может существовать только в газообразном состоянии. При температуре ниже критической, вещество может быть сжижено. Критическая температура для гелия очень низкая - 5,2 К. Поэтому долгое время его считали абсолютным газом.
В отличие от гелия, водорода, кислорода и азота, чьи критические температуры достаточно низкие, такие вещества как вода и ртуть (критические температуры 647 К и 1820 К соответственно) существуют как в жидком, так и в газообразном состояниях при комнатных температурах. Поэтому возникли такие термины как «водяной пар» и «пары ртути». Сегодня, с исчезновением понятия «абсолютный газ» исчезло различие понятий «газ» и «пар».
Для нахождения внутренней энергии газа Ван-дер-Ваальса, воспользуемся следующим приемом. Пусть над
Для нахождения внутренней энергии газа Ван-дер-Ваальса, воспользуемся следующим приемом. Пусть над
Отсюда следует:
Интегрирование этого выражения дает
Здесь произвольную константу интегрирования необходимо положить равной нулю, так как при a = 0 выражения для внутренних энергий газа Ван-дер-Ваальса и идеального газа должна совпадать: U = U'.
Использование выражения для внутренней энергии идеального газа позволяет записать формулу, для расчета внутренней энергии газа Ван-дер-Ваальса в виде
Как следует из этого выражения, внутренняя энергия газа Ван-дер-Ваальса зависит не
Как следует из этого выражения, внутренняя энергия газа Ван-дер-Ваальса зависит не
В экспериментах, проведенных Джоулем и Томсоном на реальных газах, было установлено, что при адиабатическом расширении их температура изменяется, причем может, как повышаться, так и понижаться. Это явление получило название эффекта Джоуля-Томсона.
Практическое применение эффекта Джоуля-Томсона связано в первую очередь с охлаждением газов и ожижением их. В конце XIX века Карлом Линде (1842 - 1934) была разработана машина для ожижения воздуха, в которой охлажденный вследствие эффекта Джоуля-Томсона воздух осуществляет предварительное охлаждение следующей порции воздуха, которая затем в свою очередь расширяется с уменьшением температуры. Повторяя процесс многократно, можно получить температуру воздуха ниже критической, и ожижить его. Используя эту схему, нидерландский физик Г. Камерлинг-Оннес (1853 - 1926) в 1908 году получил жидкий гелий, что стало началом новой области физики - физики низких температур.
На рисунке схематически изображен опыт Джоуля-Томсона. Внутри теплоизолированной трубки помешалась пористая
На рисунке схематически изображен опыт Джоуля-Томсона. Внутри теплоизолированной трубки помешалась пористая
2.Экспериментальные изотермы реального газа. Фазовый переход газ-жидкость.
При температурах ниже критической между
2.Экспериментальные изотермы реального газа. Фазовый переход газ-жидкость.
При температурах ниже критической между
Опыты показывают, что при сжатии газа до объема V3, соответствующего точке с, газ начинает конденсироваться в жидкость. При дальнейшем сжатии его давление перестает изменяться и по мере уменьшения объема все большая часть газа переходит в жидкое состояние. При сжатии газа до объема V1 процесс конденсации газа заканчивается, и все вещество оказывается в жидком состоянии. Таким образом, горизонтальный участок ac экспериментальной изотермы соответствует расслоению вещества на две фазы: жидкую и газообразную. Газ (или пар), находящийся в равновесии со своей жидкостью, принято называть насыщенным, а давление Р при данной температуре, при котором пар является насыщенным, называют давлением, или упругостью насыщенного пара. Давление, соответствующее горизонтальному участку экспериментальной изотермы, и будет являться давлением насыщенного пара.
При некоторых условиях удается опытным путем получить состояния, соответствующие участкам сd
При некоторых условиях удается опытным путем получить состояния, соответствующие участкам сd
Подобным же образом при изотермическом увеличении объема сжатой жидкости, можно наблюдать задержку в образовании паровой фазы, несмотря на то, что объем, занимаемый жидкостью, превышает ее молекулярный объем, а давление ниже, чем давление насыщенного пара жидкости при данной температуре. Оно соответствует участку af изотермы Ван-дер-Ваальса и называется состоянием перегретой жидкости в том смысле, что при данных объеме и температуре часть жидкости должна была бы находиться в парообразном состоянии, в то время как на опыте паровая фаза отсутствует.
Состояния, соответствующие участку fbd изотермы Ван-дер-Ваальса, являются совершенно неустойчивыми и не могут быть осуществлены.
Из рисунка видно, что с повышением температуры горизонтальный участок изотермы сокращается,
Из рисунка видно, что с повышением температуры горизонтальный участок изотермы сокращается,
На рисунке показана зависимость плотности жидкости и насыщенного пара от температуры.
В критической точке переход вещества из газообразного состояния в жидкое происходит
В критической точке переход вещества из газообразного состояния в жидкое происходит
Если соединить между собой крайние точки горизонтальных участков экспериментальных изотерм, то получим колоколообразную кривую, ограничивающую область двухфазного состояния вещества. Эта кривая и участок изотермы, лежащий слева от критической точки К, делят всю площадь диаграммы (P-V) на три области, соответствующие различным состояниям вещества: жидкому состоянию вещества, двухфазного состояния вещества, газообразное или парообразное состоянию вещества.
Переход вещества из одного фазового состояния в другое называют фазовым. В частности, фазовый переход жидкости в газообразное состояние называют испарением, а обратный переход из газообразного состояния в жидкое – конденсацией.
Испарение - непрерывный процесс вылета молекул с поверхности жидкости, обусловленный их
Испарение - непрерывный процесс вылета молекул с поверхности жидкости, обусловленный их
Очевидно, что она может быть совершена только за счет кинетической энергии теплового движения молекул жидкости. В жидкостях, как и в газах, средняя скорость теплового движения молекул при данной температуре постоянна. Однако всегда отдельные молекулы имеют скорости и большие, и меньшие, чем средняя скорость. Только наиболее быстрые молекулы жидкости обладают кинетической энергией, позволяющей совершить работу, связанную с переходом их в пар. Поэтому при испарении жидкость покидают наиболее быстрые молекулы и вследствие этого средняя энергия молекул, остающихся в жидкости, убывает, т. е. жидкость охлаждается. Чтобы при испарении температура жидкости не понижалась, жидкость необходимо непрерывно нагревать, Количество теплоты, которое нужно сообщить единице массы жидкости, имеющей температуру Т, чтобы превратить ее в пар при той же температуре, называют удельной теплотой испарения.
Естественно, что при обратном процессе перехода из пара в жидкость (конденсация)
Естественно, что при обратном процессе перехода из пара в жидкость (конденсация)
Если, например, в сосуде увеличить объем, заполненный паром, то испарение будет происходить более интенсивно до тех пор, пока вновь не наступит состояние динамического равновесия, а плотность и давление пара не примут прежних значений, т. е. до тех пор, пока вновь пар не станет насыщенным. При уменьшёнии же объема, предоставленного пару, более интенсивно будет происходить процесс конденсации, пока вновь не установится состояние динамического равновесия, соответствующее данной температуре. Поэтому в отличие от газов давление насыщенного пара нельзя изменить, сжимая его или же давая ему возможность расширяться. Давление насыщенного пара при данной температуре всегда одинаково и не зависит от занимаемого им объема.

















 Узгоджння фідерної лінії з навантаженням
Узгоджння фідерної лінії з навантаженням Аттестационная работа. Учебная деятельность учащихся среднего звена на уроках физики через использование метода проектирования
Аттестационная работа. Учебная деятельность учащихся среднего звена на уроках физики через использование метода проектирования Проблема близорукости у школьников среднего звена. Работа: Новиковой Юлии Научный руководитель: Манохина Татьяна Александровна
Проблема близорукости у школьников среднего звена. Работа: Новиковой Юлии Научный руководитель: Манохина Татьяна Александровна Лаборатории
Лаборатории Электрический ток в различных средах
Электрический ток в различных средах Физикалық және химиялық құбылыстар
Физикалық және химиялық құбылыстар Динамика материальной точки и поступательного движения твердого тела
Динамика материальной точки и поступательного движения твердого тела Классификация СВЧ элементной базы. (Тема 1)
Классификация СВЧ элементной базы. (Тема 1) Уравнение состояния идеального газа
Уравнение состояния идеального газа Несовершенства и дефекты кристаллической решетки
Несовершенства и дефекты кристаллической решетки Особенности метода Монте-Карло. Физическая постановка задачи. Генератор случайных чисел
Особенности метода Монте-Карло. Физическая постановка задачи. Генератор случайных чисел Тест по физике
Тест по физике Оборудование для зарядки ВВ ANOL CC
Оборудование для зарядки ВВ ANOL CC Причины отказов насосов
Причины отказов насосов «Действие магнитного поля на движущуюся заряженную частицу. Сила Лоренца» Урок физики в 11 классе Разработан учителем физики выс
«Действие магнитного поля на движущуюся заряженную частицу. Сила Лоренца» Урок физики в 11 классе Разработан учителем физики выс Микромир, макромир, мегамир, их пространственно - временные характеристики
Микромир, макромир, мегамир, их пространственно - временные характеристики Решение задач по теме Прямолинейное равноускоренное движение
Решение задач по теме Прямолинейное равноускоренное движение Алгоритм решения качественных задач на газовые законы. Работа выполнена Лукьянец Надеждой Николаевной учителем физики MАOУ «Cpeдня
Алгоритм решения качественных задач на газовые законы. Работа выполнена Лукьянец Надеждой Николаевной учителем физики MАOУ «Cpeдня Ионолет
Ионолет Нанофотоника
Нанофотоника Идеальный физический маятник
Идеальный физический маятник Физика и технология наноструктур
Физика и технология наноструктур Mechacnics. Molecular physics and Thermodynamics. Electricity. Magnetism
Mechacnics. Molecular physics and Thermodynamics. Electricity. Magnetism Лазеры
Лазеры Презентация по физике "Электрический ток в жидкостях" - скачать бесплатно
Презентация по физике "Электрический ток в жидкостях" - скачать бесплатно Устройство микроскопа
Устройство микроскопа Закон Джоуля-Ленца. Плотность тока. Скорость движения электронов в проводнике
Закон Джоуля-Ленца. Плотность тока. Скорость движения электронов в проводнике Разработка организации технического обслуживания и ремонта МТП в хозяйстве
Разработка организации технического обслуживания и ремонта МТП в хозяйстве