Содержание
- 2. Конкретные представления о строении атома развивались по мере накопления физикой фактов о свойствах вещества. Открыли электрон,
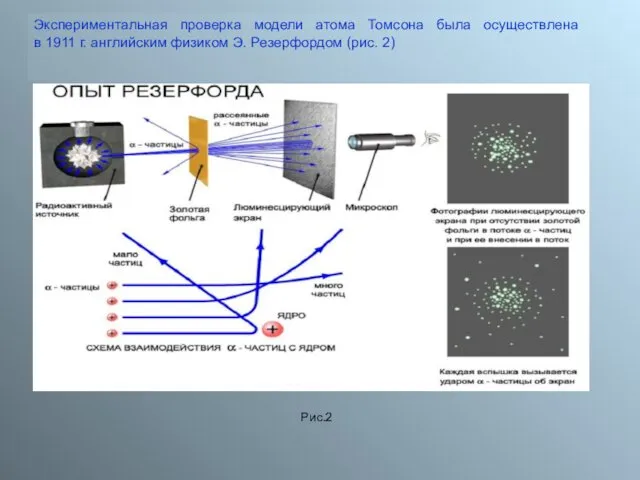
- 3. Экспериментальная проверка модели атома Томсона была осуществлена в 1911 г. английским физиком Э. Резерфордом (рис. 2)
- 4. Пропуская пучок Альфа- частиц через тонкую золотую фольгу, Э. Резерфорд обнаружил, что какая-то часть частиц отклоняется
- 5. Открытие нейтрона Идея о существовании тяжелой нейтральной частицы казалась Резерфорду настолько привлекательной, что он незамедлительно предложил
- 6. Нейтрон – это элементарная частица. Это не протон -электронная пара, как первоначально предполагал Резерфорд. По современным
- 7. Ядро атома состоит из нуклонов, которые подразделяются на протоны и нейтроны. Символическое обозначение ядра атома А
- 8. Для того, чтобы атомные ядра были устойчивыми, протоны и нейтроны должны удерживаться внутри ядер огромными силами,
- 9. ЗНАЕШЬ ЛИ ТЫ ? В середине XX века теория ядра предсказала существование стабильных элементов с порядковыми
- 10. Атомы с одинаковыми атомными номерами называют изотопами: в таблице Менделеева они расположены в одной клеточке (по-гречески
- 12. Скачать презентацию
Конкретные представления о строении атома развивались по мере накопления физикой
Конкретные представления о строении атома развивались по мере накопления физикой
электроны входят в состав атома.
Опираясь на эти открытия, Дж. Томсон в 1898 г. Предложил модель атома в виде положительно заряженного шара радиусом 10(-10) м, в котором плавают электроны, нейтрализующие положительный заряд (рис. 1)
Рис. 1
Экспериментальная проверка модели атома Томсона была осуществлена
в 1911 г. английским
Экспериментальная проверка модели атома Томсона была осуществлена в 1911 г. английским
Рис.2
Пропуская пучок Альфа- частиц через тонкую золотую фольгу, Э. Резерфорд обнаружил,
Пропуская пучок Альфа- частиц через тонкую золотую фольгу, Э. Резерфорд обнаружил,
Резерфорд показал, что модель Томсона находится в противоречии с его опытами. Обобщая результаты своих опытов.
Резерфорд предложил ядерную ( планетарную) модель строения атома (рис.4)
Атом имеет ядро, размеры которого малы по сравнению с размерами самого атома (рис. 5)
В ядре сконцентрирована почти вся масса атома.
Отрицательный заряд всех электронов распределен по всему объему атома.
Рис.3
Рис. 5
Рис.4
Открытие нейтрона
Идея о существовании тяжелой нейтральной частицы казалась Резерфорду настолько
Открытие нейтрона
Идея о существовании тяжелой нейтральной частицы казалась Резерфорду настолько
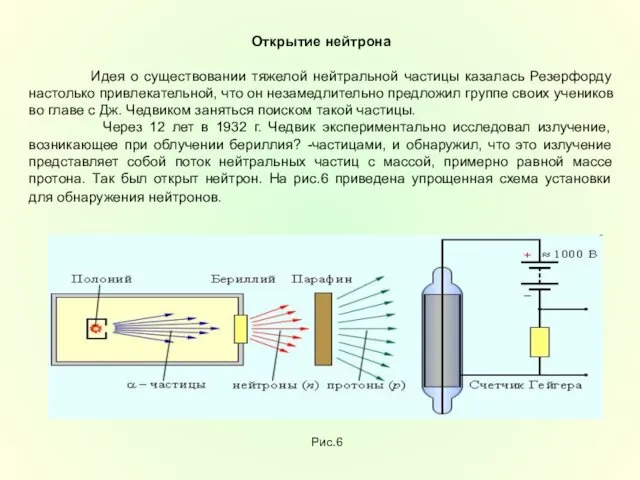
Через 12 лет в 1932 г. Чедвик экспериментально исследовал излучение, возникающее при облучении бериллия? -частицами, и обнаружил, что это излучение представляет собой поток нейтральных частиц с массой, примерно равной массе протона. Так был открыт нейтрон. На рис.6 приведена упрощенная схема установки для обнаружения нейтронов.
Рис.6
Нейтрон – это элементарная частица.
Это не протон -электронная пара, как
Нейтрон – это элементарная частица.
Это не протон -электронная пара, как
По современным измерениям, масса нейтрона mn = 1,67493·10–27 кг = 1,008665 а.е.м.
В энергетических единицах масса нейтрона равна 939,56563 МэВ.
Масса нейтрона приблизительно на две электронные массы превосходит массу протона.
Протон-нейтронная модель ядра
Сразу же после открытия нейтрона российский ученый Д. Д. Иваненко и немецкий физик В. Гейзенберг выдвинули гипотезу о протонно-нейтронном строении атомных ядер, которая полностью подтвердилась последующими исследованиями (рис. 7)
По современным измерениям, положительный заряд протона в точности равен элементарному заряду e = 1,60217733·10–19 Кл,
то есть равен по модулю отрицательному заряду электрона. В настоящее время равенство зарядов протона и электрона проверено с точностью 10–22. Такое совпадение зарядов двух непохожих друг на друга частиц вызывает удивление и остается одной из фундаментальных загадок современной физики.
Масса протона, по современным измерениям, равна mp = 1,67262·10-27 кг.
Протоны и нейтроны в ядре
принято называть нуклонами.
Рис. 7
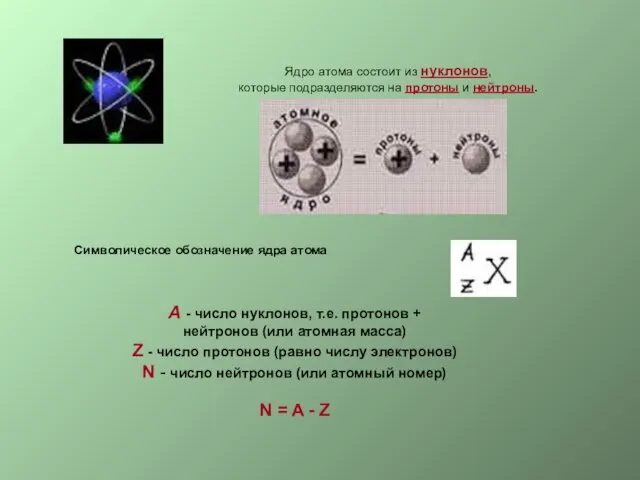
Ядро атома состоит из нуклонов,
которые подразделяются на протоны и нейтроны.
Ядро атома состоит из нуклонов,
которые подразделяются на протоны и нейтроны.
Символическое обозначение ядра атома
А - число нуклонов, т.е. протонов + нейтронов (или атомная масса)
Z - число протонов (равно числу электронов)
N - число нейтронов (или атомный номер)
N = A - Z
Для того, чтобы атомные ядра были устойчивыми, протоны и нейтроны должны
Для того, чтобы атомные ядра были устойчивыми, протоны и нейтроны должны
Особенности ядерных сил:
Ядерные силы примерно в 100 раз превосходят электростатические силы и на десятки порядков превосходят силы гравитационного взаимодействия нуклонов.
2. Важной особенностью ядерных сил является их короткодействующий характер. Ядерные силы заметно проявляются, как показали опыты Резерфорда по рассеянию
a-частиц, лишь на расстояниях порядка размеров ядра (10–14–10–15 м). Ядерные силы очень быстро спадают с расстоянием. Радиус их действия порядка 0,000 000 000 000 001 метра.
Для этой сверхмалой длины, характеризующей размеры атомных ядер, ввели специальное обозначение Фм (в честь итальянского физика Э. Ферми, 1901-1954)
Все ядра имеют размеры нескольких Ферми.
Радиус ядерных сил равен размеру нуклона, поэтому ядра – концентрация и очень плотной материи. Возможно, самой плотной в земных условиях.
Ядерные силы - сильные взаимодействия.
На больших расстояниях проявляется действие сравнительно медленно убывающих кулоновских сил.
На основании опытных данных можно заключить, что протоны и нейтроны в ядре ведут себя одинаково в отношении сильного взаимодействия, т. е. ядерные силы не зависят от наличия или отсутствия у частиц электрического заряда.
ЯДЕРНЫЕ СИЛЫ
силы притяжения;
действуют между всеми нуклонами в ядре;
короткодействующие.
.
Рис.8
ЗНАЕШЬ ЛИ ТЫ ?
В середине XX века теория ядра предсказала существование
ЗНАЕШЬ ЛИ ТЫ ? В середине XX века теория ядра предсказала существование
Атомы с одинаковыми атомными номерами называют изотопами: в таблице Менделеева
они
Атомы с одинаковыми атомными номерами называют изотопами: в таблице Менделеева они
Рис. 9






 Сопротивление материалов. Курс лекций
Сопротивление материалов. Курс лекций Решение задач. Магнитное поле и проводник с током
Решение задач. Магнитное поле и проводник с током Электрический стартер
Электрический стартер Аттестационная работа. Внеурочная работа по физике в 6 классе
Аттестационная работа. Внеурочная работа по физике в 6 классе Давление твердых тел
Давление твердых тел  Метод молекулярной динамики
Метод молекулярной динамики Развитие учения о свете до создания квантовой теории света (история физики)
Развитие учения о свете до создания квантовой теории света (история физики) Исследование скважин. Метод высокочастотного индукционноого каротажного изопараметрического зондирования
Исследование скважин. Метод высокочастотного индукционноого каротажного изопараметрического зондирования Механические характеристики металлов
Механические характеристики металлов Физические основы прочности
Физические основы прочности Преломление света
Преломление света Интегрированный урок: биологическое действие радиации
Интегрированный урок: биологическое действие радиации Зрительное восприятие трехмерного пространства человеком. Системы формирования объемного изображения
Зрительное восприятие трехмерного пространства человеком. Системы формирования объемного изображения Теоретическая механика. Статика
Теоретическая механика. Статика Бесконтактные методы контроля температуры
Бесконтактные методы контроля температуры Оптика. Электромагнитные волны, частоты
Оптика. Электромагнитные волны, частоты Механические свойства материалов
Механические свойства материалов Урок технологии 5 класс раздел: Элементы машиноведения
Урок технологии 5 класс раздел: Элементы машиноведения Закон Ома для участка цепи
Закон Ома для участка цепи Радиоактивность как свидетельство сложного строения атомов
Радиоактивность как свидетельство сложного строения атомов Взаимодействие молекул
Взаимодействие молекул Презентация по физике "Реактивное движение" - скачать бесплатно_
Презентация по физике "Реактивное движение" - скачать бесплатно_ Презентация по физике Применение фотоэффекта
Презентация по физике Применение фотоэффекта  Лекція №5. Закон збереження імпульсу
Лекція №5. Закон збереження імпульсу Измерение температуры
Измерение температуры Электродвижущая сила. Закон Ома для полной цепи Физика, 10 класс
Электродвижущая сила. Закон Ома для полной цепи Физика, 10 класс Электромагниттік толқындардың адам ағзасына тигізер әсері
Электромагниттік толқындардың адам ағзасына тигізер әсері Электронные лекции по разделам классической и релятивистской механики
Электронные лекции по разделам классической и релятивистской механики