Содержание
- 2. Л е в к и п п (5 век до н. э.) - древнегреческийфилософ-материалист, один из
- 4. Ввёл понятие «веса атомов», изложил атомистическую теорию мироздания и идея корпускулярной модели атома. К о р
- 6. 1. Атомизм Демокрита - Левкипа (460-370 гг. до н.э.)
- 7. Основные положения атомистики Демокрита - малы (невидимы), но имеют конечные размеры; - в вечном вихревом движении;
- 8. - видимые тела различаются количеством, видами и порядком сцепления атомов; - в бесконечной вселенной множество миров;
- 9. Закон сохранения массы соединений Антуан де Лавуазье (1743-1794) 2.Открытие атомов в химии (Обезглавлен: "Республика не нуждается
- 10. Интерпретация Дальтона: имеются определенные минимальные количества элементов и веществ - соединений
- 11. Ломоносов полагал, что всем свойствам вещества можно дать объяснение с помощью представления о механических движениях корпускул,
- 12. Менделеев Дмитрий Иванович (1834-1907) Русский учёный и общественный деятель. Химик, физик, метролог, экономист, технолог, геолог, метеоролог,
- 13. Окончательный удар по механистической картине мира был нанесен в к.XIX – н.XX вв. Эти открытия подрывали
- 14. 3. Проблема внутреннего строения атома Открытие электрона Исследование тока в разреженных газах
- 15. Трубка Крукса
- 16. Гипотеза: катодные лучи - это "лучистая материя", "4 состояние"
- 17. 1 - отклоняются в магнитном поле 2 - имеют отрицательный заряд
- 18. К-лучи - это поток отрицательно заряженных частиц вещества ВЫВОДЫ:
- 20. J. J. Thomson (1856-1940)
- 21. Дж.Дж.Томсон в 1897 году определил величину отношения "заряд"/"масса" для частиц К-лучей
- 22. и рассчитал массу электрона:
- 23. В состав всех атомов входят частицы малой массы - э л е к т р о
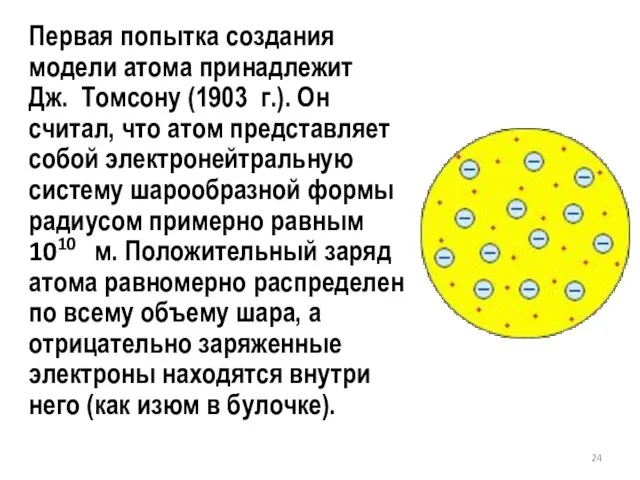
- 24. Первая попытка создания модели атома принадлежит Дж. Томсону (1903 г.). Он считал, что атом представляет собой
- 25. Модель атома Томсона Джозеф Джон Томсон (1856-1940) Эта модель атома получила среди ученых прозвище "сливовый пудинг",
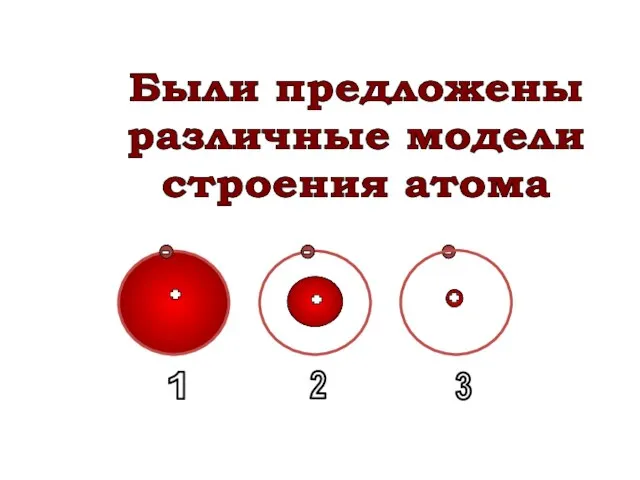
- 26. Были предложены различные модели строения атома
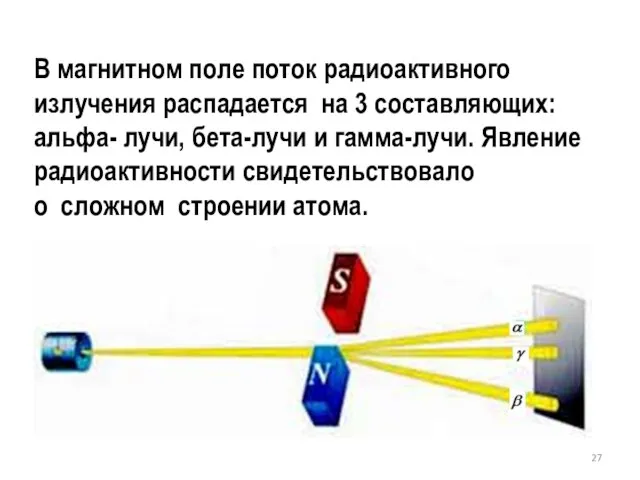
- 27. В магнитном поле поток радиоактивного излучения распадается на 3 составляющих: альфа- лучи, бета-лучи и гамма-лучи. Явление
- 28. Первые прямые эксперименты по исследованию внутренней структуры атомов были выполнены Э. Резерфордом и его сотрудниками Э.
- 29. Эрне́ст Ре́зерфорд (Ernest Rutherford; 1871 - 1937, ) — британский физик новозеландского происхождения. Создал планетарную модель
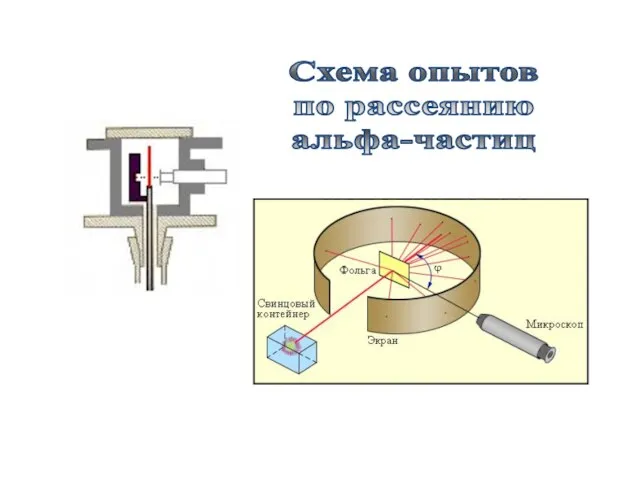
- 30. Rutherford Ernest (1871-1937), Lord of Nelson В 1909 г. в лаборатории Э. Резерфорда начали изучать рассеяние
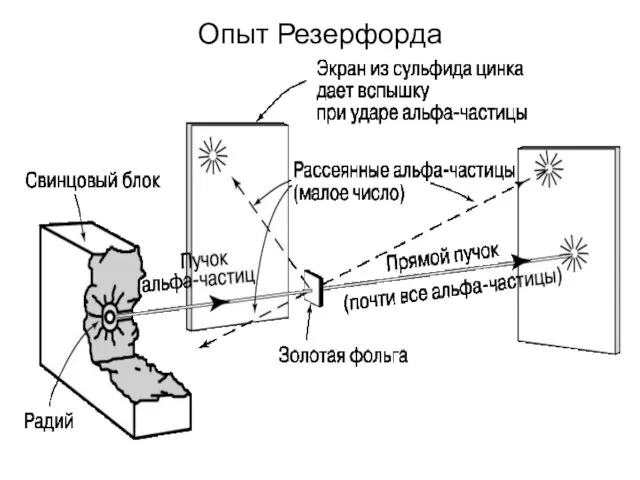
- 31. исполнители: Ханс Гейгер и Эрвин Мардсен Схема опытов по рассеянию альфа-частиц
- 32. Масса α-частиц приблизительно в 7300 раз больше массы электрона, а положительный заряд равен удвоенному элементарному заряду.
- 34. Опыты Резерфорда и его сотрудников привели к выводу, что в центре атома находится плотное положительно заряженное
- 35. Эрнест Резерфорд (1871-1937) — британский физик. Открыл альфа- и бета-излучение, радон и множество изотопов. Открыл радиоактивное
- 36. Опыт Резерфорда
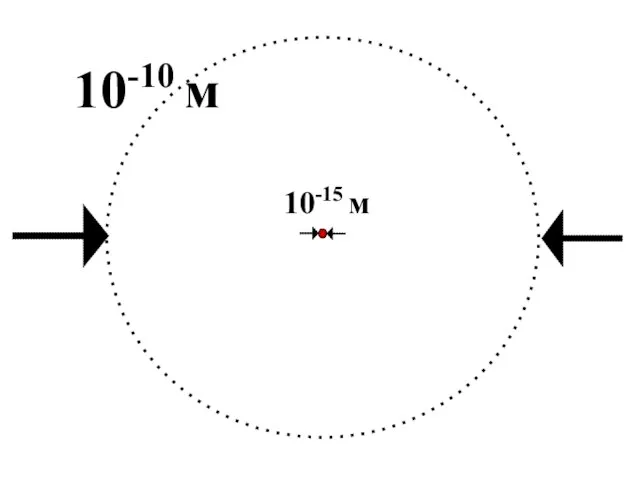
- 37. Малые размеры положительно заряженной области позволяют выбрать планетарную модель строения атомов 1911 г.
- 38. 10-10 м
- 39. планетарная модель атома противоречит электродинамике Максквелла ! ОДНАКО:
- 40. Согласно теории Максвелла, ускоренно движущийся заряд излучает электромагнитные волны
- 41. Атом не будет устойчивой системой? Электрон должен излучать энергию и падать на ядро
- 43. Нильс Хенрик Давид Бор (1885 — 1962) Датский физик, один из создателей современной физики. Создал теорию
- 44. Нильс Хе́нрик Дави́д Бор (Niels Henrik David Bohr 1885 - 1962 , Копенгаген) — датский физик-теоретик
- 45. Следующий шаг в развитии представлений об устройстве атома сделал в 1913 году датский физик Н. Бор.
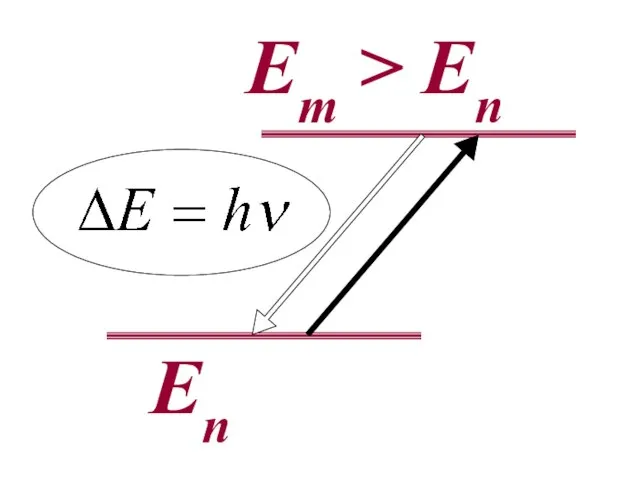
- 46. Второй постулат Бора (правило частот) формулируется следующим образом: при переходе атома из одного стационарного состояния с
- 47. Еn Em > En
- 48. Третий постулат (Правило квантования). Бор предположил, что из всех возможных орбит электрона осуществляются только те для
- 49. m - масса электрона, V - его скорость, r - радиус орбиты, n - целое число
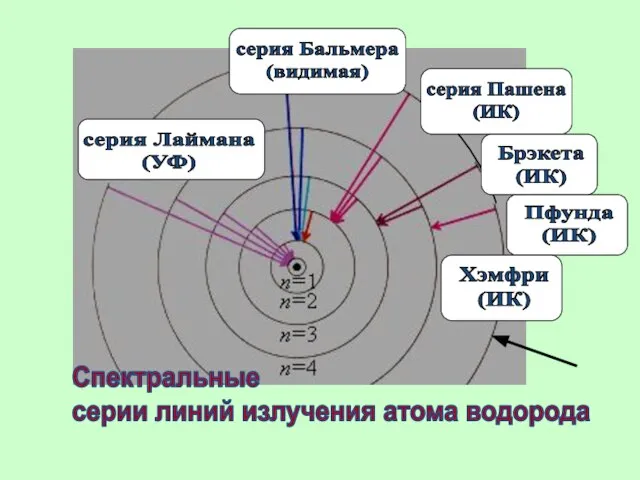
- 51. Еще в начале XIX века были открыты дискретные спектральные линии в излучении атома водорода в видимой
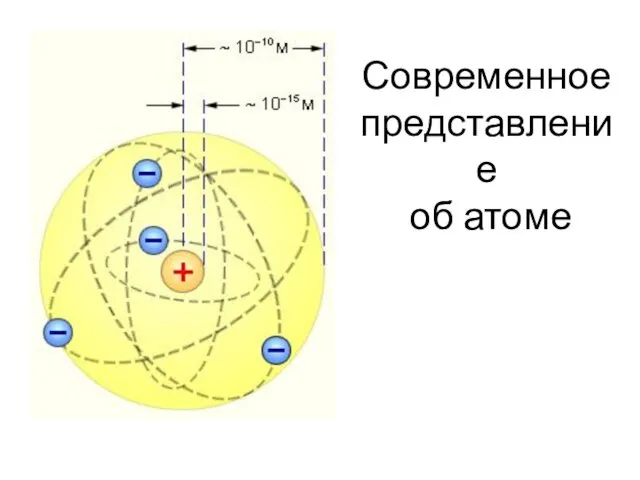
- 52. Современное представление об атоме
- 53. серия Лаймана (УФ) Спектральные серии линий излучения атома водорода
- 54. В 1890 году И. Ридберг получил эмпирическую формулу для частот спектральных линий: Для серии Бальмера m
- 55. Иоганн Якоб Бальмер ( Johann Jakob Balmer, 1825 - 1898) — швейцарский математик и физик. Читал
- 56. Йоханнес Роберт Ридберг (Johannes Robert Rydberg, 1854 - 1919) — шведский физик. С 1901 - профессор
- 58. Постулат Бора Классическая физика
- 59. Решая совместно получим
- 60. Величина энергии основного состояния n = 1
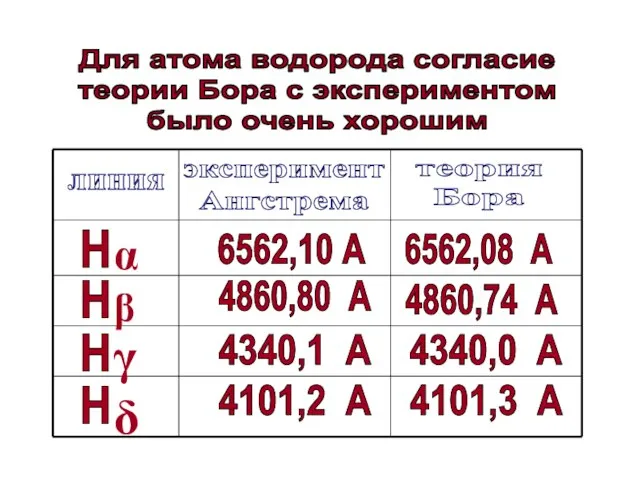
- 61. Для атома водорода согласие теории Бора с экспериментом было очень хорошим эксперимент Ангстрема теория Бора линия
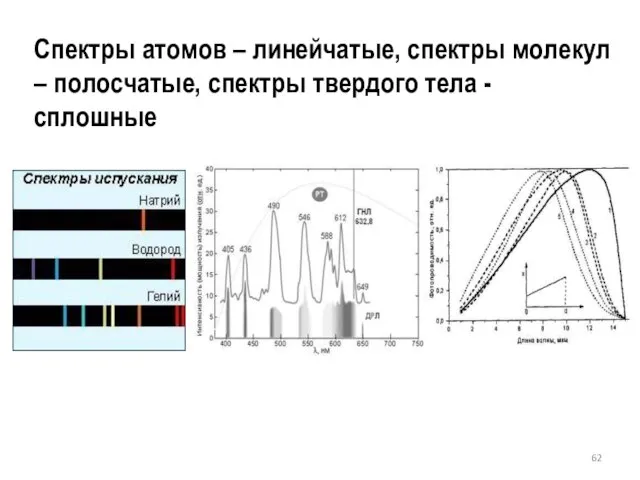
- 62. Спектры атомов – линейчатые, спектры молекул – полосчатые, спектры твердого тела - сплошные
- 63. А вот для других атомов такого согласия не было. Теория Бора была развита в работах А.
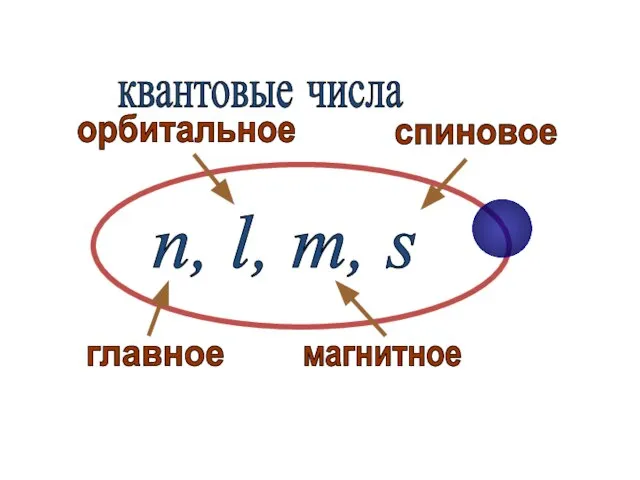
- 64. n, l, m, s главное орбитальное магнитное спиновое квантовые числа
- 65. Дополнение механической планетарной модели Резерфорда квантовыми постулатами Бора , Зоммерфельда, Паули
- 66. приводит к согласию с экспериментальными результатами Ангстрема, Бальмера, Зеемана и других исследователей
- 67. "Портрет" атома радия Н. Бор, 1925 г.
- 68. Величина радиуса орбиты при n = 1 = 53 пм
- 70. Скачать презентацию























































 Архимедова сила
Архимедова сила Цепи с распределенными параметрами
Цепи с распределенными параметрами Архимед күші
Архимед күші Активная зона реактора ВВЭР-1200 (В-392М). Назначение и проектные основы
Активная зона реактора ВВЭР-1200 (В-392М). Назначение и проектные основы Построение изображений, даваемых линзами
Построение изображений, даваемых линзами Калий в организме человека и определение его содержания с помощью гамма-спектрометра
Калий в организме человека и определение его содержания с помощью гамма-спектрометра Ядро и электронная оболочка. Состав атомных ядер
Ядро и электронная оболочка. Состав атомных ядер Основные физические явления и процессы в электрических машинах и аппаратах
Основные физические явления и процессы в электрических машинах и аппаратах Принятые технологии, история и перспективы развития: реакторы с тяжелой водой и с водой под давлением. Лекция 7
Принятые технологии, история и перспективы развития: реакторы с тяжелой водой и с водой под давлением. Лекция 7 Понятия теории электрических цепей
Понятия теории электрических цепей Исследование баланса энергии в ионном ускорителе ТЕМП-4М Магистрант 1-го года обучения Хайлов И. П. Научный руководитель: Пушкарёв
Исследование баланса энергии в ионном ускорителе ТЕМП-4М Магистрант 1-го года обучения Хайлов И. П. Научный руководитель: Пушкарёв Магнитная восприимчивость и биомагнетизм
Магнитная восприимчивость и биомагнетизм Презентация УРОК ФИЗИКИ В 10 КЛАССЕ Сила тяжести. Вес тела. Сила упругости
Презентация УРОК ФИЗИКИ В 10 КЛАССЕ Сила тяжести. Вес тела. Сила упругости Механика. Жесткость и прочность
Механика. Жесткость и прочность Живой свет свечи
Живой свет свечи Оценка температуры по мультиспектральным снимкам
Оценка температуры по мультиспектральным снимкам Волновые уравнения
Волновые уравнения Презентация по физике "Что такое свет Корпускулярно-волновой дуализм" - скачать бесплатно
Презентация по физике "Что такое свет Корпускулярно-волновой дуализм" - скачать бесплатно Электромагнитные излучения небесных тел
Электромагнитные излучения небесных тел Физические величины. Измерение физических величин. Точность и погрешность измерений
Физические величины. Измерение физических величин. Точность и погрешность измерений Моделирование взаимодействия деформируемого ударника с металлической преградой в пакете LS-DYNA
Моделирование взаимодействия деформируемого ударника с металлической преградой в пакете LS-DYNA Механические свойства твердых тел и биологических тканей. Деформация удлинение-сжатие
Механические свойства твердых тел и биологических тканей. Деформация удлинение-сжатие Презентация по физике "Использование атома" - скачать
Презентация по физике "Использование атома" - скачать  Атомная физика
Атомная физика Механические колебания. Характеристики колебательного движения
Механические колебания. Характеристики колебательного движения Аттестационная работа. Рабочая программа дополнительного образования. Кружок по физике: Удивительная физика 6 класс
Аттестационная работа. Рабочая программа дополнительного образования. Кружок по физике: Удивительная физика 6 класс Помехоустойчивость технических средств
Помехоустойчивость технических средств История происхождения физических терминов (работа, масса, сила)
История происхождения физических терминов (работа, масса, сила)