Содержание
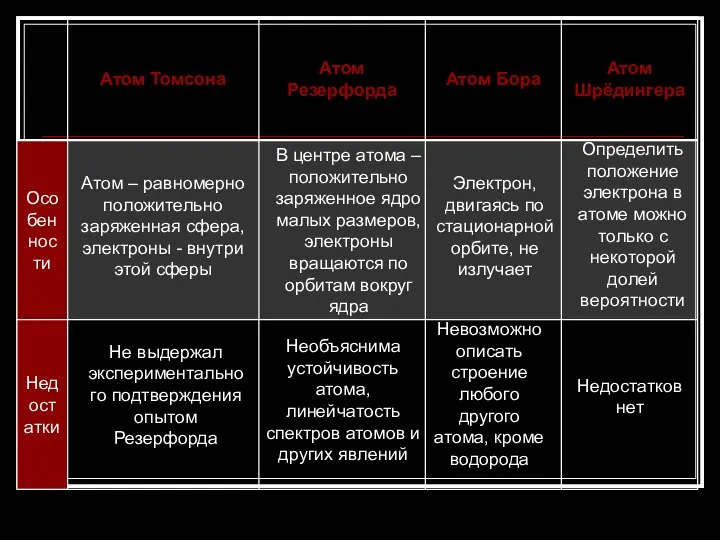
- 2. Модели атома Модель атома Томсона Модель атома Резерфорда Модель атома Бора Модель атома Шрёдингера
- 3. Модель атома Томсона «Пудинг с изюмом» Джозеф Томсон (1856 -1940), английский учёный, в 1897г. открыл электрон,
- 4. Опыт Резерфорда
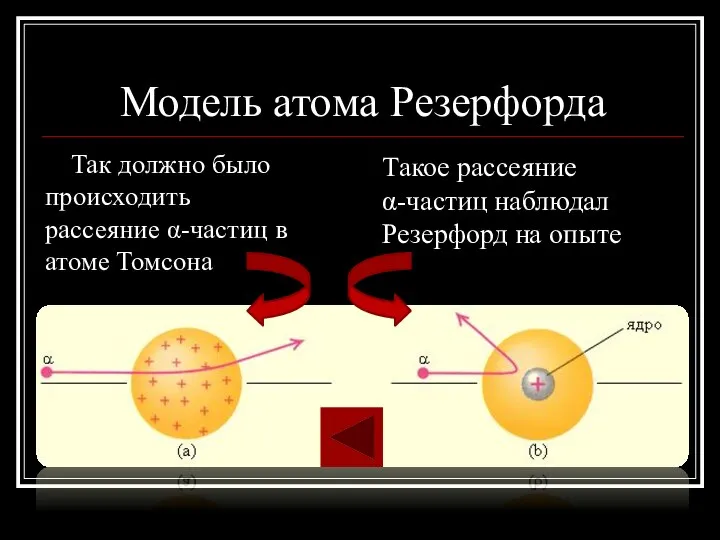
- 5. Модель атома Резерфорда Так должно было происходить рассеяние α-частиц в атоме Томсона Такое рассеяние α-частиц наблюдал
- 6. Трудности модели Резерфорда Согласно модели атома Резерфорда атом должен непрерывно излучать свет всех длин волн. Но
- 7. Модель атома Бора 1 постулат: В устойчивом атоме электрон может двигаться лишь по особым стационарным орбитам,
- 8. Правило квантования орбит На длине окружности каждой стационарной орбиты укладывается целое число n длин волн де
- 9. Правило квантования орбитального момента импульса На стационарной орбите момент импульса электрона квантуется (кратен постоянной Планка)
- 10. Радиусы стационарных орбит Радиусы стационарных орбит квантованы (имеют дискретные значения, пропорциональные квадрату главного квантового числа).
- 11. Энергетический спектр атома Энергия электрона в атоме квантуется
- 12. Излучение и поглощение света атомом Энергия излучённого фотона равна разности энергий стационарных состояний:
- 13. Серии излучения атома водорода Серия Бальмера состоит из видимых спектральных линий фиолетового, синего, зелёного и красного
- 14. Спектры излучения Сплошной (непрерывный) спектр излучают твердые тела, жидкости и сжатые газы.
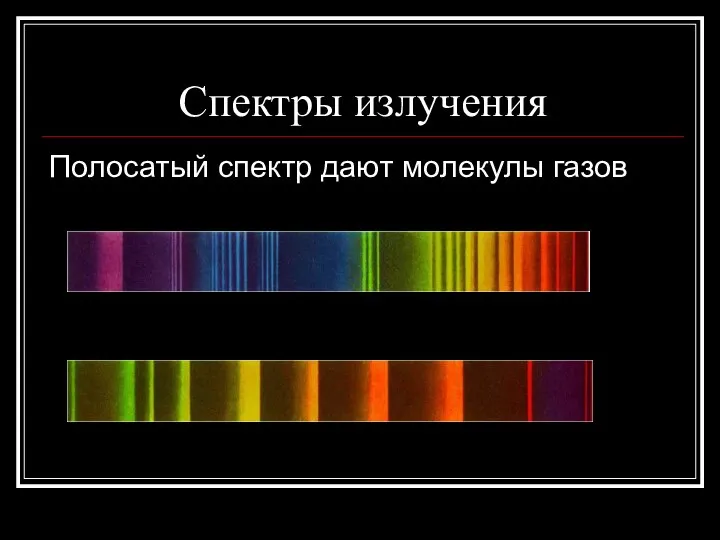
- 15. Спектры излучения Полосатый спектр дают молекулы газов
- 16. Спектры излучения Линейчатый спектр создают разреженные газы в атомарном состоянии
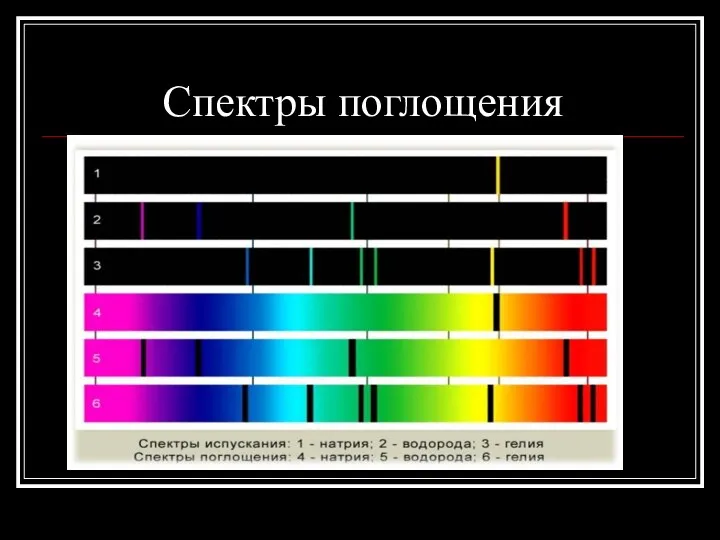
- 17. Спектры поглощения
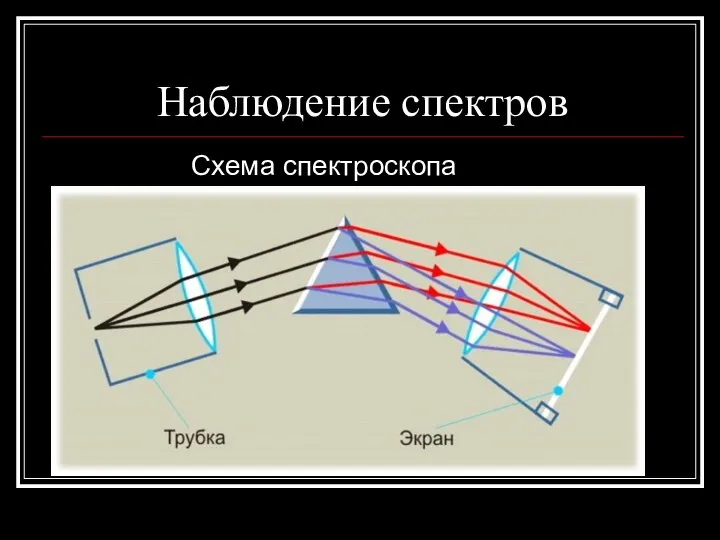
- 18. Наблюдение спектров Схема спектроскопа
- 19. Применение спектрального анализа Определение химического состава сложных веществ В криминалистике Определение химического состава небесных объектов Определение
- 20. Трудности модели атома Бора Теория Бора могла описать только атом водорода и водородоподобные системы. Рассчитать спектр
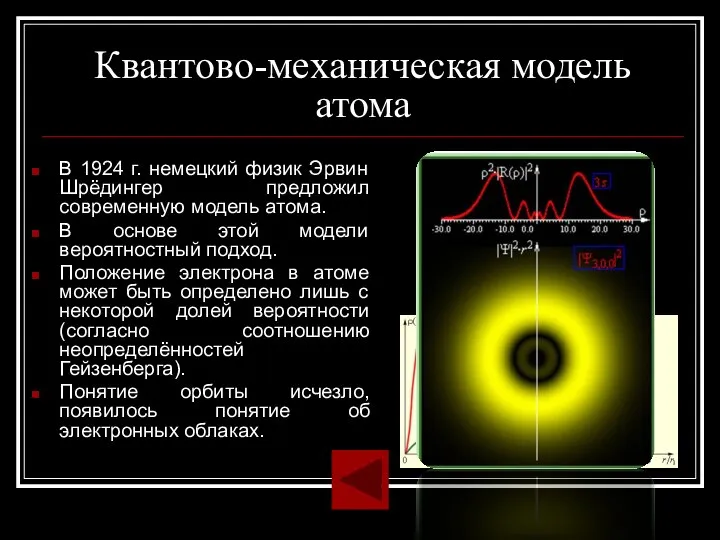
- 21. Квантово-механическая модель атома В 1924 г. немецкий физик Эрвин Шрёдингер предложил современную модель атома. В основе
- 22. Атом – равномерно положительно заряженная сфера, электроны - внутри этой сферы В центре атома – положительно
- 23. Виды излучения Тепловое излучение Люминесценция катодолюминесценция фотолюминесценция хемилюминесценция флуоресценция фосфоресценция
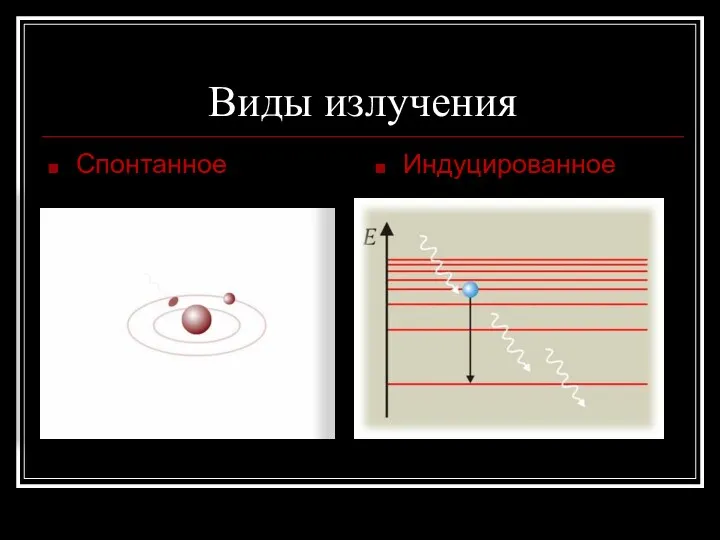
- 24. Виды излучения Спонтанное Индуцированное
- 25. Лазер Свойства лазерного излучения Узкая направленность Высокая монохроматичность Пространственная и временная когерентность Высокая мощность
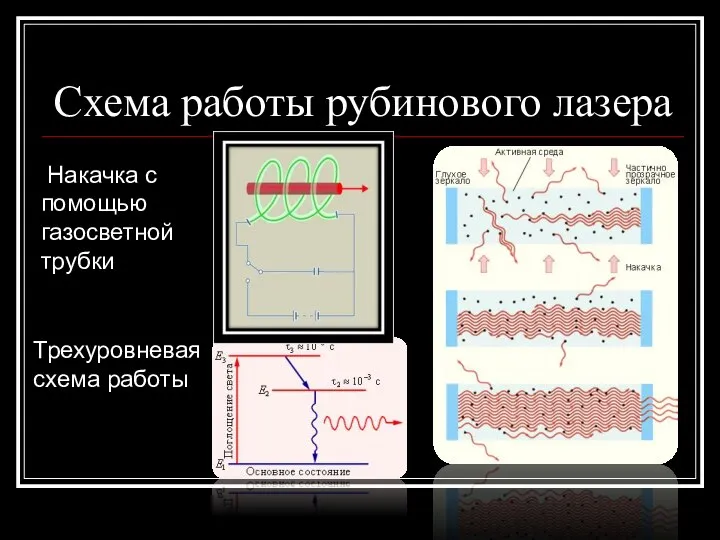
- 26. Схема работы рубинового лазера Накачка с помощью газосветной трубки Трехуровневая схема работы
- 27. Гелий – неоновый лазер 1 – стеклянная кювета со смесью гелия и неона, в которой создается
- 28. Схема работы гелий-неонового лазера Активным газом, на котором возникает генерация на длине волны 632,8 нм (ярко-красный
- 30. Скачать презентацию



















 Підготувала учениця 9-А класу Колпакчі Яна
Підготувала учениця 9-А класу Колпакчі Яна  Явления переноса в газах
Явления переноса в газах Технологические процессы и производства. Преобразование энергии на ТЭС
Технологические процессы и производства. Преобразование энергии на ТЭС Gravity or gravitation
Gravity or gravitation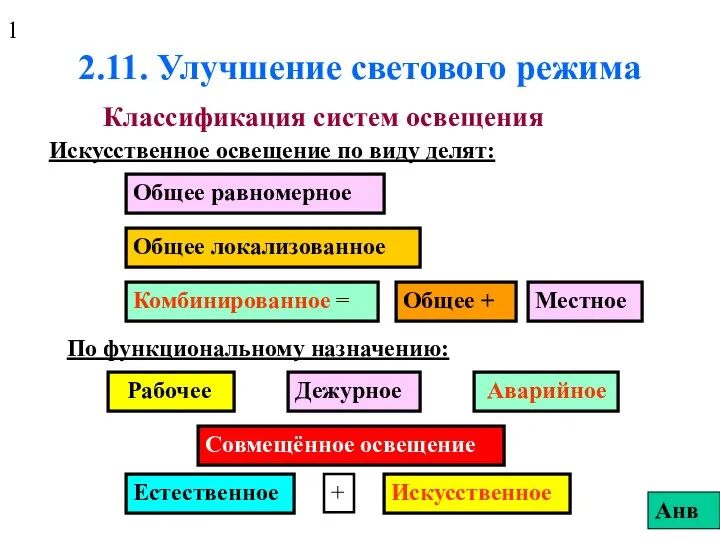 Улучшение светового режима
Улучшение светового режима Графік проведення лабораторних робіт в ІІ семестрі 2015-2016 н.р
Графік проведення лабораторних робіт в ІІ семестрі 2015-2016 н.р Физические явления Работа выполнена Учителем СШ № 121 Шумилиной А.Н.
Физические явления Работа выполнена Учителем СШ № 121 Шумилиной А.Н.  Өлшеу түрлері. Физикалық шамалардың бірліктерін көрсету мен оларға өлшем беру негіздері
Өлшеу түрлері. Физикалық шамалардың бірліктерін көрсету мен оларға өлшем беру негіздері Презентация по физике "как научится решать задачи" - скачать бесплатно
Презентация по физике "как научится решать задачи" - скачать бесплатно Физические свойства воды в разных агрегатных состояниях
Физические свойства воды в разных агрегатных состояниях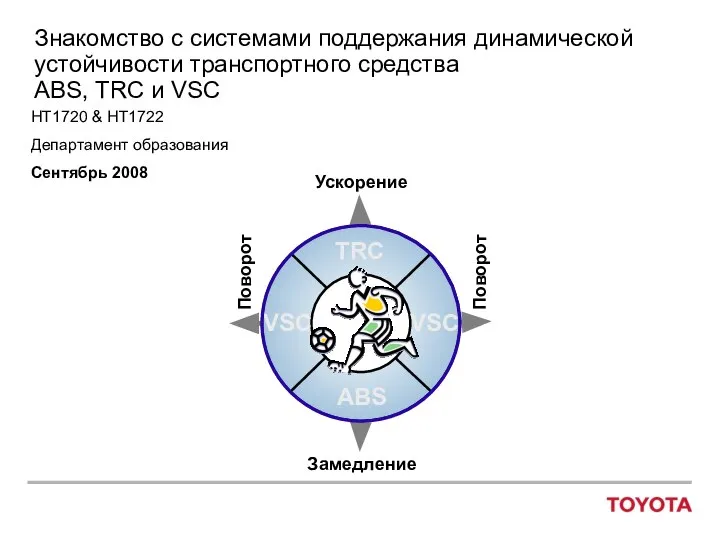 Системы поддержания динамической устойчивости транспортного средства ABS, TRC и VSC
Системы поддержания динамической устойчивости транспортного средства ABS, TRC и VSC Соединение проводников
Соединение проводников Механическая работа. Единицы работы
Механическая работа. Единицы работы Закон всемирного тяготения
Закон всемирного тяготения Телефонная связь
Телефонная связь Презентация по физике "Решение задач по теме: «Механическая работа. Мощность»." - скачать бесплатно
Презентация по физике "Решение задач по теме: «Механическая работа. Мощность»." - скачать бесплатно Радиационная биофизика. Кислородный эффект в радиобиологии. (Лекция 4)
Радиационная биофизика. Кислородный эффект в радиобиологии. (Лекция 4) Жас физик
Жас физик Открытие фотоэффекта. 1886 – 1889 года,
Открытие фотоэффекта. 1886 – 1889 года, Силы, действующие на движущиеся заряды в магнитном поле
Силы, действующие на движущиеся заряды в магнитном поле Форма и ширина спектральной линии
Форма и ширина спектральной линии «Теоретики - они рулевые» или научный путь профессора А. А. Кислицына
«Теоретики - они рулевые» или научный путь профессора А. А. Кислицына Теоретическая механика. Криволинейное движение (задачи)
Теоретическая механика. Криволинейное движение (задачи) Скорость. Единицы скорости
Скорость. Единицы скорости Введение в квантовую физику
Введение в квантовую физику Радиационные эффекты и уровни радиации
Радиационные эффекты и уровни радиации Дослідження процесів комбінованого видавлювання складнопрофільованих деталей з радіальною течією металу
Дослідження процесів комбінованого видавлювання складнопрофільованих деталей з радіальною течією металу Наземные телескопы
Наземные телескопы