Содержание
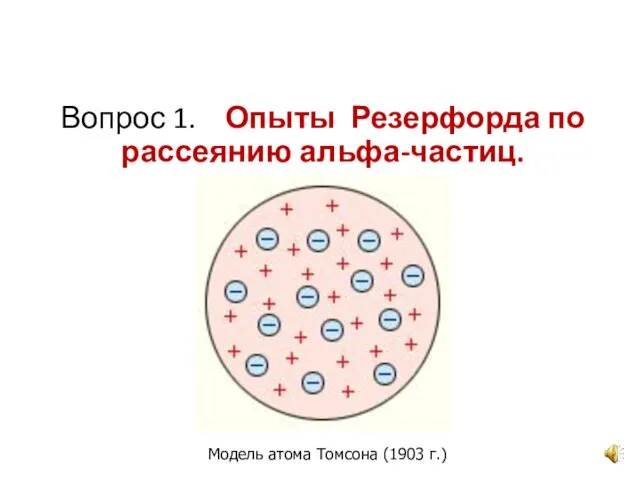
- 2. Вопрос 1. Опыты Резерфорда по рассеянию альфа-частиц. Модель атома Томсона (1903 г.)
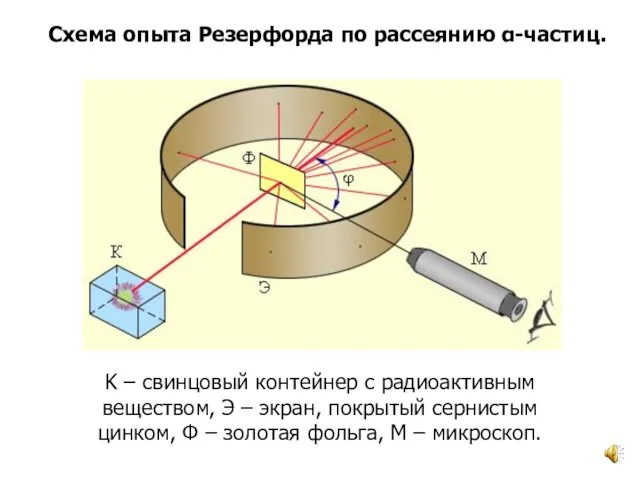
- 3. Схема опыта Резерфорда по рассеянию α-частиц. K – свинцовый контейнер с радиоактивным веществом, Э – экран,
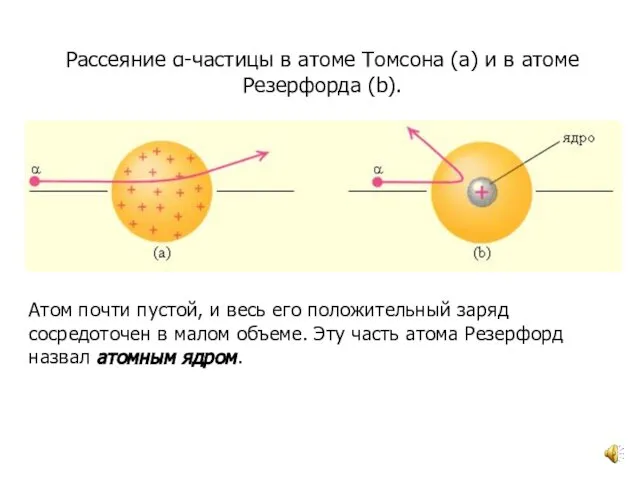
- 4. Рассеяние α-частицы в атоме Томсона (a) и в атоме Резерфорда (b). Атом почти пустой, и весь
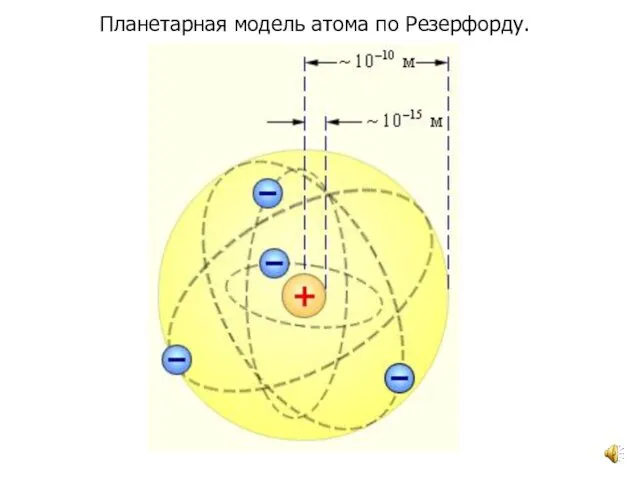
- 5. Планетарная модель атома по Резерфорду.
- 6. Вопрос 1. Строение атомного ядра. Атомные ядра различных элементов состоят из двух частиц – протонов и
- 7. Нейтрон – это элементарная частица, не имеет электрического заряда. Масса нейтрона mn = 1,675·10–27 кг или
- 8. Число протонов, входящих в состав атомного ядра, обозначают символом Z и называют зарядовым числом или атомным
- 9. Ядра одного и того же химического элемента могут отличаться числом нейтронов. Такие ядра называются изотопами. У
- 10. Вопрос 2. Энергия связи ядра. Дефект массы. Силы, удерживающие нуклоны в ядре, называются ядерными. Ядерные силы
- 11. Энергия связи ядра равна минимальной энергии, которую необходимо затратить для полного расщепления ядра на отдельные частицы.
- 12. Рассчитаем в качестве примера энергию связи ядра гелия , в состав которого входят два протона и
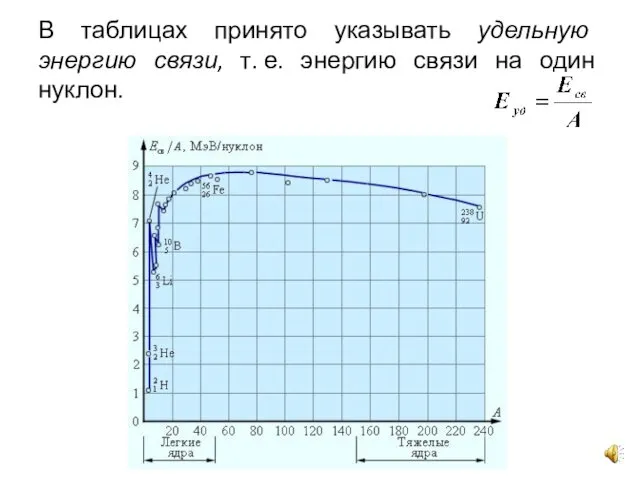
- 13. В таблицах принято указывать удельную энергию связи, т. е. энергию связи на один нуклон.
- 15. Скачать презентацию







 Аттестационная работа. Программа курса по выбору Мои открытия. (7 класс)
Аттестационная работа. Программа курса по выбору Мои открытия. (7 класс) Магнитное поле токов. Часть II. Электричество и магнетизм
Магнитное поле токов. Часть II. Электричество и магнетизм Виды излучений. Спектры
Виды излучений. Спектры Давление. Решение задач
Давление. Решение задач Построение изображений в линзах
Построение изображений в линзах Электромагнитные волны
Электромагнитные волны Учет влияния параметров двухцепных ЛЭП при симметричных коротких замыканиях при коррекции уставок релейной защиты
Учет влияния параметров двухцепных ЛЭП при симметричных коротких замыканиях при коррекции уставок релейной защиты Лабораторная работа. Изучение динамики вращения движения твёрдого тела и определение момента инерции маятника Обербека
Лабораторная работа. Изучение динамики вращения движения твёрдого тела и определение момента инерции маятника Обербека Измерение физической величины (Лекция № 6)
Измерение физической величины (Лекция № 6) Розв'язання задач. Закони Ньютона
Розв'язання задач. Закони Ньютона Аттестационная работа. Формирование проектной и исследовательской деятельности учащихся на уроках физики
Аттестационная работа. Формирование проектной и исследовательской деятельности учащихся на уроках физики Хаос и катастрофы
Хаос и катастрофы Закон Архимеда
Закон Архимеда  Презентация по физике "Измерение ускорения свободного падения" - скачать
Презентация по физике "Измерение ускорения свободного падения" - скачать  Коротаева И. А. МОУ СОШкола №98
Коротаева И. А. МОУ СОШкола №98 Шкалы разные нужны, шкалы всякие важны Какие существуют шкалы для измерения температуры?
Шкалы разные нужны, шкалы всякие важны Какие существуют шкалы для измерения температуры? Синергетика – новое междисциплинарное научное направление
Синергетика – новое междисциплинарное научное направление Динамика поступательного и вращательного движения твердого тела
Динамика поступательного и вращательного движения твердого тела Внутренняя энергия и способы ее изменения. Тест
Внутренняя энергия и способы ее изменения. Тест Презентация Масса тела. Единицы массы. Измерение массы на весах.
Презентация Масса тела. Единицы массы. Измерение массы на весах.  Радиоактивное загрязнение территории
Радиоактивное загрязнение территории Синергетика
Синергетика Иллюзии. 9 класс
Иллюзии. 9 класс Кто или что движется быстрее?
Кто или что движется быстрее? «Путешествие в страну любознательных физиков»
«Путешествие в страну любознательных физиков» Строение атома. Опыты резерфорда
Строение атома. Опыты резерфорда Анималистика в металлопластике
Анималистика в металлопластике Методы машинного обучения для краткосрочного прогноза стока почвенных вод
Методы машинного обучения для краткосрочного прогноза стока почвенных вод