Содержание
- 2. СТРОЕНИЕ АТОМА. ОПЫТЫ РЕЗЕРФОРДА. План урока: Изучение нового материала. Закрепление материала. Домашнее задание.
- 3. МОДЕЛЬ АТОМА ТОМСОНА Положительный заряд занимает весь объем атома и распределен в атоме равномерно; электроны находятся
- 4. Модель атома Томсона Джозеф Джон Томсон (1856 – 1940) Атом представляет собой непрерывно заряженный положительным зарядом
- 5. Модель атома Резерфорда Эрнест Резерфорд (1871 – 1937) Экспериментально исследовал распределение положительного заряда. В 1906 г.
- 6. ИДЕЯ РЕЗЕРФОРДА Резерфорд предложил исследовать атомные ядра с помощью альфа-частиц. Альфа частицы (α-частицы) – ядра атома
- 7. УСТАНОВКА РЕЗЕРФОРДА В свинцовый цилиндр помещен радиоактивный элемент; Через высверленный канал α-частицы попадают на тонкую золотую
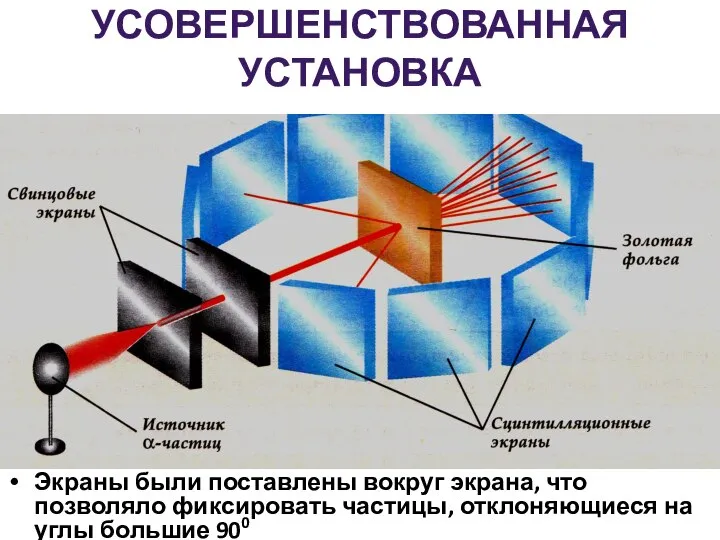
- 8. УСОВЕРШЕНСТВОВАННАЯ УСТАНОВКА Экраны были поставлены вокруг экрана, что позволяло фиксировать частицы, отклоняющиеся на углы большие 900
- 9. ВЫВОДЫ ИЗ ЭКСПЕРИМЕНТА: При распределении по всему атомному ядру положительный заряд не даст достаточно сильное поле
- 10. АТОМНОЕ ЯДРО ПО РЕЗЕРФОРДУ Атомное ядро – тело малых размеров, в котором сконцентрированы почти вся масса
- 11. «АТОМИУМ» ПАМЯТНИК АТОМНОЙ ТЕОРИИ В БРЮССЕЛЕ.
- 12. ПРОТИВОРЕЧИЯ (КАК ВСЕГДА…) Планетарная модель атома не могла объяснить устойчивости атома. Положительное ядро и отрицательный электрон
- 13. ВЫХОД ЕСТЬ! Все эти противоречия были разрешены Нильсом Бором, который сформулировал свои постулаты.
- 14. КВАНТОВЫЕ ПОСТУЛАТЫ БОРА.
- 15. ВТОРОЙ ЗАКОН НЬЮТОНА ДЛЯ ЭЛЕКТРОНА В АТОМЕ. Кулоновская сила притяжения к протону сообщает электрону центростремительное ускорение
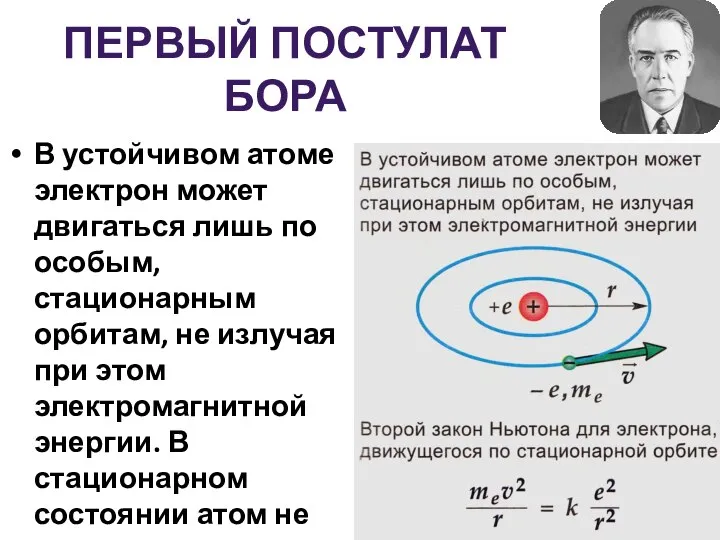
- 16. ПЕРВЫЙ ПОСТУЛАТ БОРА В устойчивом атоме электрон может двигаться лишь по особым, стационарным орбитам, не излучая
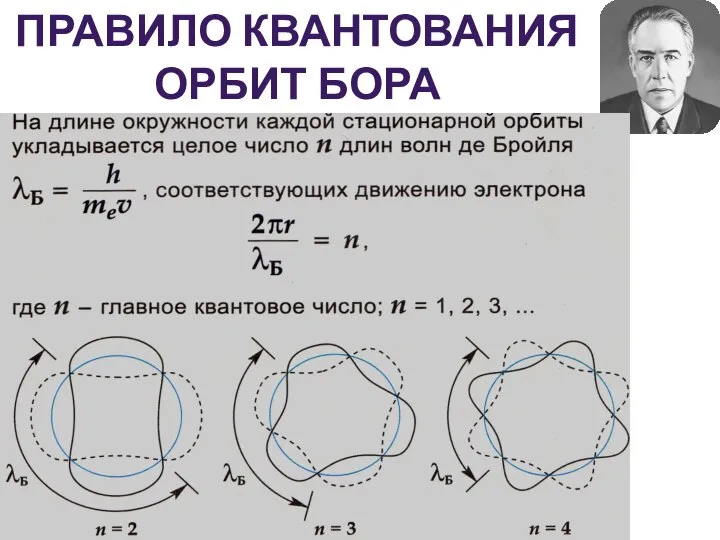
- 17. ПРАВИЛО КВАНТОВАНИЯ ОРБИТ БОРА
- 18. ВТОРОЙ ПОСТУЛАТ БОРА
- 19. ЗАКРЕПЛЕНИЕ МАТЕРИАЛА Что из себя представляет модель атома по Томсону? Что такое α-частицы? Почему отрицательно заряженные
- 21. Скачать презентацию















 Массоперенос между фазами и в пределах фазы. (Темы 5.1 - 5.2)
Массоперенос между фазами и в пределах фазы. (Темы 5.1 - 5.2)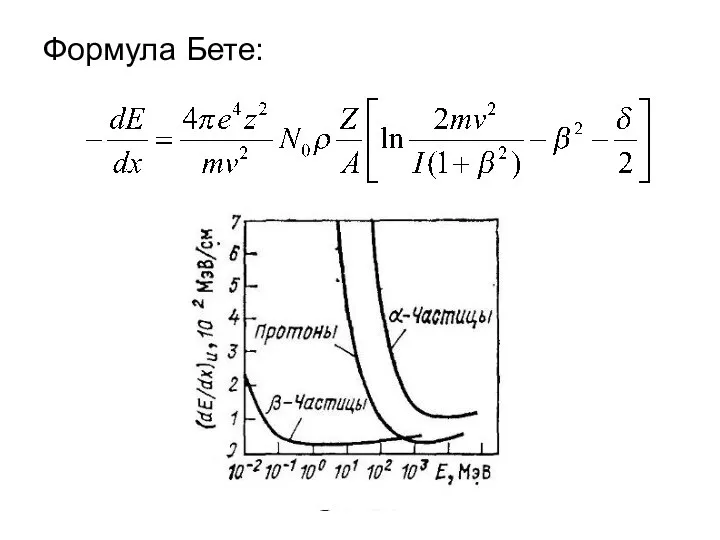 Формула Бете. (Лекция 4)
Формула Бете. (Лекция 4) Презентация по физике "«Открытие нейтрона. Строение атомного ядра»" - скачать
Презентация по физике "«Открытие нейтрона. Строение атомного ядра»" - скачать  Резистор, конденсатор, катушка индуктивности в цепи переменного тока
Резистор, конденсатор, катушка индуктивности в цепи переменного тока Поршневой жидкостный насос. Водопровод
Поршневой жидкостный насос. Водопровод Сосуды под давлением ЗАО «Силд Эйр Каустик»
Сосуды под давлением ЗАО «Силд Эйр Каустик» Досрочный ЕГЭ по физике 2017
Досрочный ЕГЭ по физике 2017 Гамма – излучение
Гамма – излучение Эмиссионный микроспектральный анализ с лазерным отбором пробы
Эмиссионный микроспектральный анализ с лазерным отбором пробы Feedback loops
Feedback loops Применение игровых технологий на уроках физики
Применение игровых технологий на уроках физики Количество теплоты
Количество теплоты Основы теории антенн. Лекция № 6. АФУ
Основы теории антенн. Лекция № 6. АФУ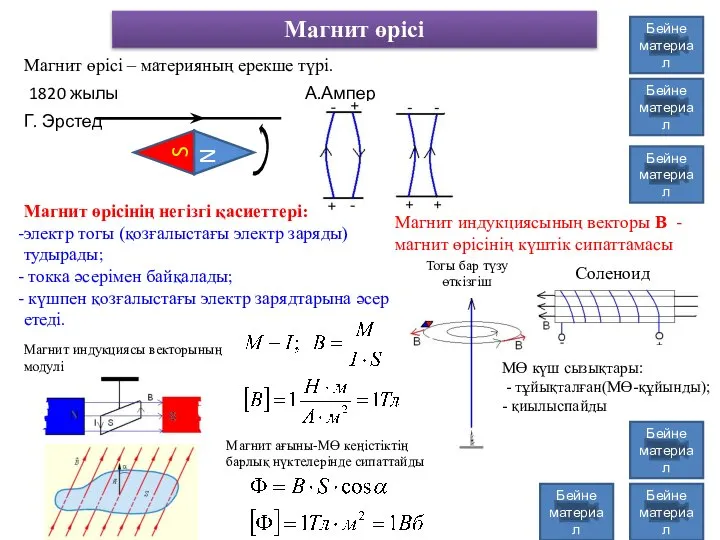 Магнит өрісі
Магнит өрісі Диэлектрики в электрическом поле
Диэлектрики в электрическом поле Развитие средств связи
Развитие средств связи Презентация по физике "Простые механизмы" - скачать бесплатно
Презентация по физике "Простые механизмы" - скачать бесплатно Электричество и магнетизм Закон Кулона. Напряженность. Электрический диполь. Потенциал.
Электричество и магнетизм Закон Кулона. Напряженность. Электрический диполь. Потенциал. 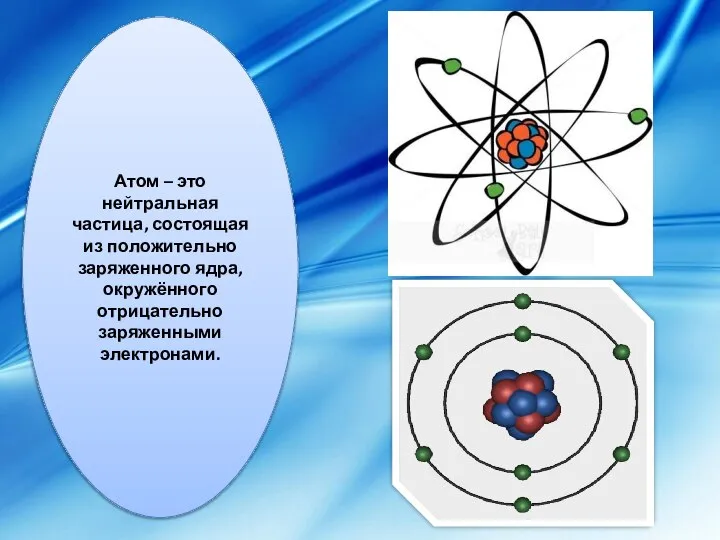 Нейтральная частица атом
Нейтральная частица атом Силы в природе
Силы в природе РЕГУЛЯРНЫЕ ИЗМЕНЕНИЯ ГРАВИТАЦИОННОГО ПОЛЯ КАК РИТМОЗАДАЮЩИЙ ФАКТОР ФИЗИКО-ХИМИЧЕСКИХ И БИОЛОГИЧЕСКИХ ПРОЦЕССОВ (Арктическ
РЕГУЛЯРНЫЕ ИЗМЕНЕНИЯ ГРАВИТАЦИОННОГО ПОЛЯ КАК РИТМОЗАДАЮЩИЙ ФАКТОР ФИЗИКО-ХИМИЧЕСКИХ И БИОЛОГИЧЕСКИХ ПРОЦЕССОВ (Арктическ Эффективность циклона
Эффективность циклона Сила пружності. Закон Гука
Сила пружності. Закон Гука Пара сил. (Лекция 3)
Пара сил. (Лекция 3) Тепловые двигатели Выполнила Ч. Валерия 8 В класс
Тепловые двигатели Выполнила Ч. Валерия 8 В класс Презентация по физике. Тема: Цепная реакция деления ядер урана . Класс: 9 «б»
Презентация по физике. Тема: Цепная реакция деления ядер урана . Класс: 9 «б» Презентация по физике "Система охлаждения" - скачать
Презентация по физике "Система охлаждения" - скачать  Раздел «Электричество»
Раздел «Электричество»