Содержание
- 2. Цель урока: преобразования ядер химических элементов, раскрыть природу радиоактивного распада, его закономерностей.
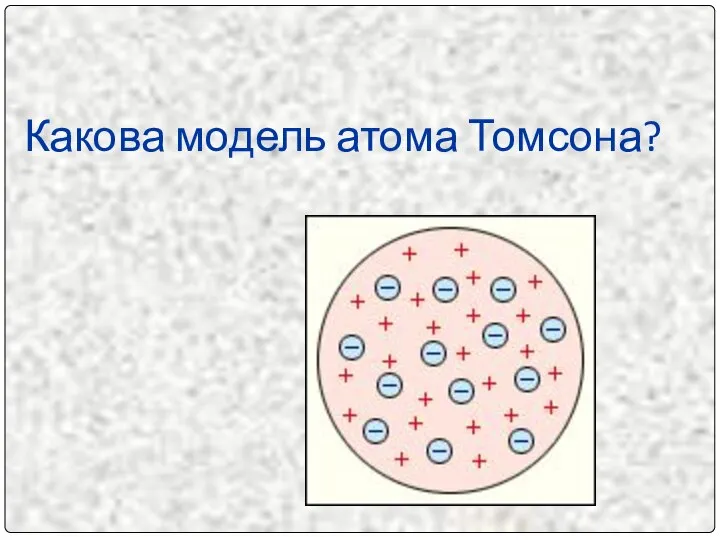
- 3. Какова модель атома Томсона?
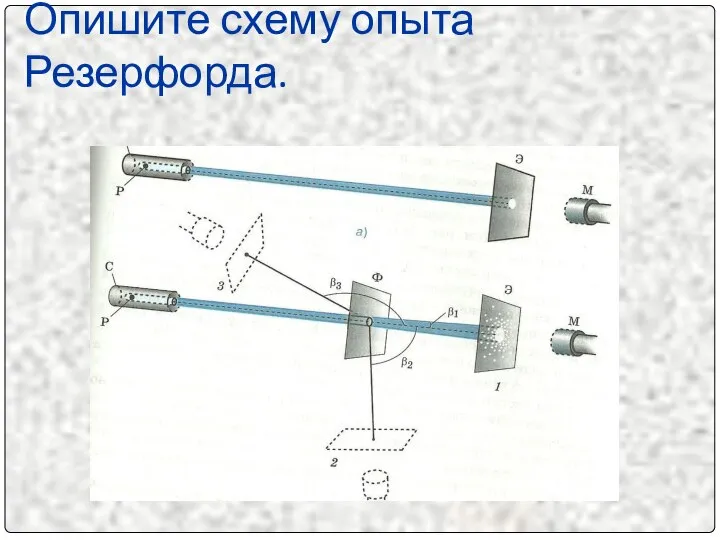
- 4. Опишите схему опыта Резерфорда.
- 5. Какие результаты были получены в ходе опыта? Отклонение альфа-частиц от прямолинейного распространения . Одна две альфа
- 6. Какую модель атома предложил Резерфорд? Планетарная модель атома Резерфорда
- 7. Вспомним строение атома из 8 кл.
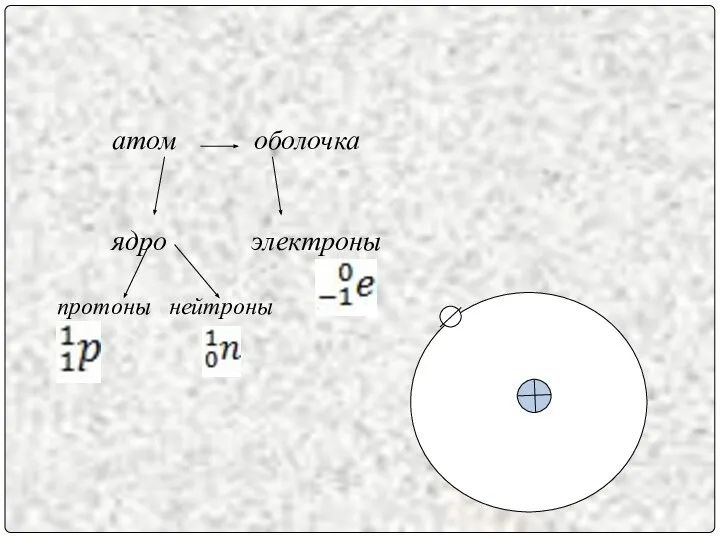
- 8. атом оболочка ядро электроны протоны нейтроны
- 9. Как записать любой химический элемент виде символа? А – атомная масса или массовое число Z –
- 10. Объясните выражение A=Z+N
- 11. Какова природа α –β –γ – излучения? α - излучение - β – излучение - γ
- 12. Фредерик Содди 1877-1956 В 1902 году Эрнест Резерфорд 1871-1937
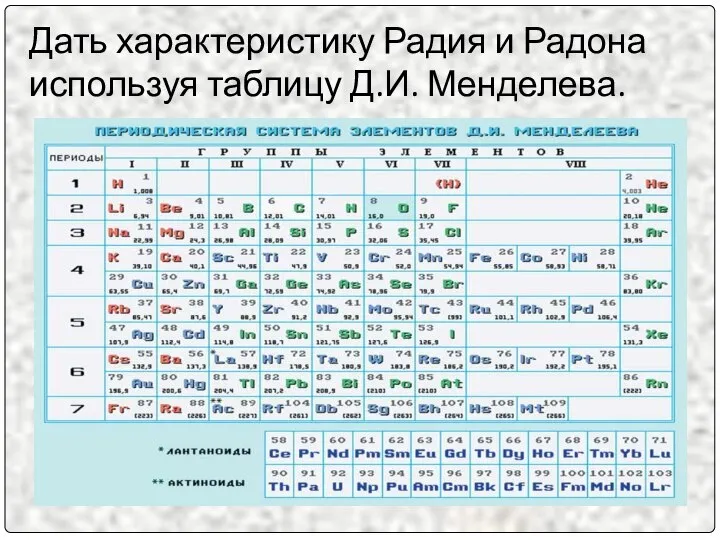
- 14. Дать характеристику Радия и Радона используя таблицу Д.И. Менделева.
- 15. Законы радиоактивного распада Смещение элемента на две клетки к началу таблицы
- 16. Законы радиоактивного распада Смещение элемента на одну клетку к концу таблицы
- 17. Законы радиоактивного распада γ – излучение - излучают ядра химических элементов находящихся в возбуждённом состоянии, поэтому
- 18. Вывод: При радиоактивном распаде претерпевают изменения ядра химических элементов
- 19. Выполняются законы сохранения зарядового и массового чисел 226=4 + 222 88 =2 + 86
- 20. Вывод: Из открытия Резерфорда и Содди следует, что Ядра атомов имеют сложный состав; Радиоактивность – способность
- 21. В ядро какого элемента превращается изотоп тория , если ядро испытывает три α - распада?
- 23. В ядро какого элемента превращается в результате β – распада ?
- 25. испытывает α и 2 β – распада. Какое ядро получится в результате этих распадов?
- 27. Домашнее задание: §57, упр. 43 (1-4)
- 28. Спасибо за внимание!!!
- 30. Скачать презентацию








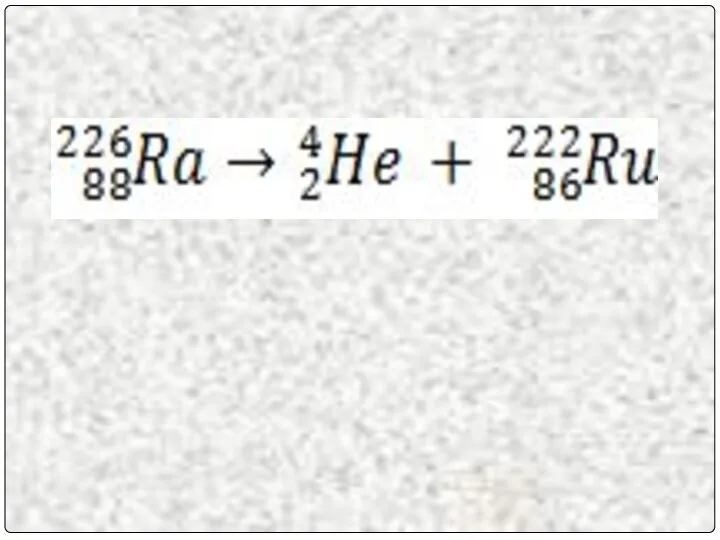














 Квантовые эффекты в нелинейных системах
Квантовые эффекты в нелинейных системах Основы радиосвязи
Основы радиосвязи Биологиялық мембраналар. Құрылымы, қасиеттері және оларды оқыту жолдары
Биологиялық мембраналар. Құрылымы, қасиеттері және оларды оқыту жолдары Аттестационная работа. Программа элективного курса по физике для 10-11 класса Решение нестандартных задач по физике
Аттестационная работа. Программа элективного курса по физике для 10-11 класса Решение нестандартных задач по физике Корреляция
Корреляция Инфракрасная спектроскопия
Инфракрасная спектроскопия Теорія Великого Вибуху. Еволюція всесвіту
Теорія Великого Вибуху. Еволюція всесвіту Самостоятельная работа 66 урок
Самостоятельная работа 66 урок Техническое обслуживание и текущий ремонт двигателя, системы охлаждения и смазки
Техническое обслуживание и текущий ремонт двигателя, системы охлаждения и смазки Катушка индуктивности
Катушка индуктивности Основні поняття термодинаміки
Основні поняття термодинаміки Корпускулярно-волновой дуализм света
Корпускулярно-волновой дуализм света Презентация по физике "Лауреаты Нобелевской премии по физике и химии" - скачать
Презентация по физике "Лауреаты Нобелевской премии по физике и химии" - скачать  Тести по КЕ
Тести по КЕ Гидрогазодинамика. Основные понятия механики жидкостей и газов
Гидрогазодинамика. Основные понятия механики жидкостей и газов Презентация по физике "Динамика Масса Импульс" - скачать
Презентация по физике "Динамика Масса Импульс" - скачать  Задачи по физике для учащихся 7 класса
Задачи по физике для учащихся 7 класса Отражение и преломление электромагнитных волн на границе раздела сред
Отражение и преломление электромагнитных волн на границе раздела сред Закон Архимеда 2005
Закон Архимеда 2005  Твердая фаза и поровое пространство почв. Плотность почвы
Твердая фаза и поровое пространство почв. Плотность почвы Формула Максвелла для относительных скоростей
Формула Максвелла для относительных скоростей Квантовая радиофизика. Лекция 5. Практическая ЯМР- спектроскопия
Квантовая радиофизика. Лекция 5. Практическая ЯМР- спектроскопия Коливальний рух. Амплітуда коливань. Період коливань. Маятники
Коливальний рух. Амплітуда коливань. Період коливань. Маятники Закон сохранения и превращения энергии в механических и тепловых процессах.
Закон сохранения и превращения энергии в механических и тепловых процессах. Кинетика ферментативных реакций
Кинетика ферментативных реакций Второе начало термодинамики и энтропия
Второе начало термодинамики и энтропия Закон сохранения импульса. Реактивное движение
Закон сохранения импульса. Реактивное движение Молекулярная физика и термодинамика Дмитриевский Александр Александрович 2010
Молекулярная физика и термодинамика Дмитриевский Александр Александрович 2010