Температура. Уравнение состояния Примем в качестве постулата, что в состоянии хаотического движения молекул газа имеет место
Содержание
- 2. Если обозначить среднюю энергию молекулы, приходящуюся на одну степень свободы через , то полная кинетическая энергия
- 3. Теперь рассмотрим вопрос о тепловом равновесии газов и введем понятие температура. Закон равнораспределения энергии применим и
- 4. Это равенство означает, что при столкновениях молекул разной массы происходит «обмен энергией» между ними, до тех
- 5. Этот результат соответствует наступлению теплового равновесия – состояния, в котором каждый из газов передает другому такое
- 6. Сделаем теперь предположение общего характера. Предположим, что любая макроскопическая система, будь то газ, или жидкость, или
- 7. Соотношение (2.15) показывает, что для идеальных газов можно принять в качестве термодинамической температуры непосредственно саму среднюю
- 8. Учитывая теперь, что полная кинетическая энергия поступательного движения всех молекул газа равна , и используя (2.16)
- 9. Уравнение состояния (2.18) связывает три макроскопических параметра, характеризующих состояние газа – объем, давление и температуру. При
- 10. Изотермический процесс можно осуществить если сжимать или расширять газ достаточно медленно, так, чтобы в любой момент
- 12. Скачать презентацию









 Магнитное поле
Магнитное поле Намагничивание магнетиков. Классификация магнетиков
Намагничивание магнетиков. Классификация магнетиков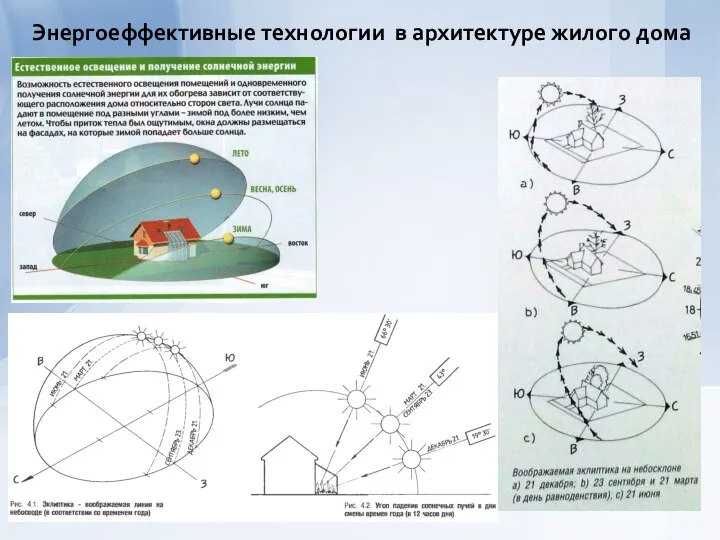 Энергоеффективные технологии в архитектуре жилого дома
Энергоеффективные технологии в архитектуре жилого дома Магнитное поле Земли
Магнитное поле Земли Основы электротехники и электроники
Основы электротехники и электроники Презентация по физике "Электрические явления в физике и пропорциональность в математике" - скачать
Презентация по физике "Электрические явления в физике и пропорциональность в математике" - скачать  Голография. Что такое голография
Голография. Что такое голография Рычаг и блок
Рычаг и блок Установка и стабилизация управляемых колес
Установка и стабилизация управляемых колес Общероссийский фестиваль исследовательских и творческих работ учащихся Общероссийский фестиваль исследовательских и творчески
Общероссийский фестиваль исследовательских и творческих работ учащихся Общероссийский фестиваль исследовательских и творчески Рентгеновское излучение
Рентгеновское излучение Закон сохранения импульса
Закон сохранения импульса  Вынужденные колебания. Резонанс
Вынужденные колебания. Резонанс Автоколлимационная зрительная труба. Автоколлимационный окуляр. Измерительный микроскоп
Автоколлимационная зрительная труба. Автоколлимационный окуляр. Измерительный микроскоп Радиационный теплообмен. Основные понятия радиационного переноса теплоты. (Тема 3. Лекции 10,11)
Радиационный теплообмен. Основные понятия радиационного переноса теплоты. (Тема 3. Лекции 10,11) Презентация Колебания и волны
Презентация Колебания и волны  Бензиновые двигатели
Бензиновые двигатели Физика вокруг нас Пословицы и поговорки Учитель физики МОУСОШ №19 Крапивенцева М.Ю.
Физика вокруг нас Пословицы и поговорки Учитель физики МОУСОШ №19 Крапивенцева М.Ю. Проектирование МДП СБИС. Структуры МДП в СБИС
Проектирование МДП СБИС. Структуры МДП в СБИС Медициналық интроскопияның негізгі техникалық құралдары. Фотоэлектрлік түрлендіргіштер
Медициналық интроскопияның негізгі техникалық құралдары. Фотоэлектрлік түрлендіргіштер Электрическое поле. Напряженность электрического поля
Электрическое поле. Напряженность электрического поля Атмосферное давление
Атмосферное давление Закон Гука и модуль Юнга
Закон Гука и модуль Юнга Презентация Золотое правило механики
Презентация Золотое правило механики  Модернизация системы главной понизительной подстанции механического завода
Модернизация системы главной понизительной подстанции механического завода Измерение жесткости пружины
Измерение жесткости пружины TES, TEC, KES salīdzinājums un klasifikācija, galvenās prasības
TES, TEC, KES salīdzinājums un klasifikācija, galvenās prasības Презентация на тему: Законы Ньютона
Презентация на тему: Законы Ньютона