Содержание
- 2. Нужны умные, образованные люди; по мере приближения человечества к лучшей жизни число этих людей будет увеличиваться,
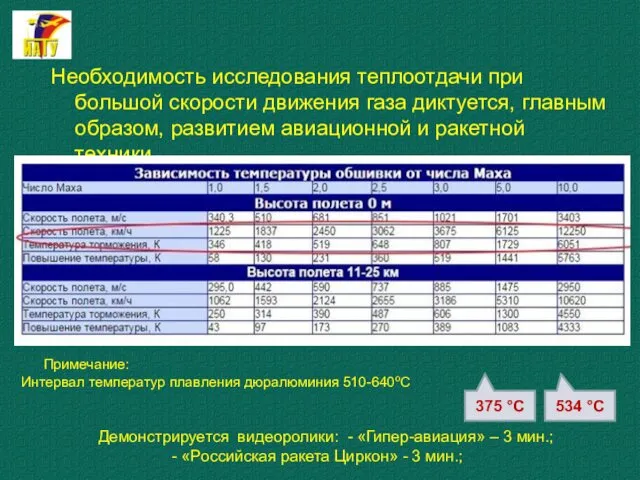
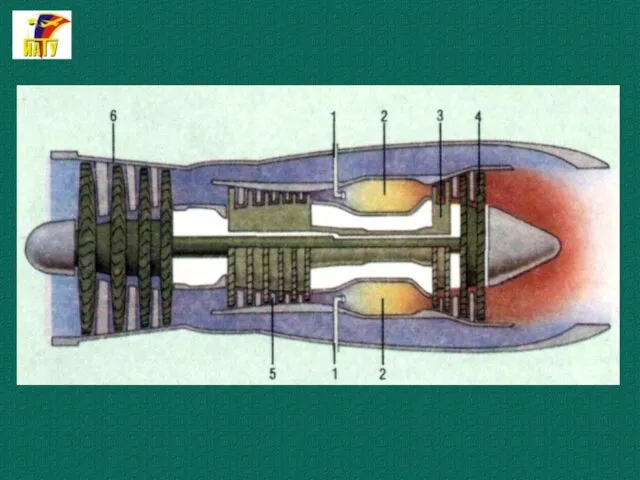
- 3. Необходимость исследования теплоотдачи при большой скорости движения газа диктуется, главным образом, развитием авиационной и ракетной техники.
- 4. Лекция № 1 по дисциплине «Термодинамика и теплопередача» «Термодинамика как наука. Основные понятия термодинамики»
- 8. 1. Цели и задачи изучения дисциплины Целями дисциплины «Термодинамика и теплопередача» является подготовка студентов к эффективной
- 9. В результате изучения дисциплины студент должен: знать: - термодинамические процессы происходящие в газах, парах и их
- 10. Порядок изучения дисциплины Раздел Термодинамика – 16 часов; Раздел Теплопередача – 16 часов. Для очной формы
- 11. 2. Первый закон термодинамики. Основные понятия и определения
- 12. 2.1.Термодинамическая система и окружающая среда Термодинамической системой называется совокупность материальных тел, являющихся объектом изучения и находящихся
- 15. Термодинамическая система и окружающая среда Термодинамические системы бывают: - изолированными, полуизолированными и неизолированными; - физически однородными,
- 16. Основные термодинамические параметры состояния Каждое состояние термодинамической системы характ-изуется определенными физическими величинами. Внутренние характеризуют внутреннее состояние
- 17. Для характеристики конкретных условий, в которых находится данная система, необходимо знать такие внутренние параметры состояния, как
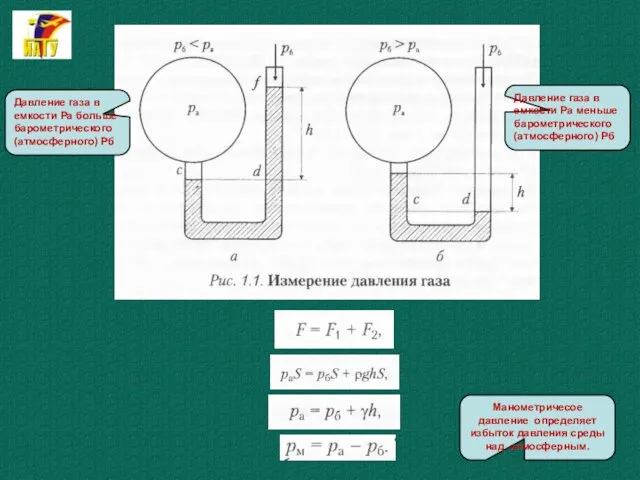
- 20. Различают давления атмосферное, избыточное и разрежение (вакуум). Атмосферным называется давление атмосферного воздуха на уровне моря. За
- 21. Давление газа в емкости Ра больше барометрического (атмосферного) Рб Давление газа в емкости Ра меньше барометрического
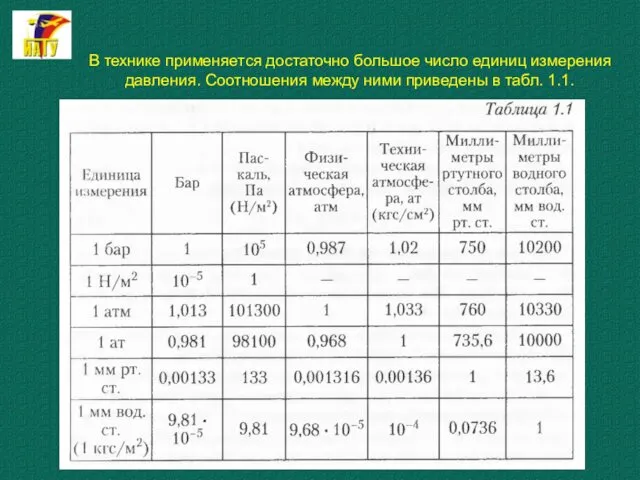
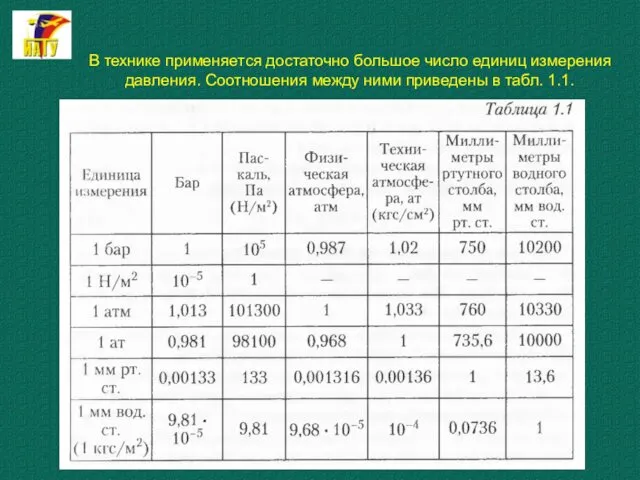
- 22. В технике применяется достаточно большое число единиц измерения давления. Соотношения между ними приведены в табл. 1.1.
- 23. В технике применяется достаточно большое число единиц измерения давления. Соотношения между ними приведены в табл. 1.1.
- 25. Взаимосвязь между средней кинетической энергией поступательного движения молекул mw2/2 и абсолютной температурой идеального газа Т описывается
- 26. Термодинамический процесс Состояние термодинамической системы может быть равновесным и неравновесным. Равновесным называется такое состояние системы, при
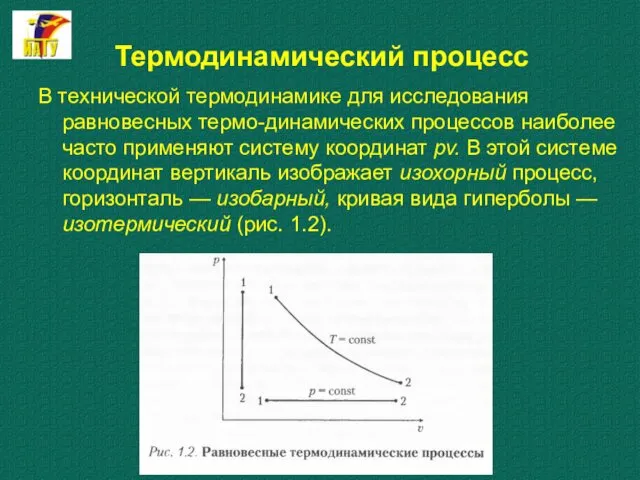
- 27. Термодинамический процесс В технической термодинамике для исследования равновесных термо-динамических процессов наиболее часто применяют систему координат pv.
- 28. Уравнения состояния Уравнение состояния идеального газа впервые было получено Клапей-роном в 1834 г, путем объединения уравне
- 33. Уравнения состояния реальных газов Реальные газы отличаются от идеальных тем, что их молекулы имеют конечные собственные
- 34. Уравнения состояния реальных газов Уравнение Ван-дер-Ваальса, которое является частным случаем общего уравнения Майера-Боголюбова, было получено в
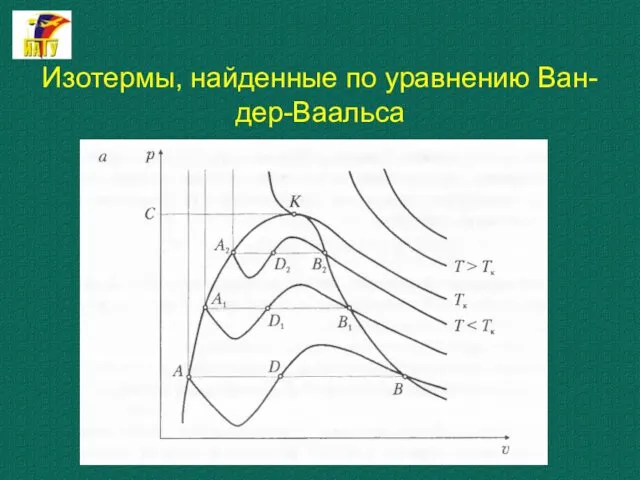
- 35. Изотермы, найденные по уравнению Ван-дер-Ваальса
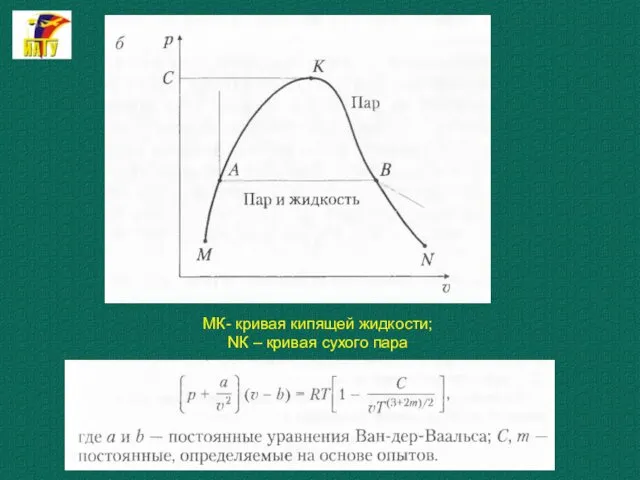
- 36. МК- кривая кипящей жидкости; NК – кривая сухого пара
- 37. 7. Энергия. Внутренняя энергия
- 38. Задание на самостоятельную работу 1. Повторить материал по конспекту. 2. По учебнику проработать материал на стр.
- 40. Скачать презентацию

























 Презентация Неорганическая химия
Презентация Неорганическая химия Нестационарная теплопроводность
Нестационарная теплопроводность Незатухаючі вимушені коливання
Незатухаючі вимушені коливання Кинематика точки
Кинематика точки Внешний фотоэффект. Опыты Столетова
Внешний фотоэффект. Опыты Столетова Выбор входного фильтра инвертора
Выбор входного фильтра инвертора Школа № 625 Н.М.Турлакова
Школа № 625 Н.М.Турлакова Система с использованием ПИД-регулятора для задачи следования по линии
Система с использованием ПИД-регулятора для задачи следования по линии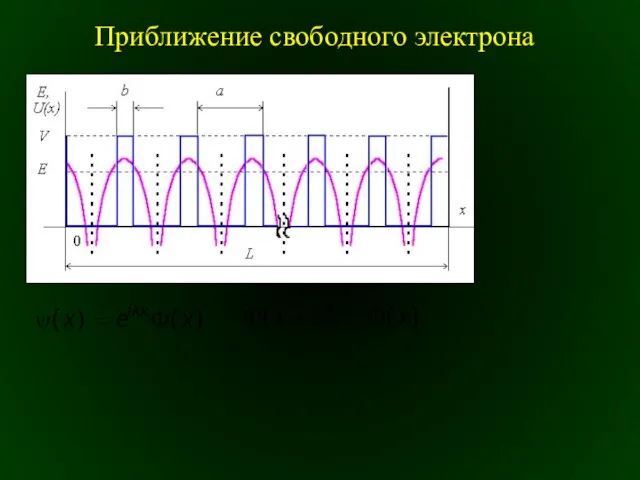 Приближение свободного электрона
Приближение свободного электрона Истина где-то рядом
Истина где-то рядом Интерференция света
Интерференция света Детекторы ионизирующих излучений. Сцинтилляционные методы детектирования ионизирующих излучений
Детекторы ионизирующих излучений. Сцинтилляционные методы детектирования ионизирующих излучений Величины, характеризующие колебательное движение
Величины, характеризующие колебательное движение Плотность. Решение задач
Плотность. Решение задач ЕГЭ ФИЗИКА
ЕГЭ ФИЗИКА Кристаллическое строение металлов
Кристаллическое строение металлов Микроскоп – знакомство, создание, опыты
Микроскоп – знакомство, создание, опыты Расчет установившихся режимов простейших электрических сетей. (Глава 6)
Расчет установившихся режимов простейших электрических сетей. (Глава 6) Транспортная энергетика. Теплопередача. (Лекция 9)
Транспортная энергетика. Теплопередача. (Лекция 9) Перемещение при прямолинейном равномерном движении
Перемещение при прямолинейном равномерном движении Презентация по физике Тепловые явления Выполнила: ученица 8 «А» класса ГОУ СОШ №1973 Прохорчик Светлана
Презентация по физике Тепловые явления Выполнила: ученица 8 «А» класса ГОУ СОШ №1973 Прохорчик Светлана Тема 3 Лекция 8 Магнитное поле в веществе 8.1 Источники магнитного поля вещества. Магнитные моменты элементарных частиц. Магн
Тема 3 Лекция 8 Магнитное поле в веществе 8.1 Источники магнитного поля вещества. Магнитные моменты элементарных частиц. Магн Siłownie turboparowe
Siłownie turboparowe Дисперсия света
Дисперсия света Биномиальное распределение. Схема Бернулли
Биномиальное распределение. Схема Бернулли История создания швейной машины
История создания швейной машины Природа света. Законы геометрической оптики
Природа света. Законы геометрической оптики Масса молекул. Количество вещества
Масса молекул. Количество вещества