Содержание
- 2. Уравнение состояния идеального газа
- 3. Цели урока: познакомиться с уравнением состояния идеального газа; записать это уравнение в классическом виде; рассмотреть следствия,
- 4. Величайшим достижением человеческого гения является то, что человек может понять вещи, которые он уже не в
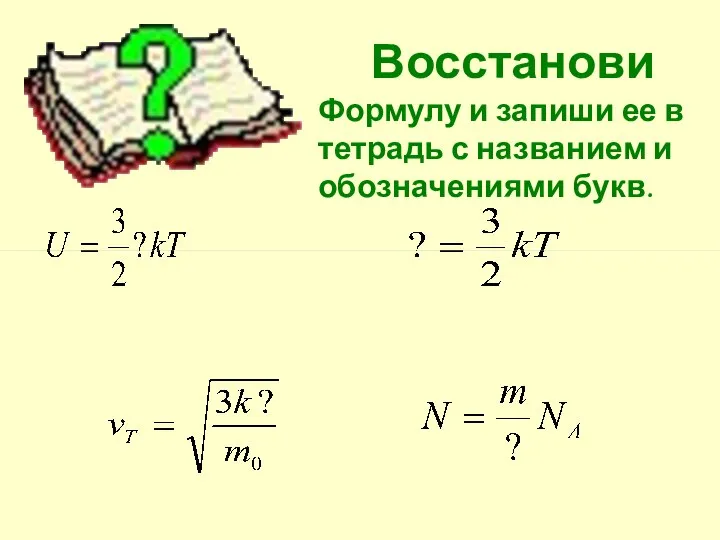
- 5. Восстанови Формулу и запиши ее в тетрадь с названием и обозначениями букв.
- 6. Проверьте свои записи: 1.Зависимость внутренней энергии идеального газа от температуры. k=1,38-23 Дж/К – постоянная Больцмана. Т-темпертура,
- 7. Уравнение состояния вещества Уравнение, выражающее связь между макроскопическими параметрами состояния вещества (p,V и Т), называется уравнением
- 8. Уравнение состояния идеального газа
- 9. R=8,31 Дж / (моль·К) NA k = R Универсальная газовая постоянная - R
- 10. Уравнение Менделеева- Клапейрона 1874
- 11. Дмитрий Иванович Менделеев (1834 – 1907) Крупнейший химик мира, физик, педагог
- 12. Закон Авогадро 1811 При одинаковых температурах и давлениях в равных объемах любых идеальных газов содержится одинаковое
- 13. Закон Дальтона 1801 Давление смеси химически не взаимодействующих идеальных газов равно сумме парциальных давлений этих газов.
- 14. Отношение произведения давления и объема идеального газа к его абсолютной температуре есть величина постоянная для данной
- 15. p0, V0, T0 – параметры начального состояния газа, p, V, T - параметры конечного состояния газа
- 16. Во всем мне хочется дойти до самой сути…
- 17. Обратите внимание: Уравнение Менделеева - Клапейрона связывает между собой 5 физических величин, характеризующих состояние газа, -
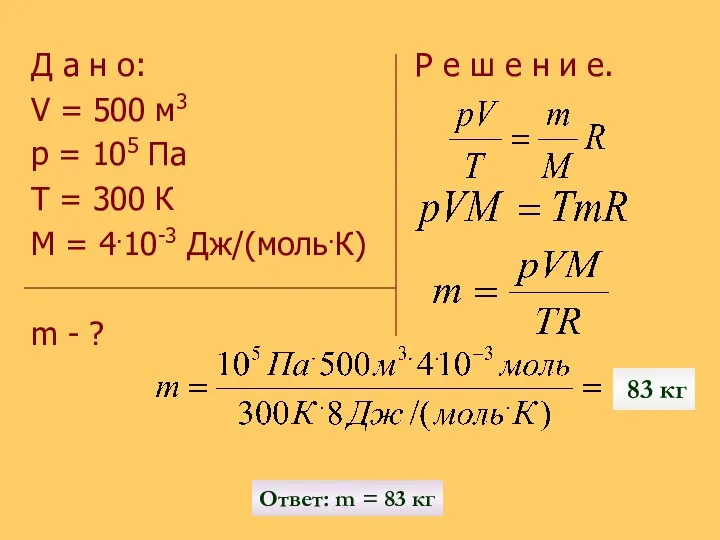
- 18. Р е ш и т ь з а д а ч у: Сколько гелия потребуется для
- 19. Д а н о: Р е ш е н и е. V = 500 м3 p
- 20. Какова плотность сжатого воздуха при 0 0С в камере шины автомобиля «Волга»? Давление 0,17 МПа. Р
- 21. Р е ш е н и е , где 2,17 кг/м3 Р е ш е н
- 23. Скачать презентацию


















 Электролиз. Использование электролиза
Электролиз. Использование электролиза Явление электромагнитной индукции
Явление электромагнитной индукции Единицы силы. Связь между силой тяжести и массой тела
Единицы силы. Связь между силой тяжести и массой тела Изотопная геология (введение)
Изотопная геология (введение) Линзы. Оптическая сила линзы Учитель физики МОУ Будинская ООШ Бабаева Валентина Васильевна.
Линзы. Оптическая сила линзы Учитель физики МОУ Будинская ООШ Бабаева Валентина Васильевна. Automaty a regularní výrazy. (Lekce 3)
Automaty a regularní výrazy. (Lekce 3) Кристаллооптический анализ
Кристаллооптический анализ Магнитное поле
Магнитное поле Розвиток судного та повітряного плавання. Дослід Торрічеллі
Розвиток судного та повітряного плавання. Дослід Торрічеллі Применение аккумуляторов
Применение аккумуляторов Электрондық парамагнитті резонанс (ЭПР) әдісі
Электрондық парамагнитті резонанс (ЭПР) әдісі Открытие протона и нейтрона
Открытие протона и нейтрона Закон преломления света
Закон преломления света Электромагнитная индукция. Закон Фарадея. Правило Ленца. Самоиндукция
Электромагнитная индукция. Закон Фарадея. Правило Ленца. Самоиндукция Первое начало термодинамики
Первое начало термодинамики Система електроживлення, вентиляції, кондиціювання та обігріву. Загальні відомості про систему електроживлення 17Х6. (Тема 9.1)
Система електроживлення, вентиляції, кондиціювання та обігріву. Загальні відомості про систему електроживлення 17Х6. (Тема 9.1) Электрические явления
Электрические явления Водяное охлаждение. Сфера применения
Водяное охлаждение. Сфера применения Философские проблемы науки и техники. Философские основания физики. (Лекция 10)
Философские проблемы науки и техники. Философские основания физики. (Лекция 10) Презентация по физике "Оптика" - скачать
Презентация по физике "Оптика" - скачать  Квантовая радиофизика. Лекция 5. Практическая ЯМР- спектроскопия
Квантовая радиофизика. Лекция 5. Практическая ЯМР- спектроскопия Основные уравнения классической динамики
Основные уравнения классической динамики Малая Распределенная Генерация в России и Мире. Решения для промышленности, ЖКХ и прочих потребителей.
Малая Распределенная Генерация в России и Мире. Решения для промышленности, ЖКХ и прочих потребителей.  Определение расстояния до недоступной точки
Определение расстояния до недоступной точки Второй закон термодинамики
Второй закон термодинамики Оптика 8 класс
Оптика 8 класс Модификация модели сечения выведения для различных спектров. Модификация модели сечения выведения для неводородосодержащих сред
Модификация модели сечения выведения для различных спектров. Модификация модели сечения выведения для неводородосодержащих сред История изобретения паровых машин. Работу выполнила ученица 8б класса МКОУ СОШ пгт Подосиновец Пунченко Анастасия
История изобретения паровых машин. Работу выполнила ученица 8б класса МКОУ СОШ пгт Подосиновец Пунченко Анастасия