Содержание
- 2. ИДЕАЛЬНЫЙ ГАЗ теоретическая модель, широко применяемая для описания свойств и поведения реальных газов при умеренных давлениях
- 3. В основе молекулярно-кинетической теории строения вещества (МКТ) лежат три основных положения: все вещества состоят из мельчайших
- 4. Газ представляет собой собрание молекул, беспорядочно движущихся по всем направлениям независимо друг от друга. Газы не
- 5. Идеальный газ – это газ, взаимодействие между молекулами которого пренебрежимо мало. (Ек>>Ер)
- 6. Свойства идеального газа: расстояние между молекулами много больше размеров молекул; молекулы газа очень малы и представляют
- 7. Состояние некоторой массы газообразного вещества характеризуют зависимыми друг от друга физическими величинами, называемыми параметрами состояния. К
- 8. Объем газа обозначается V. Объем газа всегда совпадает с объемом того сосуда, который он занимает. Единица
- 9. Давление – физическая величина, равная отношению силы F, действующей на элемент поверхности перпендикулярно к ней, к
- 10. УРАВНЕНИЕ МЕНДЕЛЕЕВА-КЛАПЕЙРОНА уравнение состояния для идеального газа, отнесенное к 1 молю газа. В 1874 г. Д.
- 11. pV = RT, где R — универсальная газовая постоянная, R = 8,31 Дж/(моль.К) Уравнение Клапейрона-Менделеева показывает,
- 12. ЗАКО́Н АВОГА́ДРО закон, согласно которому в равных объёмах различных газов, взятых при одинаковых температурах и давлениях,
- 13. CЛЕДСТВИЯ ИЗ ЗАКОНА АВОГАДРО: 1 следствие: Одинаковое число молекул различных газов при одинаковых условиях занимает одинаковый
- 14. Молярный объём – это постоянная величина для веществ – газов при нормальных условиях (н.у.): Vm =
- 16. Взаимосвязь молярной массы, молярного объёма, числа Авогадро и количества вещества: υ = V / Vm =
- 17. ЗАКОН ДАЛЬТОНА Парциальное давление каждого газа, входящего в состав смеси, это давление, которое создавалось бы той
- 18. Как уже отмечалось, отдельные компоненты смеси газов считаются независимыми. Поэтому каждая компонента создает давление: p=pikT(1),p=pikT(1), а
- 19. ИСТОЧНИКИ ИНФОРМАЦИИ: https://bb31e6b6-a-62cb3a1a-s-sites.googlegroups.com/site/himulacom/zvonok-na-urok/8-klass/urok-no59-zakon-avogadro-molarnyj-obeem-gazov/%D0%B7%D0%B0%D0%BA%D0%BE%D0%BD%20%D0%B0%D0%B2%D0%BE%D0%B3%D0%B0%D0%B4%D1%80%D0%BE.jpg?attachauth=ANoY7cqfdSgc5Lj6XJ4zYchp4Ko-IQSptXxIjbU81ii3boXENVZcTDHyJ5kNBgiQzT8pK4SCHeKzAmfaxad8JokGUWuWidCEaFDXK9Obfe9dq9Xt8lLByCiWR-MKhHacLz9q522oFEfV6r8bYE2ZgWuvcBTBxPGXWe231J_r1RDh-a5Bv3iKBBxwPidn7BVDceB1h5objfwWGvnw8solGkoCb2YVtVKXWTMSskMr6SmTZT6ydGXRbVTiDlWJqqOoE4V4bJSTrKufVtlSf8ke5bHXNvFddq-IpG7wbnDWMPXHCUrFvOZyFaUHmreq-I-7hQ5806zDtXH_j43S2m5lg7GKWQ85iSfz3mtZ9C5ltmAdMY4X_VRa_ca2W0lxlKS8BtkJaMQElqEkucoQbWn6jE0Htr0uS99NXg%3D%3D&attredirects=0 ФОТО http://fn.bmstu.ru/data-physics/library/physbook/tom2/ch2/texthtml/ch2_1.htm Физика. 10 класс: учеб, для общеобразоват. организаций с прил. на электрон,
- 21. Скачать презентацию


















 Газокинетическое уравнение переноса нейтронов в неразмножающей среде. Уравнение баланса нейтронов. Граничные условия
Газокинетическое уравнение переноса нейтронов в неразмножающей среде. Уравнение баланса нейтронов. Граничные условия Основы квантовой физики. Лазеры
Основы квантовой физики. Лазеры Скорость. Расчет пути и времени
Скорость. Расчет пути и времени Решение задач механики различными способами - Презентация_
Решение задач механики различными способами - Презентация_ Растяжение - сжатие
Растяжение - сжатие Презентация по физике "Закон сохранения энергии в тепловых процессах" - скачать
Презентация по физике "Закон сохранения энергии в тепловых процессах" - скачать  Комплексная интерпритация геофизических исследований скважин
Комплексная интерпритация геофизических исследований скважин Сравнительная характеристика проводниковых материалов. Медь и алюминий
Сравнительная характеристика проводниковых материалов. Медь и алюминий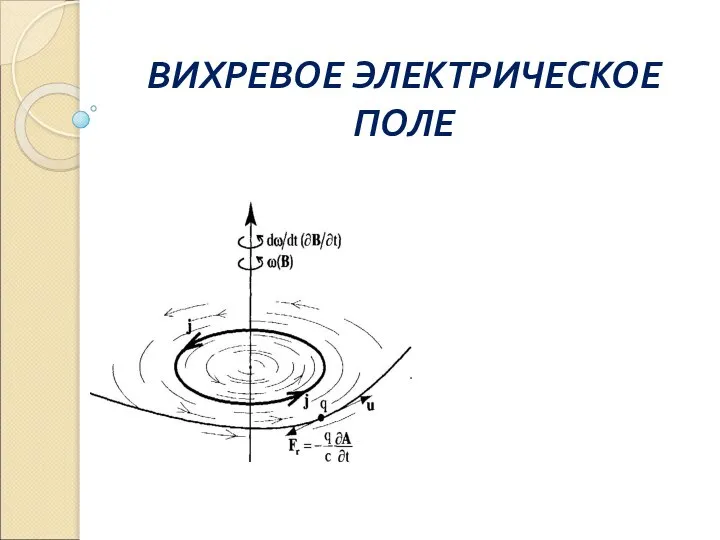 ВИХРЕВОЕ ЭЛЕКТРИЧЕСКОЕ ПОЛЕ
ВИХРЕВОЕ ЭЛЕКТРИЧЕСКОЕ ПОЛЕ  Электроны. История открытия.
Электроны. История открытия. Комплексные методы анализа ГХ-МС и ВЭЖХ-МС
Комплексные методы анализа ГХ-МС и ВЭЖХ-МС Теплотехника. Паросиловая установка. (Лекция 10)
Теплотехника. Паросиловая установка. (Лекция 10) Электризация тел при соприкосновении. Взаимодействие заряженных тел. Урок физики в 8 классе
Электризация тел при соприкосновении. Взаимодействие заряженных тел. Урок физики в 8 классе Дискретное преобразование Фурье. (Лекция 11)
Дискретное преобразование Фурье. (Лекция 11) Движение тела в гравитационном поле.
Движение тела в гравитационном поле. Radio Mstiev Arsen
Radio Mstiev Arsen Источники энергии будущего
Источники энергии будущего Неуравновешенный термометр сопротивления
Неуравновешенный термометр сопротивления Колебательные состояния многоатомных молекул. Классическая теория
Колебательные состояния многоатомных молекул. Классическая теория Электродвижущая сила. Закон Ома для полной цепи
Электродвижущая сила. Закон Ома для полной цепи Презентация по физике "М.В. Ломоносов – первый российский академик" - скачать
Презентация по физике "М.В. Ломоносов – первый российский академик" - скачать  СИЛЫ ТРЕНИЯ
СИЛЫ ТРЕНИЯ Даими магнитларның магнит кыры. дайм Жирнең магнит кыры
Даими магнитларның магнит кыры. дайм Жирнең магнит кыры Турбинные масла
Турбинные масла Робота в електростатичному полі. Потенціал
Робота в електростатичному полі. Потенціал  Жизнь и творческий путь Альберта Эйнштейна
Жизнь и творческий путь Альберта Эйнштейна  Шкала электромагнитных излучений
Шкала электромагнитных излучений Измерительная техника и технология. Основы метрологии
Измерительная техника и технология. Основы метрологии