Содержание
- 2. Энтропия выступает, как мера беспорядочности, хаотичности состояния, мера необратимого рассеяния энергии Энтропия – функция, характеризующая меру
- 3. Второе начало термодинамики устанавливает существование энтропии как функции состояния термодинамической системы и вводит понятие абсолютной термодинамической
- 4. ВТОРОЕ НАЧАЛО ТЕРМОДИНАМИКИ Николя Леонар Сади Карно французский физик и математик (1796 – 1832) Исследование «Размышления
- 5. ВТОРОЕ НАЧАЛО ТЕРМОДИНАМИКИ Рудольф Юлиус Эмануэль Клаузиус немецкий физик, механик и математик (1822 – 1888) Вильгельм
- 6. ВТОРОЕ НАЧАЛО ТЕРМОДИНАМИКИ Николай Иович Белокоонь советский учёный (1899 – 1970) На основе анализа формулировок второго
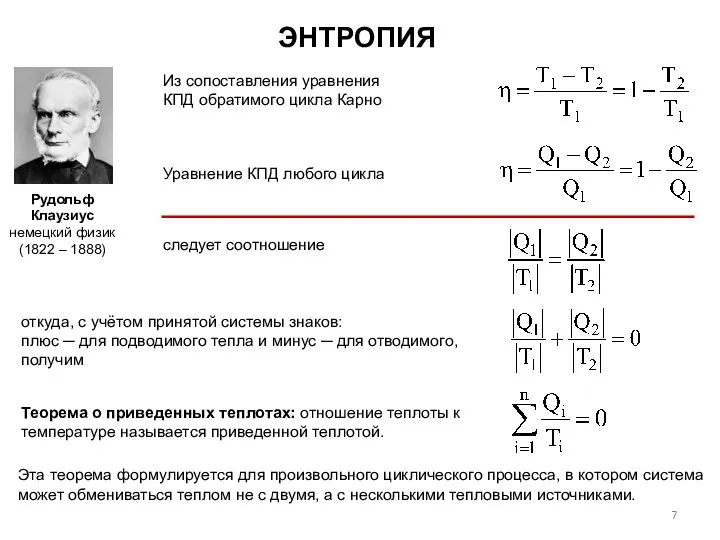
- 7. ЭНТРОПИЯ Рудольф Клаузиус немецкий физик (1822 – 1888) Уравнение КПД любого цикла следует соотношение Из сопоставления
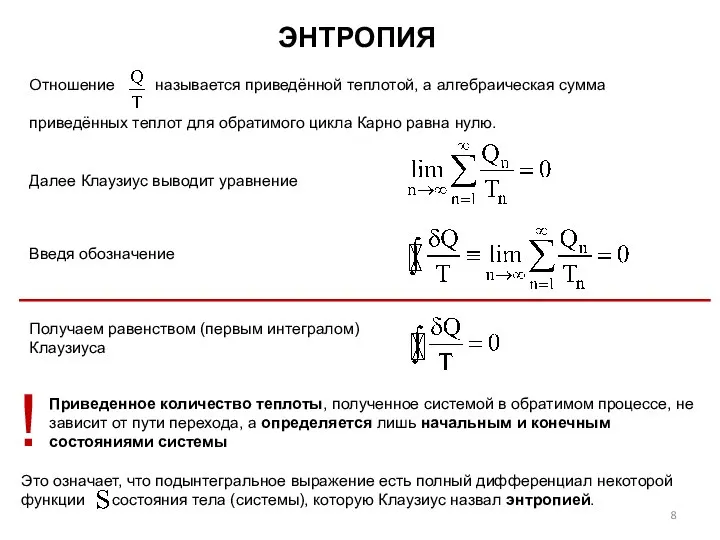
- 8. ЭНТРОПИЯ Отношение называется приведённой теплотой, а алгебраическая сумма приведённых теплот для обратимого цикла Карно равна нулю.
- 9. ЭНТРОПИЯ Энтропия S – это отношение полученной или отданной теплоты к температуре, при которой происходил этот
- 10. ЭНТРОПИЯ С физической точки зрения энтропия характеризует степень необратимости, неидеальности реального термодинамического процесса. Энтропия – мера
- 11. Запишем математическую формулировку первого начала термодинамики dQ – бесконечно малое количество тепла, сообщенное системе, dU –
- 12. Второе начало термодинамики является статистическим законом, оно применимо только к системам, состоящим из огромного числа молекул.
- 13. ВТОРОЕ НАЧАЛО ТЕРМОДИНАМИКИ Второе начало термодинамики k – постоянная Больцмана W - термодинамическая вероятность (или статистический
- 14. Внутренняя энергия U энтропия S давление р объем V температура Т ТЕРМОДИНАМИЧЕСКИЕ ПОТЕНЦИАЛЫ Эти параметры независимы
- 15. ТЕРМОДИНАМИЧЕСКИЕ ПОТЕНЦИАЛЫ
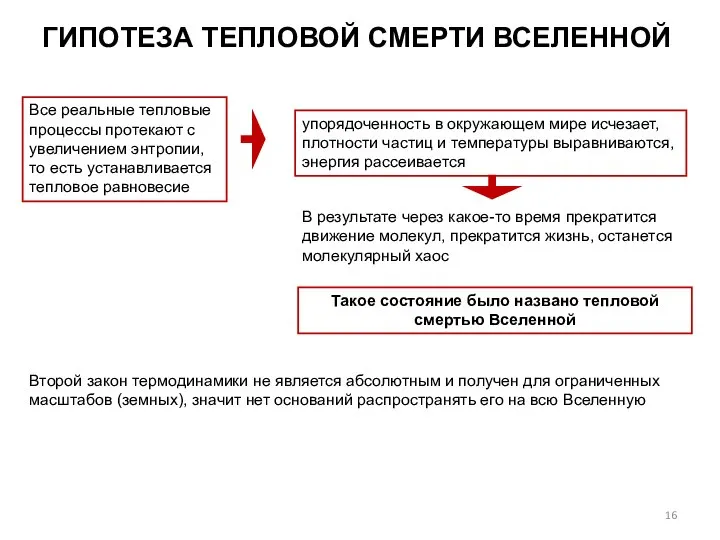
- 16. Все реальные тепловые процессы протекают с увеличением энтропии, то есть устанавливается тепловое равновесие упорядоченность в окружающем
- 17. ТРЕТЬЕ НАЧАЛО ТЕРМОДИНАМИКИ На основании обобщения экспериментальных исследований свойств веществ при сверхнизких температурах был установлен закон
- 18. ФАЗОВЫЕ ПРЕВРАЩЕНИЯ Фазовые превращения ‒ это переход вещества из одной фазы в другую, связанный с качественными
- 19. ФАЗОВЫЕ ПЕРЕХОДЫ ПЕРВОГО И ВТОРОГО РОДА Фазовый переход - переход вещества от одной фазы в другую,
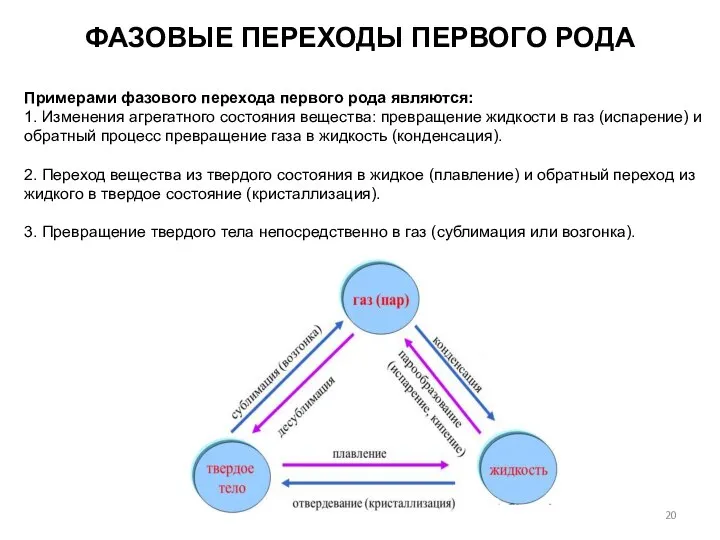
- 20. ФАЗОВЫЕ ПЕРЕХОДЫ ПЕРВОГО РОДА Примерами фазового перехода первого рода являются: 1. Изменения агрегатного состояния вещества: превращение
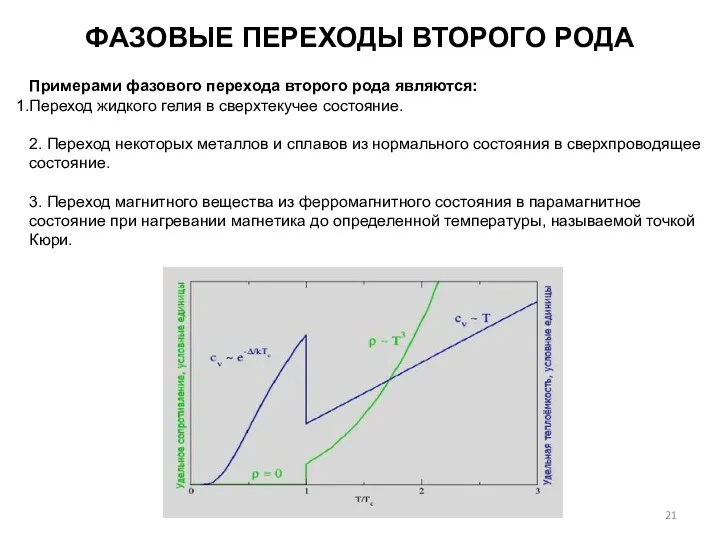
- 21. ФАЗОВЫЕ ПЕРЕХОДЫ ВТОРОГО РОДА Примерами фазового перехода второго рода являются: Переход жидкого гелия в сверхтекучее состояние.
- 22. Фазовый переход «твердое тело – жидкость» 1.Переход вещества из твердого состояния (фазы) в жидкое называется плавлением,
- 23. Фазовый переход «жидкость – газ» 1. Переход вещества из жидкости в газовую фазу называется испарением, а
- 24. Если система однокомпонентная, т.е. состоит из химически однородного вещества, то понятие фазы совпадает с понятием агрегатного
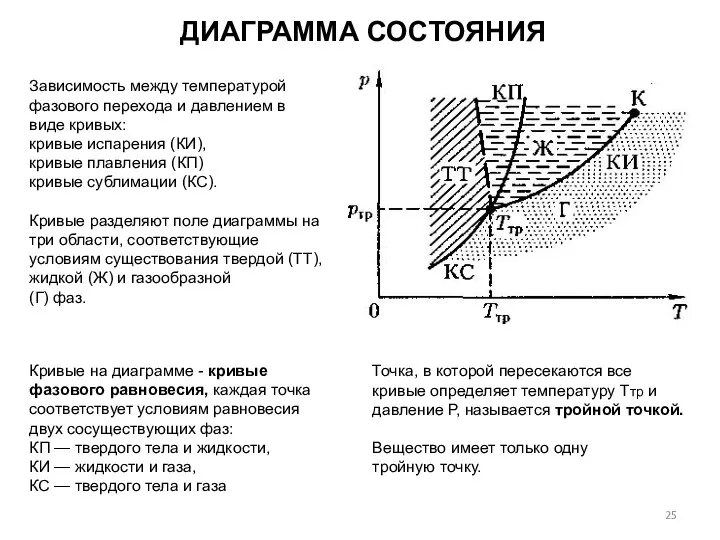
- 25. Зависимость между температурой фазового перехода и давлением в виде кривых: кривые испарения (КИ), кривые плавления (КП)
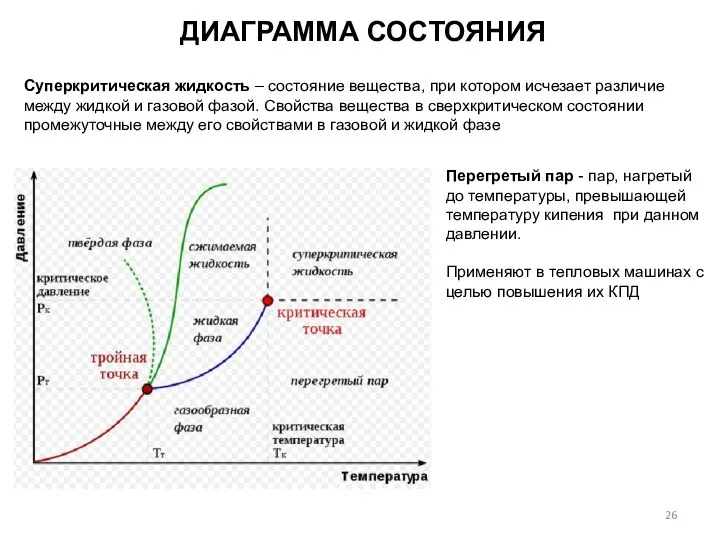
- 26. ДИАГРАММА СОСТОЯНИЯ Суперкритическая жидкость – состояние вещества, при котором исчезает различие между жидкой и газовой фазой.
- 27. Федеральное государственное автономное образовательное учреждение высшего образования «СИБИРСКИЙ ФЕДЕРАЛЬНЫЙ УНИВЕРСИТЕТ» Лекция 2.6 РЕАЛЬНЫЕ ГАЗЫ Е.В. Феськова,
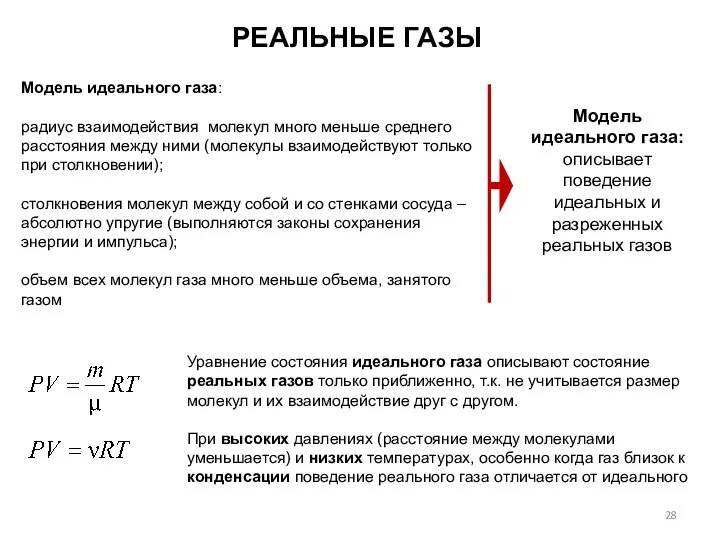
- 28. РЕАЛЬНЫЕ ГАЗЫ Модель идеального газа: радиус взаимодействия молекул много меньше среднего расстояния между ними (молекулы взаимодействуют
- 29. РЕАЛЬНЫЕ ГАЗЫ при малых плотностях и средних температурах РЕАЛЬНЫЙ ГАЗ при большой плотности и при низких
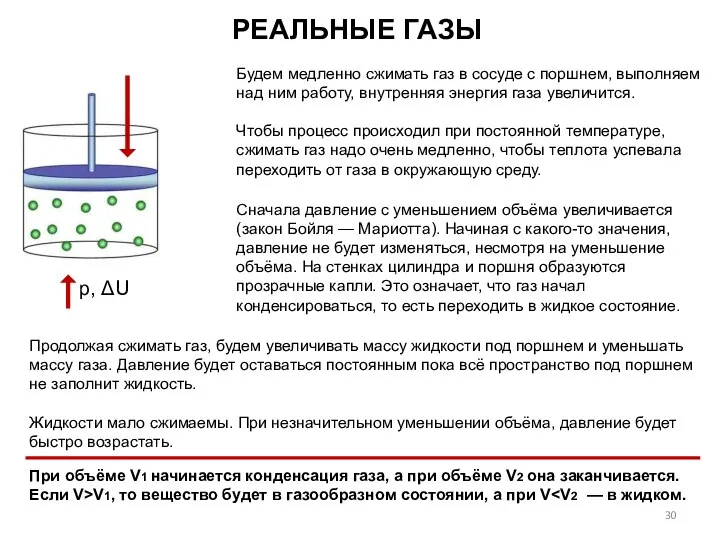
- 30. Будем медленно сжимать газ в сосуде с поршнем, выполняем над ним работу, внутренняя энергия газа увеличится.
- 31. Когда газ превращается в жидкость при изменении его объёма от V1 до V2 давление газа остаётся
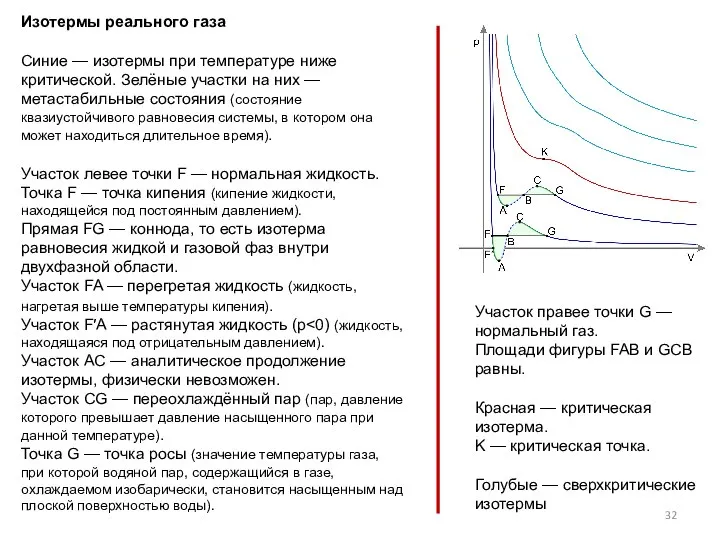
- 32. Изотермы реального газа Синие — изотермы при температуре ниже критической. Зелёные участки на них — метастабильные
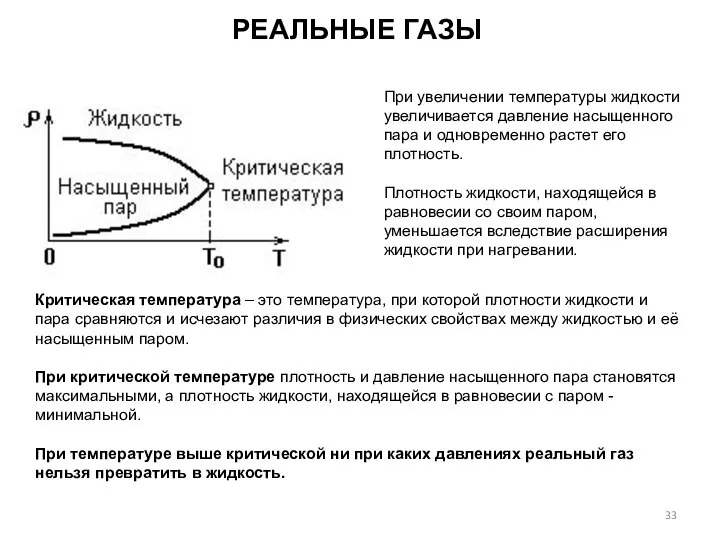
- 33. При увеличении температуры жидкости увеличивается давление насыщенного пара и одновременно растет его плотность. Плотность жидкости, находящейся
- 34. РЕАЛЬНЫЕ ГАЗЫ Основное отличие реального газа от идеального: идеальный газ нельзя перевести в жидкое состояние ни
- 35. РЕАЛЬНЫЕ ГАЗЫ Реальные газы – газы, свойства которых зависят от взаимодействия молекул Силы межмолекулярного взаимодействия. Они
- 36. РЕАЛЬНЫЕ ГАЗЫ Йоханнес Дидерик Ван-дер-Ваальс голландский физик (1837 – 1923) Газом Ван-дер-Ваальса называется модель реального газа,
- 37. УРАВНЕНИЕ ВАН-ДЕР-ВААЛЬСА Уравнение Ван-дер-Ваальса для 1 киломоля газа (уравнение состояния реальных газов) Уравнение учитывает конечные размеры
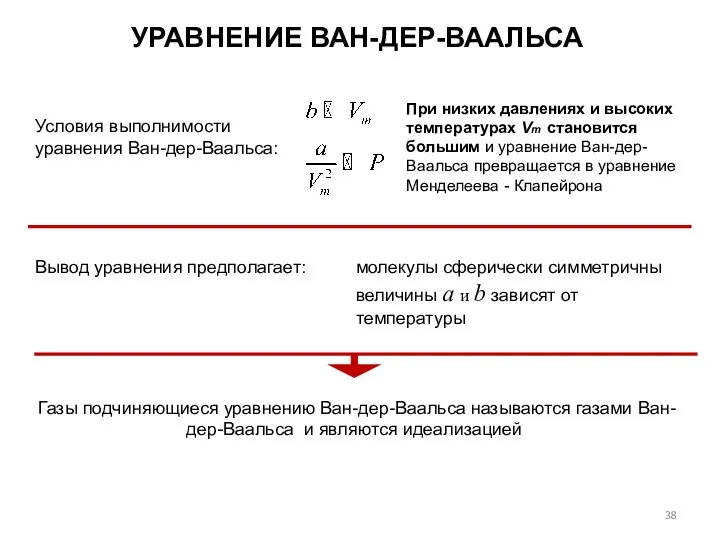
- 38. УРАВНЕНИЕ ВАН-ДЕР-ВААЛЬСА Условия выполнимости уравнения Ван-дер-Ваальса: Вывод уравнения предполагает: молекулы сферически симметричны величины а и b
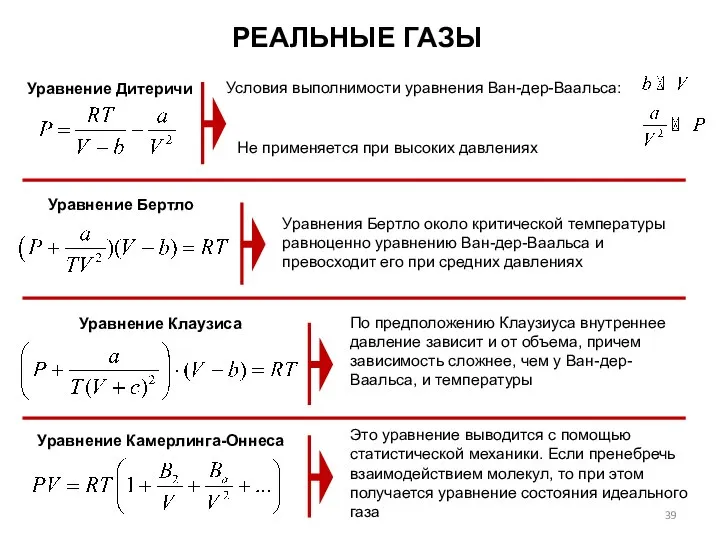
- 39. РЕАЛЬНЫЕ ГАЗЫ Уравнение Дитеричи Условия выполнимости уравнения Ван-дер-Ваальса: Уравнения Бертло около критической температуры равноценно уравнению Ван-дер-Ваальса
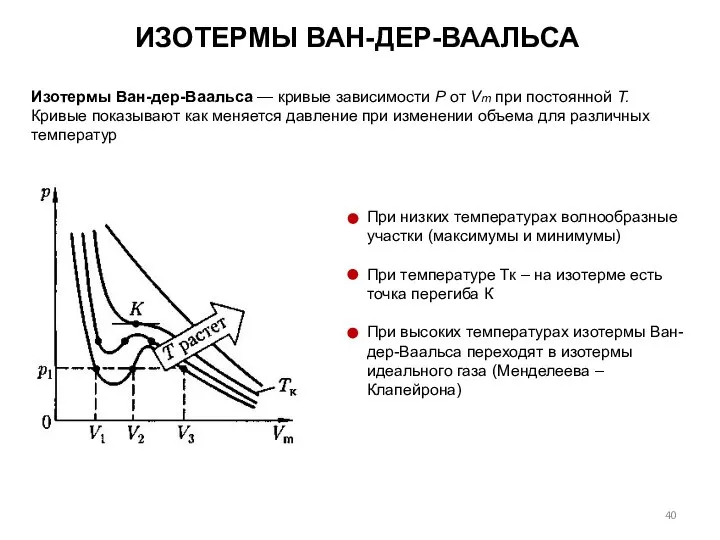
- 40. ИЗОТЕРМЫ ВАН-ДЕР-ВААЛЬСА Изотермы Ван-дер-Ваальса — кривые зависимости Р от Vm при постоянной Т. Кривые показывают как
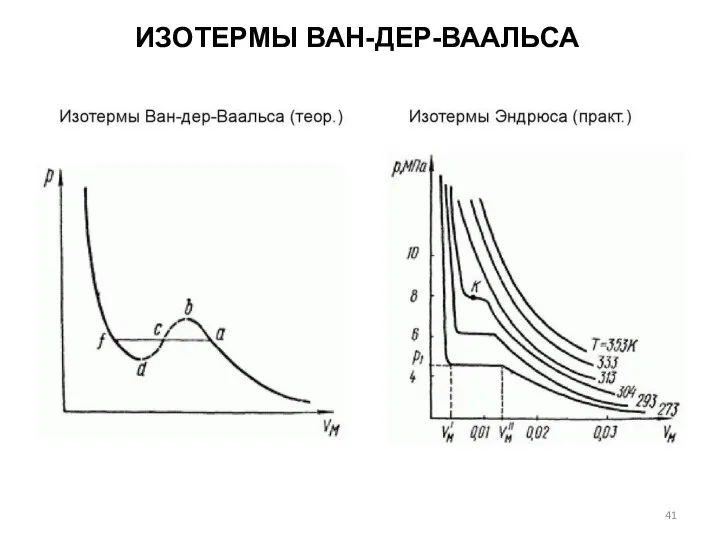
- 41. ИЗОТЕРМЫ ВАН-ДЕР-ВААЛЬСА
- 42. ИЗОТЕРМЫ ВАН-ДЕР-ВААЛЬСА В 1866 г. экспериментально исследовал зависимость молярного объема Vm углекислого газа от давления при
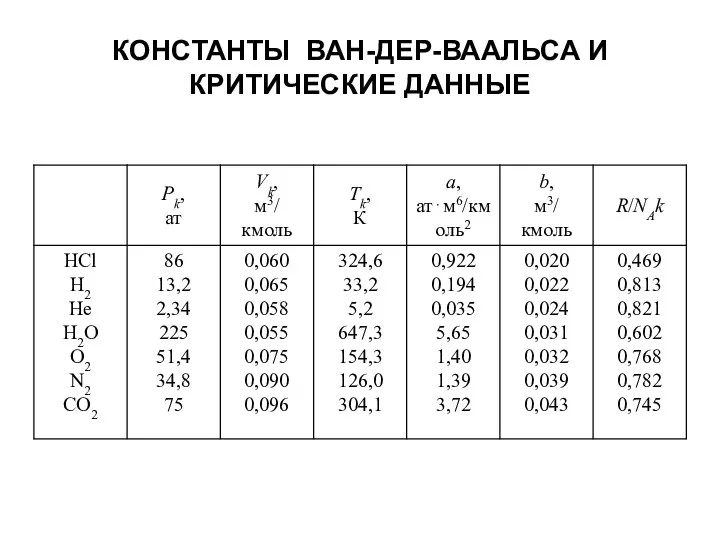
- 43. КОНСТАНТЫ ВАН-ДЕР-ВААЛЬСА И КРИТИЧЕСКИЕ ДАННЫЕ
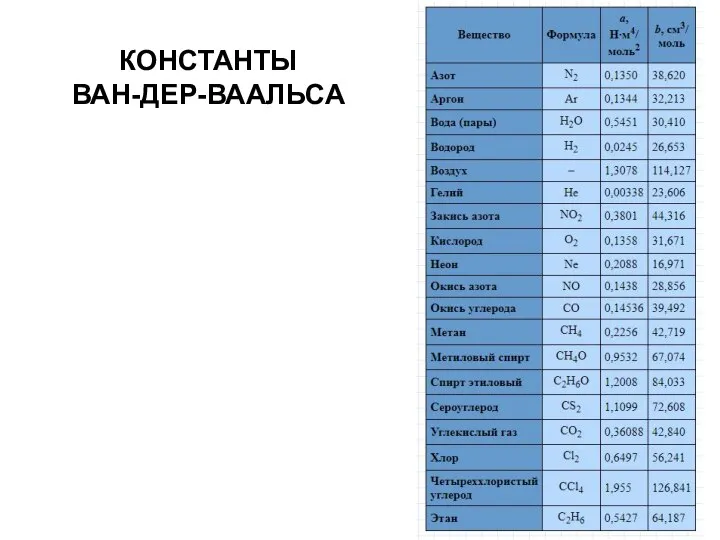
- 44. КОНСТАНТЫ ВАН-ДЕР-ВААЛЬСА
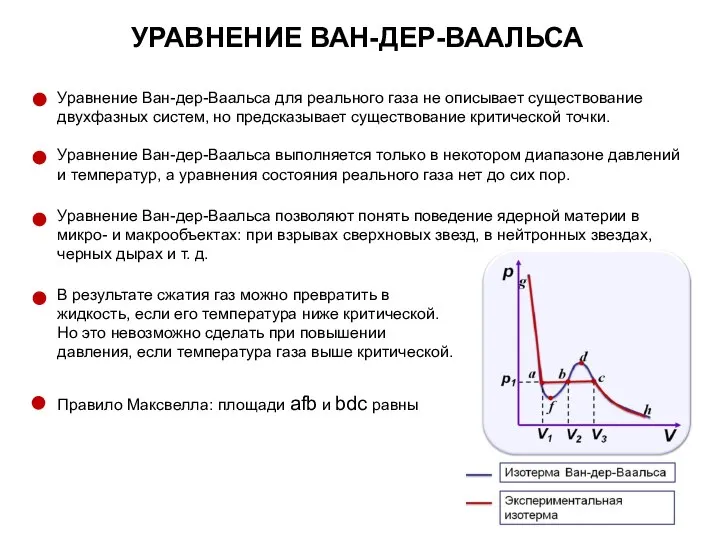
- 45. УРАВНЕНИЕ ВАН-ДЕР-ВААЛЬСА Уравнение Ван-дер-Ваальса для реального газа не описывает существование двухфазных систем, но предсказывает существование критической
- 46. Внутренняя энергия одного моля газа Ван-дер-Ваальса (реального газа) складывается из: кинетической энергии теплового движения молекул потенциальной
- 47. при адиабатном расширении без совершения внешней работы внутренняя энергия газа не изменяется Равенство справедливо как для
- 49. Скачать презентацию



























 Презентация-сопровождение урока физики в 7 классе «Физическая олимпиада» Учитель физики МОУ «Моргаушская СОШ» Моргаушского р
Презентация-сопровождение урока физики в 7 классе «Физическая олимпиада» Учитель физики МОУ «Моргаушская СОШ» Моргаушского р Виды теплопередачи. Конвекция. Излучение (8 класс)
Виды теплопередачи. Конвекция. Излучение (8 класс) Равновесие тел урок физики, 10 класс _
Равновесие тел урок физики, 10 класс _ Аттестационная работа. Программа элективного курса по физике «Мир удивительной оптики». (9 класс)
Аттестационная работа. Программа элективного курса по физике «Мир удивительной оптики». (9 класс) Сила трения
Сила трения Лекция 8. Общая физика. Элементы квантовой механики
Лекция 8. Общая физика. Элементы квантовой механики Учитель: Попова И.А. МОУ СОШ № 30 Белово 2010
Учитель: Попова И.А. МОУ СОШ № 30 Белово 2010  Использование информационных технологий в школьном лабораторном эксперименте: определение ускорения свободного падения
Использование информационных технологий в школьном лабораторном эксперименте: определение ускорения свободного падения Лазеры: строение, свойства, основные виды
Лазеры: строение, свойства, основные виды Радиационный контроль
Радиационный контроль Общая физика
Общая физика Электротехника и электроника. Классический метод анализа переходных процессов. (Лекция 10)
Электротехника и электроника. Классический метод анализа переходных процессов. (Лекция 10) История происхождения физических терминов (работа, масса, сила)
История происхождения физических терминов (работа, масса, сила) Естественно-научная картина мира. (Лекция 5)
Естественно-научная картина мира. (Лекция 5) Механическое движение тела
Механическое движение тела Шкала электромагнитных волн
Шкала электромагнитных волн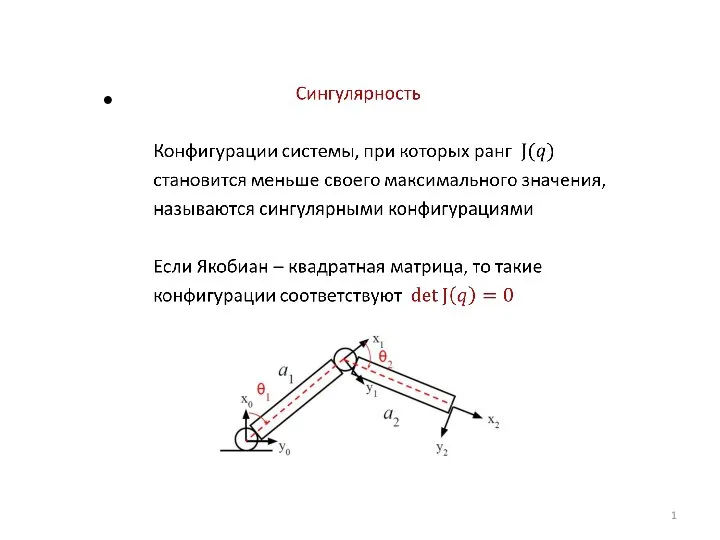 Сингулярность. Сингулярные конфигурации
Сингулярность. Сингулярные конфигурации Гидропривод и пневмопривод
Гидропривод и пневмопривод Показатели качества регулирования. Точность регулирования
Показатели качества регулирования. Точность регулирования Энтропия и вероятность
Энтропия и вероятность Исследование гидродинамических характеристик и процессов смешения потока теплоносителя в ТВС-квадрат реактора PWR
Исследование гидродинамических характеристик и процессов смешения потока теплоносителя в ТВС-квадрат реактора PWR Основы молекулярной физики и термодинамики
Основы молекулярной физики и термодинамики Електричний заряд. Електростатичне поле. Конденсатори
Електричний заряд. Електростатичне поле. Конденсатори Скалярное поле. Поверхности и линии уровня. Градиент скалярного поля. Лекция 30
Скалярное поле. Поверхности и линии уровня. Градиент скалярного поля. Лекция 30 Геоэлектрика (электроразведка, электрометрия)
Геоэлектрика (электроразведка, электрометрия) Види з’єднання провідників
Види з’єднання провідників Переходная функция. Импульсная характеристика. ТАУ 2
Переходная функция. Импульсная характеристика. ТАУ 2 Тесты. Изменение агрегатных состояний вещества
Тесты. Изменение агрегатных состояний вещества