Содержание
- 2. АЛКАНЫ И ЦИКЛОАЛКАНЫ АЛКАНЫ И ЦИКЛОАЛКАНЫ – углеводороды, в которых все атомы углерода соединены друг с
- 3. Названия алканов. Слово «алкан» того же происхождения, что и «алкоголь» (см. ниже). Устаревший термин «парафин» произошел
- 5. Строение и физические свойства алканов. В алканах четыре sp3-гибридные орбитали атома углерода (см. ОРБИТАЛИ) направлены к
- 8. Основные источники алканов – нефть и природный газ. Метан составляет основную массу природного газа, в нем
- 9. Алканы в составе бензина, керосина, солярового масла, мазута используются в качестве топлива. Высшие алканы входят в
- 12. Скачать презентацию
АЛКАНЫ И ЦИКЛОАЛКАНЫ
АЛКАНЫ И ЦИКЛОАЛКАНЫ – углеводороды, в которых все атомы углерода
АЛКАНЫ И ЦИКЛОАЛКАНЫ
АЛКАНЫ И ЦИКЛОАЛКАНЫ – углеводороды, в которых все атомы углерода
Названия алканов. Слово «алкан» того же происхождения, что и «алкоголь» (см. ниже).
Названия алканов. Слово «алкан» того же происхождения, что и «алкоголь» (см. ниже).
Названия алканов
Строение и физические свойства алканов. В алканах четыре sp3-гибридные орбитали атома углерода
Строение и физические свойства алканов. В алканах четыре sp3-гибридные орбитали атома углерода
Строение и физические свойства алканов
Температуры плавления и кипения алканов возрастают с увеличением числа атомов углерода в молекуле, при этом рост температуры постепенно замедляется, так, С100Н202 плавится при 115° С, С150Н302– при 123° С. Температуры плавления и кипения для первых 25 алканов приведены в таблице – видно, что начиная с октадекана, алканы – твердые вещества.
Основные источники алканов – нефть и природный газ. Метан составляет основную
Основные источники алканов – нефть и природный газ. Метан составляет основную
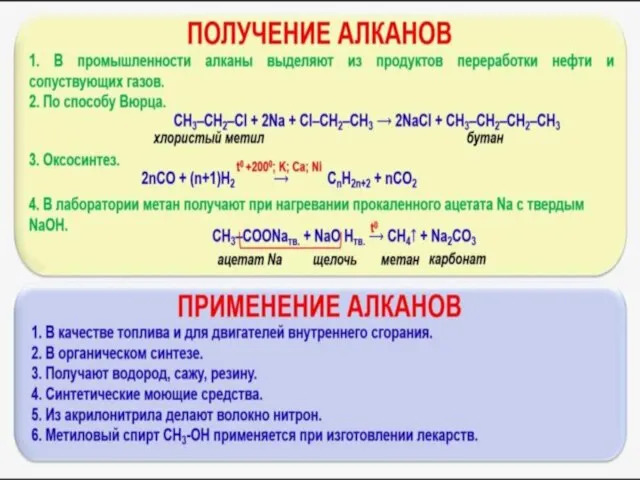
Нахождение в природе и получение
Алканы в составе бензина, керосина, солярового масла, мазута используются в качестве
Алканы в составе бензина, керосина, солярового масла, мазута используются в качестве
Применение алканов








 Тема: Липиды. Лекция № 2 для студентов 2 курса
Тема: Липиды. Лекция № 2 для студентов 2 курса Презентація на тему: Корозія. Шляхи захисту від неї.
Презентація на тему: Корозія. Шляхи захисту від неї.  Строение атома
Строение атома Презентация по Химии "Жири,вуглеводи,білки,втаміни як компоненти їжі" - скачать смотреть бесплатно
Презентация по Химии "Жири,вуглеводи,білки,втаміни як компоненти їжі" - скачать смотреть бесплатно Хімія у нашому житті вода
Хімія у нашому житті вода  Оксиды. Номенклатура, классификация, свойства
Оксиды. Номенклатура, классификация, свойства Кислотность органических соединений. Типы химических реакций
Кислотность органических соединений. Типы химических реакций Характеристики химического процесса. Степень превращения, селективность, выход продукта. (Лекция 1.2)
Характеристики химического процесса. Степень превращения, селективность, выход продукта. (Лекция 1.2) Гравиметрический метод анализа
Гравиметрический метод анализа Каталитическая активность ферментов Работу выполнили: Кичаева Нина Иванькова Елена Ученицы 10 класса МОУ Сергиевской СОШ №1 «О
Каталитическая активность ферментов Работу выполнили: Кичаева Нина Иванькова Елена Ученицы 10 класса МОУ Сергиевской СОШ №1 «О (+)-Plumisclerin A. Плюмисклин А
(+)-Plumisclerin A. Плюмисклин А История открытия бензола Впервые бензол описал немецкий химик Иоганн Глаубер. Он получил это соединение в 1649 г. в результате пе
История открытия бензола Впервые бензол описал немецкий химик Иоганн Глаубер. Он получил это соединение в 1649 г. в результате пе Хімічна небезпека: походження, джерела та дії при хімічних забрудненнях
Хімічна небезпека: походження, джерела та дії при хімічних забрудненнях  Обмен железа и его нарушения
Обмен железа и его нарушения Разбор 25 задания. Установим соответствие
Разбор 25 задания. Установим соответствие Соединения галогенов
Соединения галогенов Драгоценные камни Агат, амазонит, кварц, нефрит, оникс, яшма.
Драгоценные камни Агат, амазонит, кварц, нефрит, оникс, яшма. Исследование соединений со структурой слоистого перовскита
Исследование соединений со структурой слоистого перовскита Презентация по Химии "Презентация Ионы и ионная химическая связь" - скачать смотреть
Презентация по Химии "Презентация Ионы и ионная химическая связь" - скачать смотреть  Еріту. Сұйықтықтарды араластыру. Қатты заттарды және сұйықтықтарды бөліп алу
Еріту. Сұйықтықтарды араластыру. Қатты заттарды және сұйықтықтарды бөліп алу Актиний. Нахождение в природе
Актиний. Нахождение в природе Особенности познания в химии
Особенности познания в химии Аммиак
Аммиак Химическая викторина Пятый элемент
Химическая викторина Пятый элемент Химия и организм человека
Химия и организм человека Кремний и его соединения
Кремний и его соединения Структура гетероциклов, нуклеозидов и нуклеотидов
Структура гетероциклов, нуклеозидов и нуклеотидов Аттестационная работа. Образовательная программа элективного курса по химии Химия и мы
Аттестационная работа. Образовательная программа элективного курса по химии Химия и мы