Содержание
- 2. План лекции: Алканы: общая формула, состав, гомологический ряд. Номенклатура алканов. Строение молекулы метана. Физические свойства. Нахождение
- 3. Понятие алканы Алканы (парафины, алифатические соединения) – соединения углерода с водородом, в молекулах которых атомы углерода
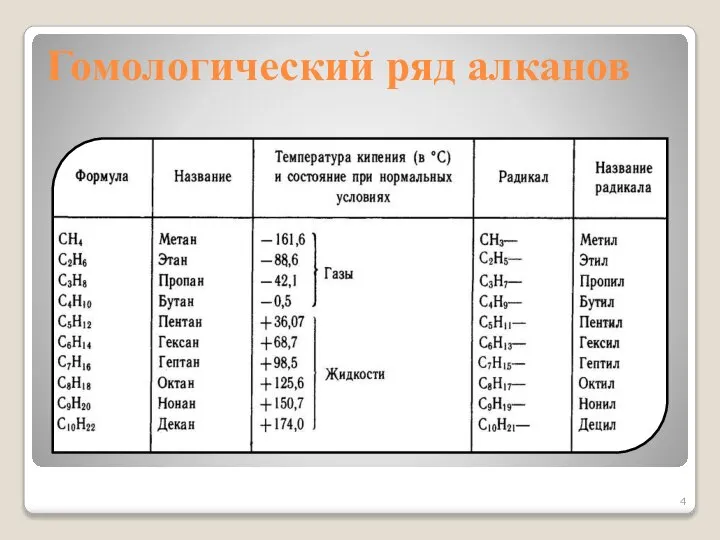
- 4. Гомологический ряд алканов
- 5. Номенклатура алканов Номенклатура IUPAC (ЮПАК) Выбрать цепь, пронумеровать атомы углерода в цепи с того конца, к
- 6. Если разветвлений два и они равноудалены от концов главной цепи, то нумеровать углеродную цепь необходимо с
- 7. Дать название радикалу – боковому разветвлению. Причем перед ним ставят номер того атома в углеродной цепи,
- 8. Если замещающих разветвлений несколько, то цифрой отмечают каждое из них, перечисляя радикалы в алфавитном порядке 5-пропил-3-этил
- 9. Если встречаются одинаковые радикалы, то сначала через запятые перечисляют цифрами местоположения разветвлений, затем их количество и
- 10. К названию последнего радикала добавляют название того алкана, который содержит такое же количество атомов углерода, как
- 11. Дайте название соединению 3-метил-4-этилгексан
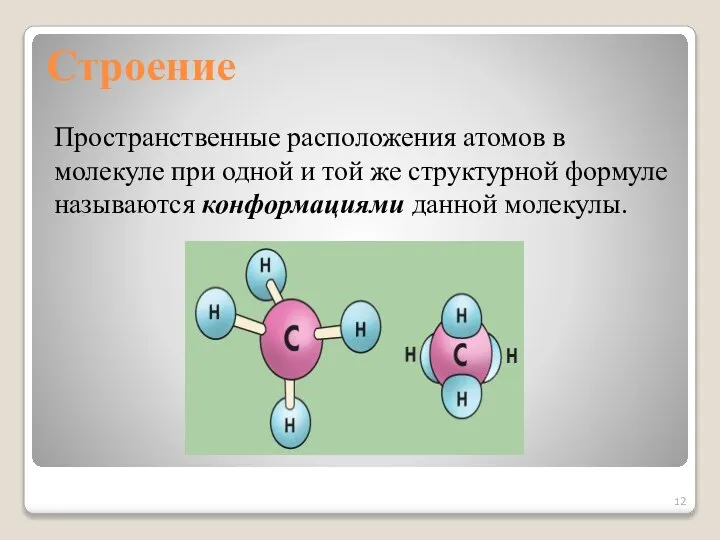
- 12. Строение Пространственные расположения атомов в молекуле при одной и той же структурной формуле называются конформациями данной
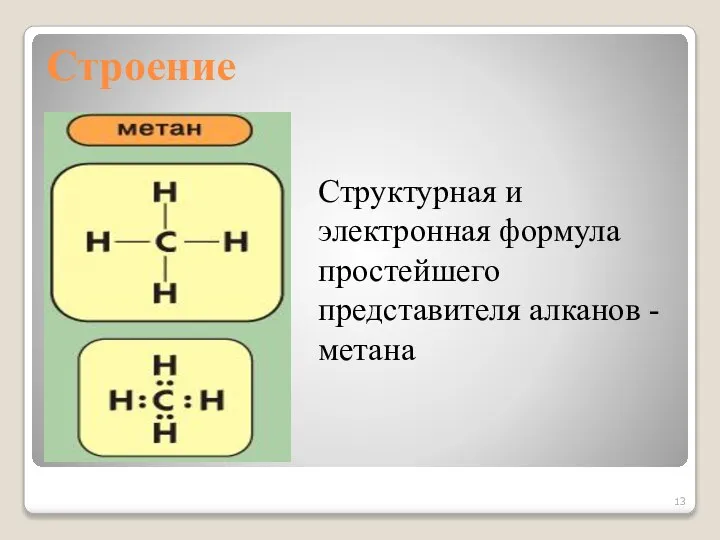
- 13. Строение Структурная и электронная формула простейшего представителя алканов - метана
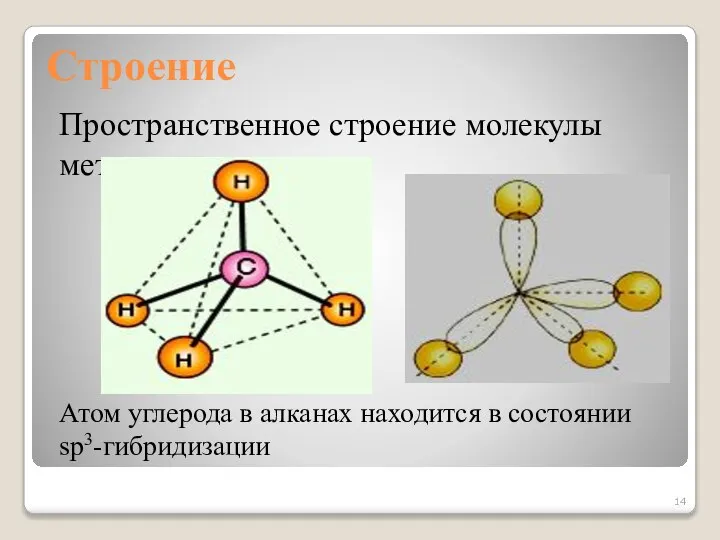
- 14. Строение Пространственное строение молекулы метана Атом углерода в алканах находится в состоянии sp3-гибридизации
- 15. Изомерия алканов Для алканов характерна изомерия углеродного скелета
- 16. Физические свойства
- 17. Нахождение в природе Атмосфера планет Солнечной системы
- 18. Метан на спутнике Сатурна - Титане
- 19. Метан в кометах и метеоритах
- 20. В природе метан образуется в результате разложения растительных и животных объектов без доступа кислорода
- 21. Алканы в составе нефти
- 22. Высшие алканы в кутикулах растений защищают от высыхания
- 23. Алканы встречаются в качестве феромонов у мухи цеце
- 24. Некоторые орхидеи при помощи алканов-феромонов привлекают опылителей
- 25. Получение Установка для получения биогаза в Австралии
- 26. Лабораторные способы получения 1. При сплавлении солей карбоновых кислот с щелочами: СН3-СН2-C + NaOH → СH3-СН3
- 27. 2. Получение метана при гидролизе карбита алюминия: Al4C3 + 12H2O = 4Al(OH)3 + 3CH4
- 28. 3. Реакцией Вюрца из галогенпроизводных углеводородов (1855 г.): 2 СН3Br + 2Na → 2NaBr + СН3-
- 29. 4. Гидрирование ненасыщенных и циклических углеводородов с никелевым катализатором: CH2=CH2 + H2 → CH3-CH3
- 30. Химические свойства 1. Реакции замещения А) Галогенирование Реакция хлорирования протекает по цепному радикальному механизму. Теорию цепных
- 31. Б) Нитрование При действии разбавленной (10%) азотной кислоты на алканы под давлением при температуре 140o C
- 32. 2. Горение Все предельные углеводороды горят с образованием углекислого газа и воды. Эта экзотермическая реакция имеет
- 33. Горение метана
- 34. 3. При температурах 1400-1500 o С происходит дегидрирование метана и образуются этилен и ацетилен 2CH4 →
- 35. 4. Пиролиз Разложение под высокими температурами CH4 → С + 2H2 – при 1000 °C
- 36. 5. Конверсия алканлов Взаимодействие алканов с парами воды. При высокой температуре (1000), в присутствии никелевого катализатора
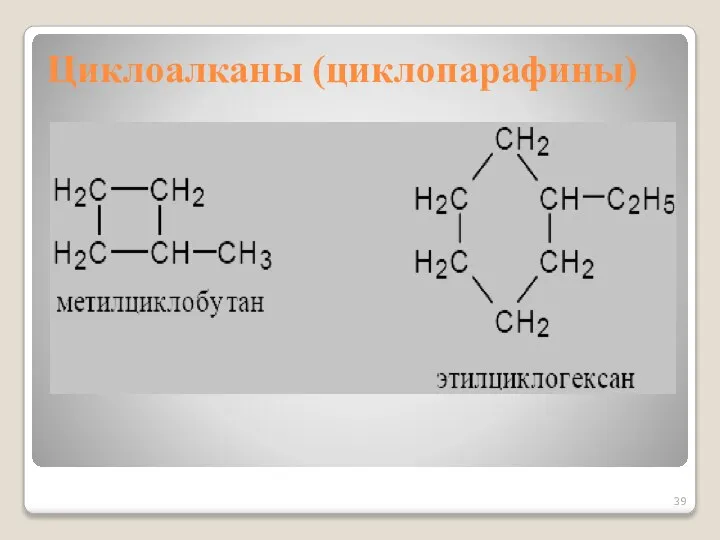
- 37. Циклоалканы (циклопарафины)
- 38. Циклоалканы − углеводороды циклического строения. Общая формула CnH2n Циклизация начинается с C3, названия образуются от Cn
- 39. Циклоалканы (циклопарафины)
- 40. Химические свойства У циклопропана и циклобутана отчетливо выражена способность вступать в реакции присоединения с разрывом цикла:
- 41. Для циклогексана реакции присоединения не характерны, а, как и для алканов, наблюдаются реакции замещения:
- 42. Применение 1. В виде топлива
- 43. 2. Получение алкенов, ароматические УВ
- 44. 3. Сажу - важный наполнитель для резины, синтетические моющие средства. 4. Жидкие алканы - как растворители.
- 45. Применение в медицине 1. Циклопропан Бесцветный газ со сладковатым запахом. Используется в хирургии в качестве средства
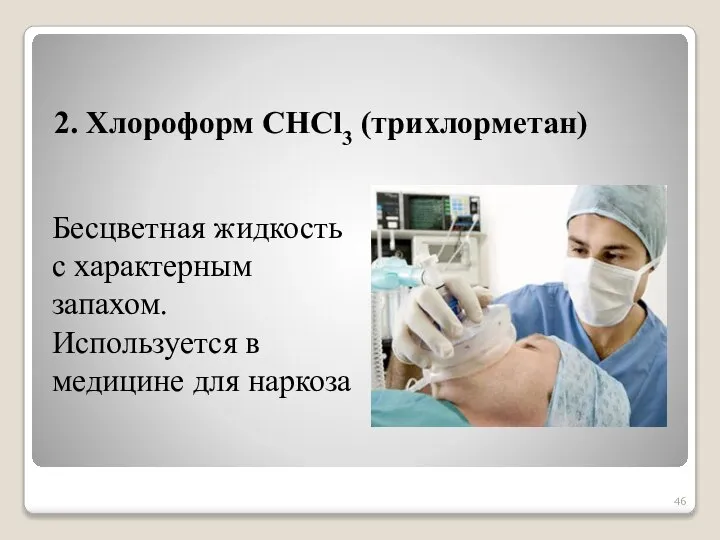
- 46. 2. Хлороформ СНСl3 (трихлорметан) Бесцветная жидкость с характерным запахом. Используется в медицине для наркоза
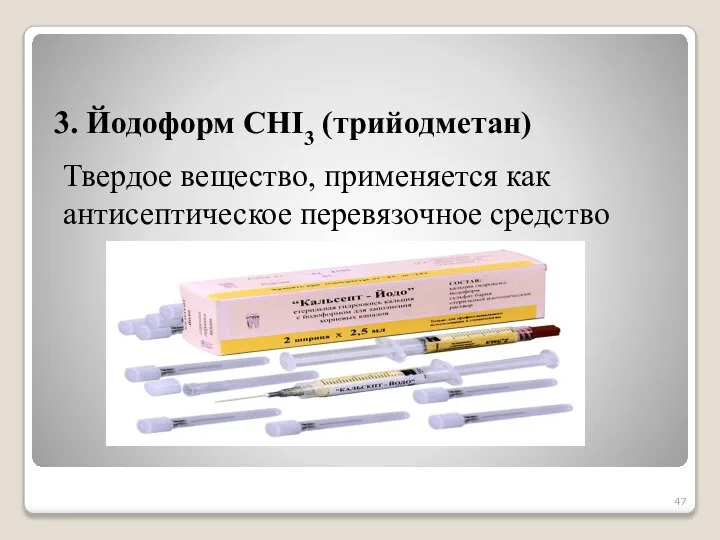
- 47. 3. Йодоформ СНI3 (трийодметан) Твердое вещество, применяется как антисептическое перевязочное средство
- 48. 4. Перфторалканы (УВ, в которых все атомы водорода замещены на атомы фтора) Эффективные газопереносящие среды, что
- 49. Закрепление Общая формула алканов имеет вид: а) СnH2n-6 б) CnH2n-2 в) CnH2n г) CnH2n+2
- 50. Валентность атомов углерода в алканах равна: а) 2 б) 4 в) 6 г) 1
- 51. Углеводород 2,4-диметилгептан является изомером: а) н-гептана б) 2,3- диметилпентана в) 2,3,4-триметилпентана г) 3- этилгептана
- 52. Укажите пару соединений, которая относится к алканам: а) С4Н10 и С5Н10 б) С3Н8 и С5Н12 в)
- 53. Литература Основная литература: Габриелян, О. С. Химия. 10 класс. Базовый уровень : учебник / О. С.
- 55. Скачать презентацию













































 Миметик глицина на основе производного Гераниола
Миметик глицина на основе производного Гераниола Цеолиты. Свойства и область применения
Цеолиты. Свойства и область применения Химические процессы
Химические процессы Бор (Borum)
Бор (Borum) Химия и стирка
Химия и стирка  Презентация по Химии "Электролиз расплавов и растворов" - скачать смотреть
Презентация по Химии "Электролиз расплавов и растворов" - скачать смотреть  Аттестационная работа. Использование цифровой лаборатории Архимед во внеурочной деятельности по химии
Аттестационная работа. Использование цифровой лаборатории Архимед во внеурочной деятельности по химии д.з.051
д.з.051 Химические и физико-химические методы стандартизации и контроля качества лекарственных. (Лекция 3)
Химические и физико-химические методы стандартизации и контроля качества лекарственных. (Лекция 3) Азотная кислота
Азотная кислота Окислительно-восстановительные реакции. (Лекция 18)
Окислительно-восстановительные реакции. (Лекция 18) Переваривание углеводов в пищеварительном тракте. Гликолиз. Окислительное декарбоксилирование пирувата. (Тема 6)
Переваривание углеводов в пищеварительном тракте. Гликолиз. Окислительное декарбоксилирование пирувата. (Тема 6) Майда еритін витаминдер. А,D,E,K витаминдері
Майда еритін витаминдер. А,D,E,K витаминдері Использование уксусной кислоты в жизни
Использование уксусной кислоты в жизни Ауылшаруашылық дақылдарының тұқымдарын фунгецидтермен улау және химиялық қорғау тәсілдерінің биологиялық
Ауылшаруашылық дақылдарының тұқымдарын фунгецидтермен улау және химиялық қорғау тәсілдерінің биологиялық Презентация Соли
Презентация Соли Lekcii_ - 2017-lech_ped 11
Lekcii_ - 2017-lech_ped 11 V група періодичної системи Менделєєва
V група періодичної системи Менделєєва Химико-технологические процессы современных производств
Химико-технологические процессы современных производств Органическая химия. Химические свойства и типы реакций. (9 класс)
Органическая химия. Химические свойства и типы реакций. (9 класс) Химия. Вопросы. Практическая работа
Химия. Вопросы. Практическая работа Химическая идентификация
Химическая идентификация Почему протекают химические реакции
Почему протекают химические реакции Презентация по Химии "Солі в природі" - скачать смотреть бесплатно
Презентация по Химии "Солі в природі" - скачать смотреть бесплатно Пегматитовые месторождения
Пегматитовые месторождения Ароматичні вуглеводні Арени Підготував Учень 11-А класу Пазуханич Руслан
Ароматичні вуглеводні Арени Підготував Учень 11-А класу Пазуханич Руслан 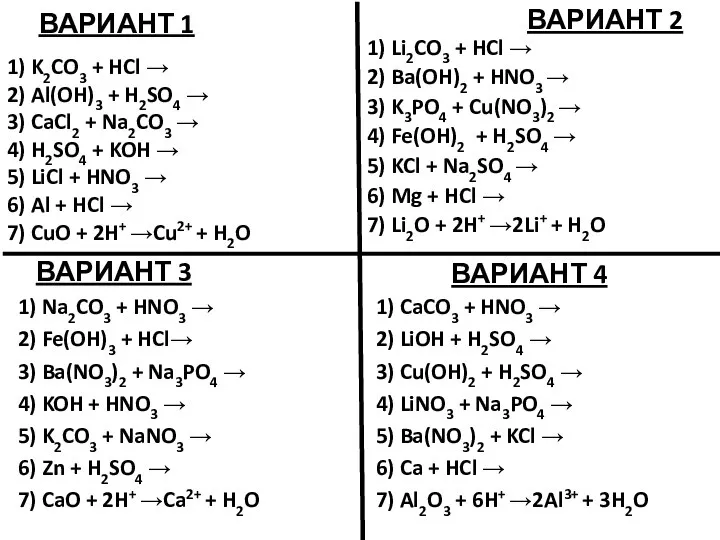 Уравнения возможных реакций. Задание
Уравнения возможных реакций. Задание Методы измерения и приборное обеспечение радиационно-экологического мониторинга. (Лекция 6)
Методы измерения и приборное обеспечение радиационно-экологического мониторинга. (Лекция 6)