Содержание
- 2. Понятие алкинов. Формула алкинов. Алкины – это углеводороды, в молекулах которых два атома углерода находятся в
- 3. Гомологический ряд алкинов. По международной номенклатуре ИЮПАК названия алкинов производятся от названий соответствующих предельных углеводородов путем
- 4. Модель ацетилена.
- 5. Изомерия алкинов. Для алкинов характерна структурная изомерия. Первые два члена гомологического ряда – этин и пропин
- 6. Получение алкинов. 1. Крекинг метана и его гомологов Ацетилен получают в промышленности путем высокотемпературного крекинга метана:
- 7. Физические свойства алкинов. Физические свойства алкинов похожи на свойства алканов и алкенов. Температуры кипения и плавления
- 8. C2H2, C3H4, C4H6 газы C5H8…C15H28 жидкости C16H30… твёрдые вещества
- 9. Из алкинов особое значение имеет ацетилен. Ацетилен из-за достигаемой высокой температуры пламени широко используется для резки
- 11. Скачать презентацию
Понятие алкинов. Формула алкинов.
Алкины – это углеводороды, в молекулах которых
Понятие алкинов. Формула алкинов.
Алкины – это углеводороды, в молекулах которых
Алкины (ацетиленовые углеводороды) – непредельные алифатические (ациклические) углеводороды, молекулы которых содержат одну тройную связь.
Ацетиленовыми углеводородами (алкинами) называются непредельные (ненасыщенные) углеводороды, содержащие в молекуле одну тройную связь и имеющие общую формулу:
СnH2n-2
Первый представитель этого класса – ацетилен НС≡СН, в связи с этим алкины называют ацетиленовыми углеводородами.
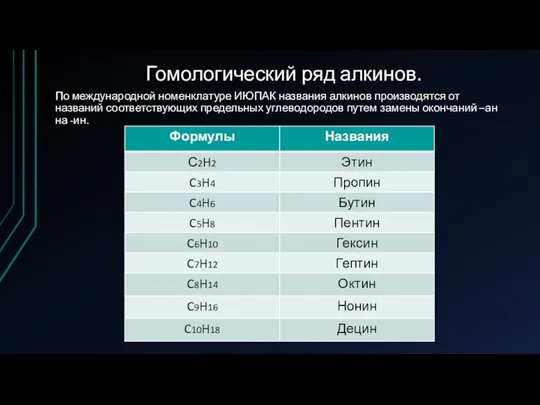
Гомологический ряд алкинов.
По международной номенклатуре ИЮПАК названия алкинов производятся от названий
Гомологический ряд алкинов.
По международной номенклатуре ИЮПАК названия алкинов производятся от названий
Модель ацетилена.
Модель ацетилена.
Изомерия алкинов.
Для алкинов характерна структурная изомерия. Первые два члена гомологического ряда
Изомерия алкинов.
Для алкинов характерна структурная изомерия. Первые два члена гомологического ряда
1. Изомерия углеродного скелета (начиная с С5Н8):
2. Изомерия положения тройной связи (начиная с С4Н6):
3. Межклассовая изомерия с алкадиенами и циклоалкенами, начиная с С4Н6:
Пространственная изомерия относительно тройной связи в алкинах не проявляется, т.к. заместители могут располагаться только одним способом — вдоль линии связи.
Получение алкинов.
1. Крекинг метана и его гомологов
Ацетилен получают в промышленности путем
Получение алкинов.
1. Крекинг метана и его гомологов
Ацетилен получают в промышленности путем
или его ближайших гомологов – этана и пропана, в этом случае ацетилен образуется при более низких температурах:
Сырьем в этих способах служит природный газ или нефть.
2. Гидролиз карбида кальция
В лаборатории ацетилен получают гидролизом карбида кальция (взаимодействие с водой).
Карбид кальция образуется при нагревании смеси оксида кальция СаО (негашеная известь, жженая известь, едкая известь) и кокса до 2500°С:
Вследствие большой энергоемкости этот метод экономически менее выгоден.
Физические свойства алкинов.
Физические свойства алкинов похожи на свойства алканов и алкенов.
Температуры
Физические свойства алкинов.
Физические свойства алкинов похожи на свойства алканов и алкенов.
Температуры
При обычных условиях алкины С2Н2-С4Н6– газы, С5Н8-С15Н28 – жидкости, с С16Н30 – твердые вещества. Алкины имеют специфический запах.
Наличие тройной связи в цепи приводит к повышению температуры кипения, плотности и растворимости их в воде по сравнению с олефинами и парафинами. Они хорошо растворяются в органических неполярных растворителях.
Ацетилен (С2Н2) – бесцветный газ, в чистом виде почти без запаха, технический ацетилен обладает неприятным запахом, легче воздуха, мало растворим в воде. Ацетилен взрывоопасен!
C2H2, C3H4, C4H6
газы
C5H8…C15H28
жидкости
C16H30…
твёрдые вещества
C2H2, C3H4, C4H6
газы
C5H8…C15H28
жидкости
C16H30…
твёрдые вещества
Из алкинов особое значение имеет ацетилен.
Ацетилен из-за достигаемой высокой температуры пламени
Из алкинов особое значение имеет ацетилен.
Ацетилен из-за достигаемой высокой температуры пламени
При его горении в кислороде пламя его достигает температуры 28000С.
Простота получения, относительно низкая стоимость, имическая активность сделали ацетилен важнейшим сырьем для многочисленных промышленных синтезов:
Хлорированием ацетилена получают дихлорэтилен и трихлорэтилен, применяемые в качестве растворителей. А также получают тетрахлорэтан, который применяется как растворитель (жиров, смол, каучука и др.), для получения фреонов, как экстрагент, в медицине.
Димеризацией ацетилена с последующим гидрохлорированием получают хлоропрен – мономер для хлоропренового каучука.
Гидрохлорированием ацетилена получают винилхлорид – мономер для получения поливинилхлорида (основа линолеума, разнообразной упаковки, труб и др.).
Гидратацией ацетилена получают уксусный альдегид, идущий на получение уксусной кислоты. Присоединением циановодорода к ацетилену получают акрилонитрил – мономер для получения синтетического волокна «нитрон».
Присоединением к ацетилену уксусной кислоты получают винилацетат – мономер для получения поливинилацетата (ПВА).
Поливиилацетат – основа для клеев, водоэмульсионных и акриловых красок, используется в производстве лаков.
Использование алкинов.







 Обзор основных методов исследования супрамолекулярных объектов
Обзор основных методов исследования супрамолекулярных объектов Презентация по Химии "Многоатомные спирты" - скачать смотреть
Презентация по Химии "Многоатомные спирты" - скачать смотреть  Родючість ґрунтів , можливості її регулювання. Учень 9-Г класу Юрчак Владислав Керівник Садовська Т.Я.
Родючість ґрунтів , можливості її регулювання. Учень 9-Г класу Юрчак Владислав Керівник Садовська Т.Я. Симметрия в химии. Кристаллы
Симметрия в химии. Кристаллы Количественное определение лекарственных средств
Количественное определение лекарственных средств Электронные конфигурации атомов
Электронные конфигурации атомов Презентація З хімії На тему : ” Майбутнє альтернативного палива” Виконала учениця 11-А класу Твердохліб Анжеліка
Презентація З хімії На тему : ” Майбутнє альтернативного палива” Виконала учениця 11-А класу Твердохліб Анжеліка  Кислоты органические и неорганические.
Кислоты органические и неорганические. Синтетические моющие средства.(СМС) Подготовила Живулько Елена.
Синтетические моющие средства.(СМС) Подготовила Живулько Елена.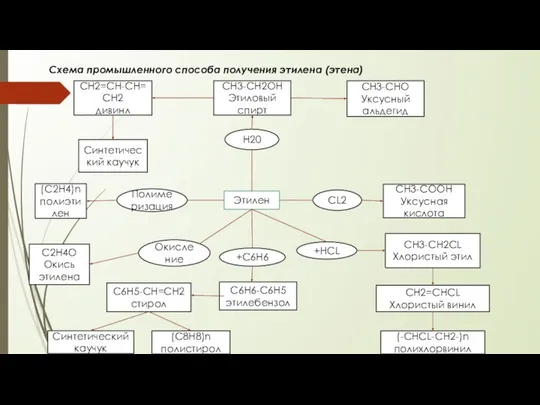 Промышленній способ получения этилена (этена)
Промышленній способ получения этилена (этена) Сложные эфиры
Сложные эфиры Растворы. Способы выражения концентрации растворенного вещества
Растворы. Способы выражения концентрации растворенного вещества Титани органічної хімії
Титани органічної хімії Энергетика химических процессов
Энергетика химических процессов Презентация по химии Химические уравнения Реакции обмена
Презентация по химии Химические уравнения Реакции обмена  Выращивание кристаллов в домашних условиях
Выращивание кристаллов в домашних условиях Неметаллы. Обобщение. Открытый урок
Неметаллы. Обобщение. Открытый урок Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Биогеохимия Оренбургской области
Биогеохимия Оренбургской области Химия элементов VIA группы. Сера
Химия элементов VIA группы. Сера Кремнийорганическая гипотеза
Кремнийорганическая гипотеза Неметаллы. Положение неметаллов в ПСХЭ
Неметаллы. Положение неметаллов в ПСХЭ Полифункциональды (гетерофункциональды) биоорганикалық қосылыстар: оксиқышқылдар, альдегидо- және кетоқышқылдар
Полифункциональды (гетерофункциональды) биоорганикалық қосылыстар: оксиқышқылдар, альдегидо- және кетоқышқылдар - Это оружие массового поражения, действие которого основано на токсических свойствах химических веществ. - Это оружие массового
- Это оружие массового поражения, действие которого основано на токсических свойствах химических веществ. - Это оружие массового  Задачи по теме Энергетический обмен
Задачи по теме Энергетический обмен Горение паро-газо-воздушного облака
Горение паро-газо-воздушного облака Ковалентная полярная связь
Ковалентная полярная связь Нітратна кислота. Нітрати Підготувала:Рибальчук Вікторія
Нітратна кислота. Нітрати Підготувала:Рибальчук Вікторія