Содержание
- 2. Цель: более полно познакомить учащихся с примерами металлов, образующих амфотерные соединения; раскрыть причины амфотерности по расположению
- 3. Алюминий – самый распространенный в природе элемент, по содержанию в земной коре (8%) находится на третьем
- 4. Он входит в состав глин, полевых шпатов, слюд. Важнейший минерал алюминия – боксит содержит 28-60% глинозёма
- 5. Корунд Al2O3
- 6. Прозрачные кристаллы корунда, окрашенные примесями в синий цвет, называют сапфиром, в красный – рубином. Рубин Сапфир
- 7. Получение алюминия Впервые получен восстановлением хлорида алюминия металлическим калием или натрием без доступа воздуха: AlCl3 +
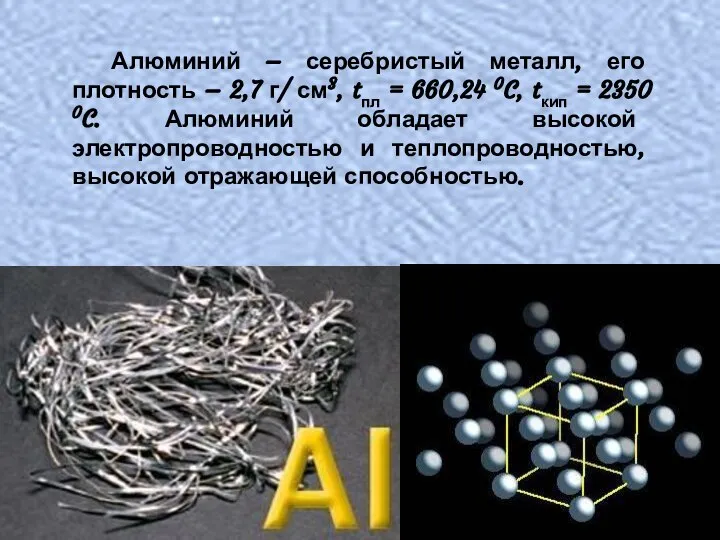
- 8. Алюминий – серебристый металл, его плотность – 2,7 г/ см3, tпл = 660,24 0C, tкип =
- 9. химические свойства Алюминий - химически активен. Легко окисляется кислородом воздуха, при этом покрывается пленкой оксида, предохраняющей
- 10. Без оксидной пленки алюминий активно взаимодействует с неметаллами. При обычной температуре реагирует с хлором и бромом,
- 11. Металлический алюминий является сильным восстановителем и восстанавливает другие металлы из их оксидов: Fe2O3 + 2Al =
- 12. Алюминий растворяется в соляной и серной кислотах, а также в водных растворах щелочей. 2Al + 6HCl
- 13. соединения алюминия Al2O3 + 6HCl = 2AlCl3 + 3H2O Al2O3 + NaOH = NaAlO2 + H2O
- 14. При добавлении избыточного количества щелочи осадок растворяется: Al(ОН)3 + NaOH = NaAlO2 + 2H2O Гидроксид алюминия
- 15. Применение алюминия Al
- 16. Применение алюминия и его соединений В чистом виде алюминий находит применение из-за своей мягкости: из него
- 17. Сплавы алюминия используют в строительстве, т. к. из них легко изготовить различные профили балок и разные
- 18. Производство алюминиевых труб.
- 19. Гель из гидроксида алюминия входит в состав лекарств для лечения болезней желудка. Гидроксид алюминия используется для
- 21. Скачать презентацию

















 Петрография
Петрография Аморфные тела
Аморфные тела Химия S - элементов
Химия S - элементов Основания. Гидроксид лития
Основания. Гидроксид лития Тіршілік гетерофункционалды қосылыстар
Тіршілік гетерофункционалды қосылыстар Элементарный состав живых организмов
Элементарный состав живых организмов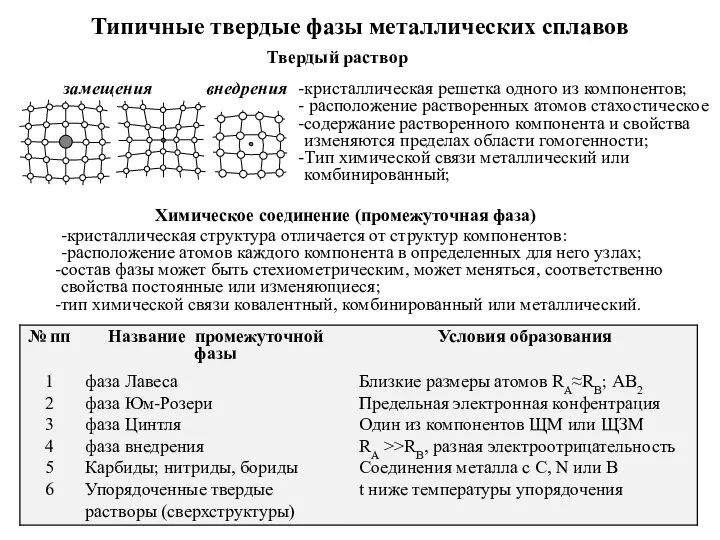 Типичные твердые фазы металлических сплавов
Типичные твердые фазы металлических сплавов Разработка реактора для отопления домов путем извлечения водорода из воды
Разработка реактора для отопления домов путем извлечения водорода из воды Классификация лекарственных растений (ЛР) и лекарственного растительного сырья (ЛРС)
Классификация лекарственных растений (ЛР) и лекарственного растительного сырья (ЛРС) Теоретическое и прикладное материаловедение
Теоретическое и прикладное материаловедение Классификация органических веществ
Классификация органических веществ Сероводород. Сернистый водород, сульфид водорода, дигидросульфид
Сероводород. Сернистый водород, сульфид водорода, дигидросульфид Пептиды. Тема 3
Пептиды. Тема 3 Элементы V группы Периодической системы химических элементов Д.И.Менделеева Работу выполнила учитель химии МОУ Северн
Элементы V группы Периодической системы химических элементов Д.И.Менделеева Работу выполнила учитель химии МОУ Северн Природный газ и нефть
Природный газ и нефть Физические свойства металлов. (9 класс)
Физические свойства металлов. (9 класс) Эмпирические правила
Эмпирические правила Химия вокруг нас
Химия вокруг нас Физические и химические свойства кислот
Физические и химические свойства кислот Метангидратное ружье. Задача 3. Команда: Когнитивная машина
Метангидратное ружье. Задача 3. Команда: Когнитивная машина Химические элементы человеческого организма и их свойства
Химические элементы человеческого организма и их свойства Курс лекций по химии
Курс лекций по химии Поняття про валентність. Ребус
Поняття про валентність. Ребус Тема 1. Металлы и сплавы
Тема 1. Металлы и сплавы Радиоспектроскопические методы исследования, часть 1
Радиоспектроскопические методы исследования, часть 1 Теория химического строения А. М. Бутлерова. Часть III
Теория химического строения А. М. Бутлерова. Часть III Скорость химических реакций. Химическое равновесие
Скорость химических реакций. Химическое равновесие Особенности гигиенического нормирования экзогенных химических веществ в воде водоемов
Особенности гигиенического нормирования экзогенных химических веществ в воде водоемов