Содержание
- 2. История Гидроксид лития при стандартных условиях представляет собой бесцветные кристаллы с тетрагональной решёткой. Едкое вещество. Обладает
- 3. Физические свойства Формула LiOH. Гидроксид лития представляет собой бесцветные кристаллы, без запаха. Температура плавления 462°С. Температура
- 4. Химические свойства Взаимодействие с кислотами с образованием соли и воды (реакция нейтрализации): LiOH + HNO3 →
- 5. Получение Взаимодействие лития с водой: 2Li + 2H2O → 2LiOH + H2↑ Взаимодействие оксида лития с
- 7. Скачать презентацию




 NaCl – хлорид натрия
NaCl – хлорид натрия Полимеры
Полимеры Фосфор туралы
Фосфор туралы Электронное строение атома. Лекция № 2
Электронное строение атома. Лекция № 2 Ковалентная химическая связь
Ковалентная химическая связь Многоядерные Арены
Многоядерные Арены Нитробактерии. Нитратное дыхание
Нитробактерии. Нитратное дыхание EPR of phosphorus in diamond crystals. An influence of nitrogen impurity, HTHP treatment and high phosphorus concentration
EPR of phosphorus in diamond crystals. An influence of nitrogen impurity, HTHP treatment and high phosphorus concentration Водород как элемент и простое вещество
Водород как элемент и простое вещество Презентация1
Презентация1 6-я группа элементов. 9 класс
6-я группа элементов. 9 класс Химия элементов. Лекция 7 Общая характеристика элементов IIБ-группы. Цинк и кадмий. Ртуть
Химия элементов. Лекция 7 Общая характеристика элементов IIБ-группы. Цинк и кадмий. Ртуть  Полиморфизм кристаллов изатина
Полиморфизм кристаллов изатина IIIB (d-элемент). Скандий
IIIB (d-элемент). Скандий Полистирол. Вспенивающийся полистирол
Полистирол. Вспенивающийся полистирол Кремний и его соединения
Кремний и его соединения Решение задач по химии (ОГЭ, ЕГЭ, Олимпиады)
Решение задач по химии (ОГЭ, ЕГЭ, Олимпиады)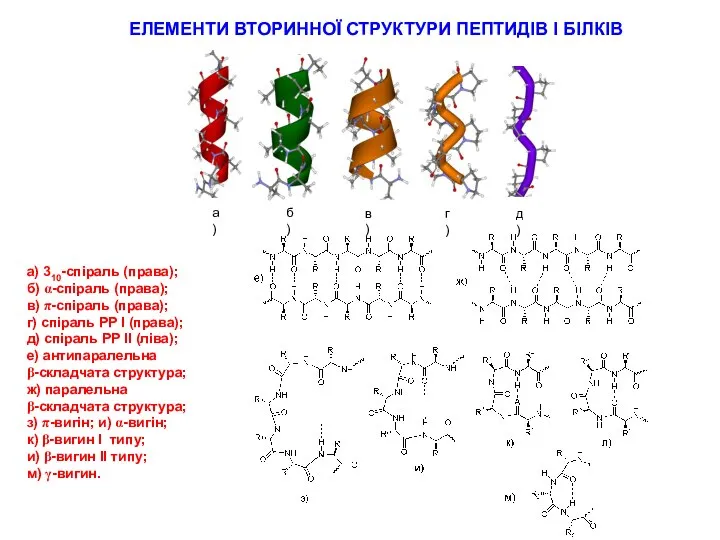 Елементи вторинної структури пептидів і білків
Елементи вторинної структури пептидів і білків Галогены
Галогены The production of stable isotopes
The production of stable isotopes Углеводы. 10 класс
Углеводы. 10 класс Презентация по химии Тема : « Большое приключение маленькой спички»
Презентация по химии Тема : « Большое приключение маленькой спички» Композиционные материалы для изоляции электрических машин
Композиционные материалы для изоляции электрических машин Проектная работа «Кристаллизация»
Проектная работа «Кристаллизация» Углеводородные и неуглеводородные соединения нефти. Физические свойства нефти. Химические классификации нефти
Углеводородные и неуглеводородные соединения нефти. Физические свойства нефти. Химические классификации нефти Аттестационная работа. Химия в продуктах питания
Аттестационная работа. Химия в продуктах питания Презентация по Химии "Симметрия в мире химии: кристаллы" - скачать смотреть
Презентация по Химии "Симметрия в мире химии: кристаллы" - скачать смотреть  Неорганические вещества клетки
Неорганические вещества клетки