Содержание
- 2. Древние люди были очень близки к открытию этого металлы во всех точках земного шара. Так, например,
- 3. ИНТЕРЕСНЫЕ ФАКТЫ ОБ АЛЮМИНИИ -Это третий по распространённости на земле элемент. -На его долю приходится более
- 4. ИСТОРИЯ ОТКРЫТИЯ Впервые алюминий был получен датским физиком Гансом Эрстедом в 1825 году действием амальгамы калия
- 5. Положение в ПСХЭ Д.И. Менделеева и строение атома алюминия 3 период, 3 группа, главная подгруппа
- 6. НАХОЖДЕНИЕ АЛЮМИНИЯ В ПРИРОДЕ По распространённости в земной коре занимает 1-е место среди металлов и 3-е
- 7. ФИЗИЧЕСКИЕ СВОЙСТВА АЛЮМИНИЯ Металл серебристо-белого цвета, лёгкий, пластичен, плотность — 2712 кг/м³, температура плавления у технического
- 8. ХИМИЧЕСКИЕ СВОЙСТВА АЛЮМИНИЯ Алюминий легко взаимодействует с кислородом при обычных условиях и покрыт оксидной пленкой (она
- 9. С др. неМе Аl + S → … Аl + N2 → . Аl + Р→
- 10. В) Al2Br3 + H2 ПЕРВИЧНОЕ ПРИМЕНЕНИЕ ЗНАНИЙ УСТАНОВИТЕ СООТВЕТСТВИЕ МЕЖДУ ИСХОДНЫМИ ВЕЩЕСТВАМИ И ПРОДУКТАМИ РЕАКЦИЙ: 1)
- 12. Скачать презентацию
Древние люди были очень близки к открытию этого металлы во всех
Древние люди были очень близки к открытию этого металлы во всех
АЛЮМИНИЙ.
НАХОЖДЕНИЕ АЛЮМИНИЯ В ПРИРОДЕ.
ФИЗИЧЕСКИЕ И ХИМИЧЕСКИЕ СВОЙСТВА
Как вы думаете, о каком металле шла речь?
Сами, трудясь, вы сделаете все и для близких людей и для себя, а если при труде успеха не будет, неудача - не беда, попробуйте ещё.
Д. И. Менделеев.
ИНТЕРЕСНЫЕ ФАКТЫ ОБ АЛЮМИНИИ
-Это третий по распространённости на земле элемент.
-На его
ИНТЕРЕСНЫЕ ФАКТЫ ОБ АЛЮМИНИИ
-Это третий по распространённости на земле элемент.
-На его
-В 1978 г. в породах Сибирской платформы обнаружен самородок этого металла в виде нитевидных кристаллов длиной 0,5 мм.
-Найден в лунном грунте.
-Был открыт в 1825 г. и стоил в 1500 раз дороже золота.
-Погремушку, изготовленную из этого металла, торжественно преподнесли сыну Наполеона III.
-Только очень богатые люди могли позволить себе употреблять пищу из таких тарелок, изготовленных из этого металла.
-1855 год, Парижская выставка – алюминий демонстрировался как самый редкий и дорогой металл, который был почти в 10 раз дороже золота.
Что вы знаете об алюминии?
Почему алюминий, которого так много в природе, был в XIX веке очень дорогим металлом, а в XX веке стал повседневным?
ИСТОРИЯ ОТКРЫТИЯ
Впервые алюминий был получен датским физиком Гансом Эрстедом в 1825
ИСТОРИЯ ОТКРЫТИЯ
Впервые алюминий был получен датским физиком Гансом Эрстедом в 1825
До открытия промышленного способа получения алюминия этот металл был дороже золота. В 1889 году британцы, желая почтить богатым подарком великого русского химика Д. И. Менделеева, подарили ему весы из золота и алюминия.
Положение в ПСХЭ Д.И. Менделеева и строение атома алюминия
3 период, 3
Положение в ПСХЭ Д.И. Менделеева и строение атома алюминия
3 период, 3
НАХОЖДЕНИЕ АЛЮМИНИЯ В ПРИРОДЕ
По распространённости в земной коре занимает 1-е место
НАХОЖДЕНИЕ АЛЮМИНИЯ В ПРИРОДЕ
По распространённости в земной коре занимает 1-е место
Каолинит
Al2O3·2SiO2 · 2H2O
Корунд
Al2O3- (рубин, сапфир)
Полевой шпат, ортоклаз
(K,Na)2O·Al2O3·6SiO2, Ca[Al2Si2O8]
Боксит Al2O3 · H2O
Нефелин
KNa3[AlSiO4]4
ФИЗИЧЕСКИЕ СВОЙСТВА АЛЮМИНИЯ
Металл серебристо-белого цвета, лёгкий, пластичен, плотность — 2712
ФИЗИЧЕСКИЕ СВОЙСТВА АЛЮМИНИЯ
Металл серебристо-белого цвета, лёгкий, пластичен, плотность — 2712
ПОЛУЧЕНИЕ АЛЮМИНИЯ
Лабораторный способ получения алюминия предложил Фридрих Вёлер в 1827 году восстановлением металлическим калием безводного хлорида алюминия (реакция протекает при нагревании без доступа воздуха): AlCI3 + 3K → 3KCI + Al
Современный метод получения, процесс Холла — Эру, был разработан независимо американцем Чарльзом Холлом и французом Полем Эру в 1886 году. Он заключается в растворении оксида алюминия Al2O3 в расплаве криолита Na3AlF6 с последующим электролизом Такой метод получения требует очень больших затрат электроэнергии и поэтому получил промышленное применение только в XX веке.
ХИМИЧЕСКИЕ СВОЙСТВА АЛЮМИНИЯ
Алюминий легко взаимодействует с кислородом при обычных условиях и
ХИМИЧЕСКИЕ СВОЙСТВА АЛЮМИНИЯ
Алюминий легко взаимодействует с кислородом при обычных условиях и
С.О. +3
Al + H2O → …
С водой
2Al + 6 H2O = 2Al (OH)3 + 3H2
В виде стружек или порошка он ярко горит на воздухе, выделяя большое количество теплоты: 4Аl + 3O2 = 2Аl2О3 + 1676 кДж.
С О2
С Gal
2Аl + 3I2 → …
2Аl + 3СI2 → …
2Аl + 3I2 = 2AlI3 (йодид алюминия)
2Аl + 3СI2 = 2AlCI3 (хлорид алюминия)
Во втором уравнении, покажите процессы восстановления и окисления, а также определите восстановитель и окислитель
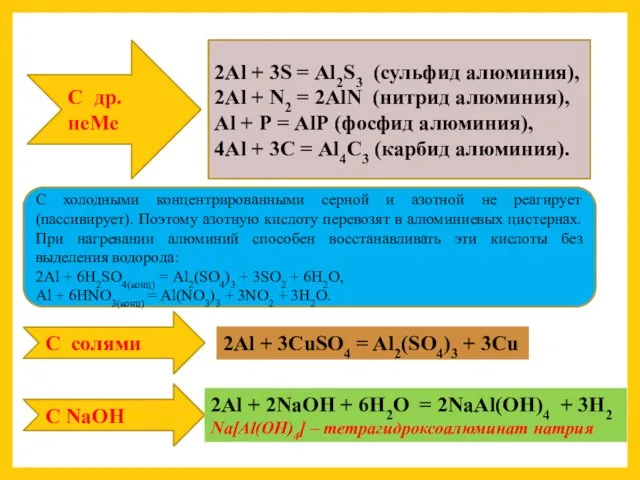
С др. неМе
Аl + S → …
Аl + N2 → .
Аl + Р→ …
Аl + С→ …
2Аl +
С др. неМе
Аl + S → …
Аl + N2 → .
Аl + Р→ …
Аl + С→ …
2Аl +
2Аl + N2 = 2АlN (нитрид алюминия),
Аl + Р = АlР (фосфид алюминия),
4Аl + 3С = Аl4С3 (карбид алюминия).
С кислотами
2 Al + 3 H2SO4 → …
2 Al + 3 H2SO4 = Al2(SO4)3 + 3 H2
С солями
С холодными концентрированными серной и азотной не реагирует (пассивирует). Поэтому азотную кислоту перевозят в алюминиевых цистернах. При нагревании алюминий способен восстанавливать эти кислоты без выделения водорода:
2Аl + 6Н2SО4(конц) = Аl2(SО4)3 + 3SО2 + 6Н2О,
Аl + 6НNO3(конц) = Аl(NO3)3 + 3NO2 + 3Н2О.
2Al + 3CuSO4 → …
2Al + 3CuSO4 = Al2(SO4)3 + 3Cu
С NaOH
2Al + 2NaOH + 6H2O → …
2Al + 2NaOH + 6H2O = 2NaAl(OH)4 + 3H2
Na[Аl(ОН)4] – тетрагидроксоалюминат натрия
В) Al2Br3 + H2
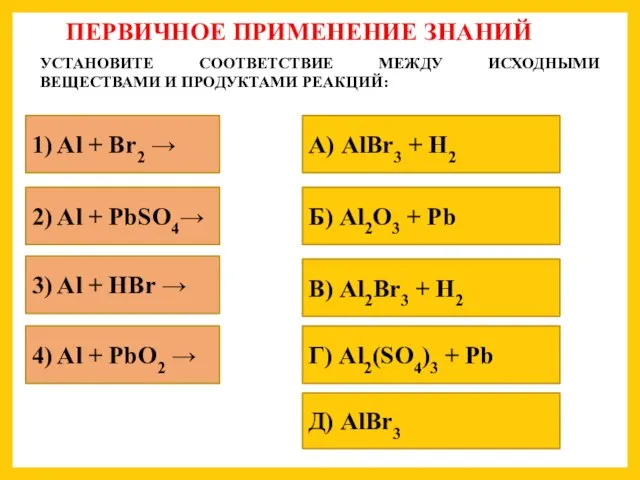
ПЕРВИЧНОЕ ПРИМЕНЕНИЕ ЗНАНИЙ
УСТАНОВИТЕ СООТВЕТСТВИЕ МЕЖДУ ИСХОДНЫМИ ВЕЩЕСТВАМИ И
В) Al2Br3 + H2
ПЕРВИЧНОЕ ПРИМЕНЕНИЕ ЗНАНИЙ
УСТАНОВИТЕ СООТВЕТСТВИЕ МЕЖДУ ИСХОДНЫМИ ВЕЩЕСТВАМИ И
1) Al + Br2 →
3) Al + HBr →
2) Al + PbSO4→
4) Al + PbO2 →
А) AlBr3 + H2
Б) Al2O3 + Pb
Д) AlBr3
Г) Al2(SO4)3 + Pb







 Перечень практических навыков по общей химии для экзамена
Перечень практических навыков по общей химии для экзамена Химия вокруг нас
Химия вокруг нас Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Химическая реакция – превращение одних веществ в другие
Химическая реакция – превращение одних веществ в другие Минералдарды зерттеу әдістері
Минералдарды зерттеу әдістері Биохимия
Биохимия Эколого-геохимическая оценка состояния компонентов природной среды особо охраняемых территорий. Парк Смоленское Поозерье
Эколого-геохимическая оценка состояния компонентов природной среды особо охраняемых территорий. Парк Смоленское Поозерье Типы химических реакций
Типы химических реакций Петрология. Классификации магматических горных пород
Петрология. Классификации магматических горных пород Химия және денсаулық
Химия және денсаулық Атомная энергетика
Атомная энергетика Титан как элемент
Титан как элемент Алюминий. Сплавы алюминия. Учитель: Белозерова Татьяна Анатольевна Учени
Алюминий. Сплавы алюминия. Учитель: Белозерова Татьяна Анатольевна Учени Углеводороды и их природные источники. Гомологический ряд алканов. Строение алканов
Углеводороды и их природные источники. Гомологический ряд алканов. Строение алканов Каталитическая активность ферментов Работу выполнили: Кичаева Нина Иванькова Елена Ученицы 10 класса МОУ Сергиевской СОШ №1 «О
Каталитическая активность ферментов Работу выполнили: Кичаева Нина Иванькова Елена Ученицы 10 класса МОУ Сергиевской СОШ №1 «О Метаболизм - обмен веществ
Метаболизм - обмен веществ Химия актиноидов
Химия актиноидов Чистые вещества и смеси. Способы разделения смесей
Чистые вещества и смеси. Способы разделения смесей КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ
КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ  Лекция №6. Применение закона действующих масс к окислительно-восстановительным равновесиям
Лекция №6. Применение закона действующих масс к окислительно-восстановительным равновесиям Химиялық термодинамиканың негіздері. Негізгі түсініктері мен аңдары. Термохимиялық есептеулер
Химиялық термодинамиканың негіздері. Негізгі түсініктері мен аңдары. Термохимиялық есептеулер Кетоновые тела
Кетоновые тела Нанохимия, как наука
Нанохимия, как наука Autoionization of water Hydrolysis of salts
Autoionization of water Hydrolysis of salts Строение гетероциклических соединений
Строение гетероциклических соединений Применение s-, p-, d- элементов в медицине
Применение s-, p-, d- элементов в медицине Чипсы, вред или польза
Чипсы, вред или польза Бродильні мікроорганізми і бродіння. Лекція 5
Бродильні мікроорганізми і бродіння. Лекція 5