Содержание
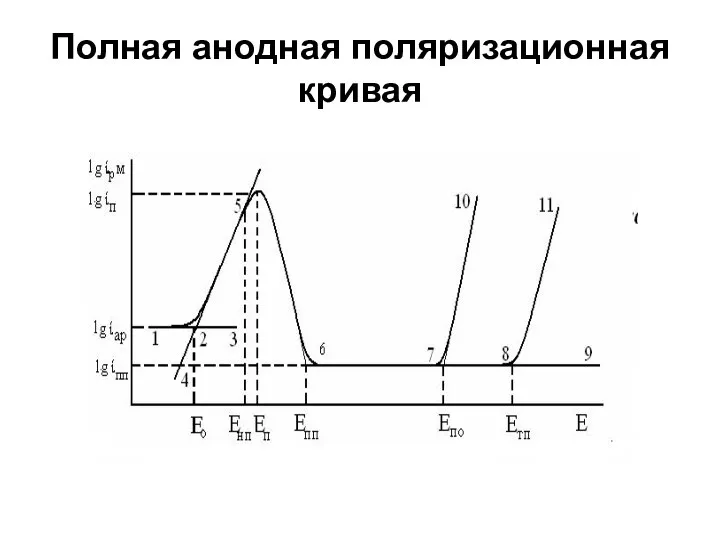
- 2. Полная анодная поляризационная кривая
- 3. - аномального растворения (1, 2, 3), - электрохимического активного растворения (4, 2, 5), пассивации (5, 6),
- 4. Указанные области при изменении состава раствора, сплава и температуры могут частично исчезать. При снижении рН и
- 5. Способы получения полной кривой 1. С помощью потенциостата 2. Измерение последовательно меняющихся j при варьировании Екор
- 6. Активное растворение Растворение металла - с т а д и й н ы й п р
- 7. При АР анодная поляризация может быть вызвана замедленностью ионизации или диффузии. Причина концентрационной поляризации - накопление
- 8. Влияние анионов Изменяют строение ДЭС и к образуют с ионами металла поверхностные комплексы и в объеме
- 9. Если прочность связи М-А и А-растворитель выше, чем М-М, анионы ускоряют процесс. Если связь М-М и
- 10. Примером процессов, протекающих по стадийному механизму с образованием промежуточных комплексов низковалентных частиц, является растворение Fe, скорость
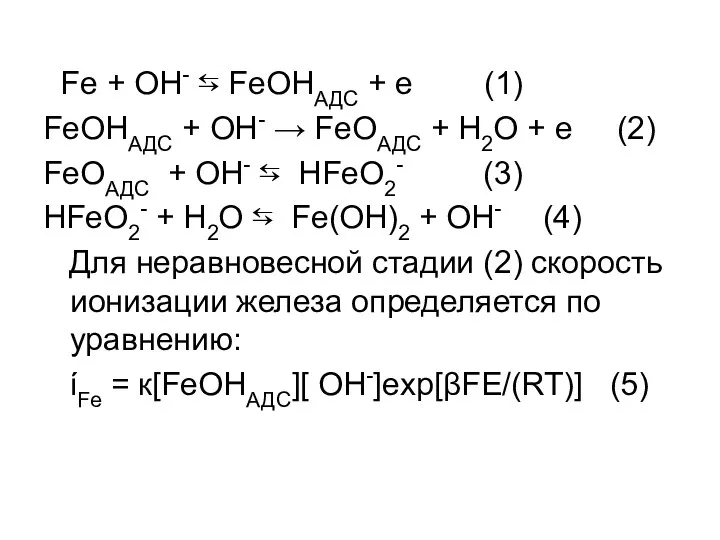
- 11. Fe + OH- ⇆ FeOHАДС + e (1) FeOHАДС + OH- → FeOАДС + Н2О +
- 12. Для равновесной стадии (1): Е = рЕо + RT/Fln [FeOHАДС]/[OH-] (6) Откуда следует: [FeOHАДС] = к2[
- 13. дает правильный порядок реакции по ОН--ионам (δlgί/δpH)E = 2 и тафелев коэффициент (δE/δlgίFe)pH = 2,3RT/ F
- 14. Mеханизм растворения Fe в кислых сульфатных средах: Fe + Н2О ⇆ FeOH-АДС+ Н+ (10) FeOH-АДС ⇆
- 15. П а с с и в а ц и я и п а с с и
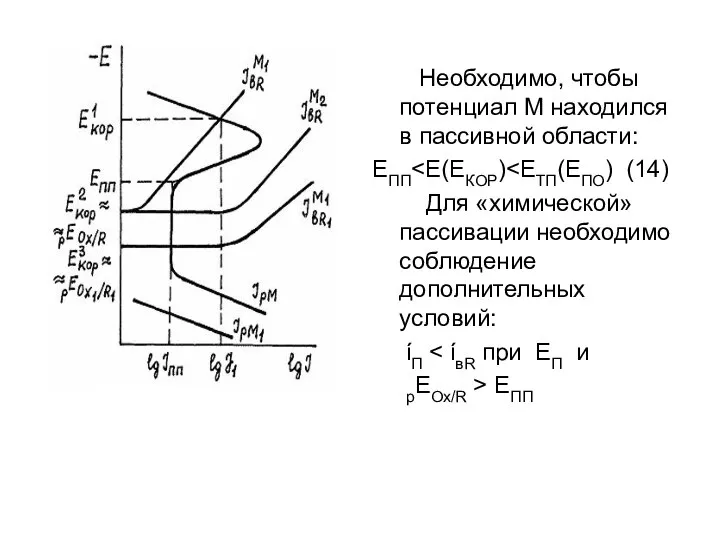
- 16. Необходимо, чтобы потенциал М находился в пассивной области: ЕПП Для «химической» пассивации необходимо соблюдение дополнительных условий:
- 17. Пленочная теория пассивации Снижение ίрМ обусловлено образованием на поверхности металла фазы оксида, обладающей электронной и слабой
- 18. Слабая зависимость ίПП от Е объясняется компенсацией двух эффектов: ростом ίрМ с Е и повышением защитной
- 19. Для определения области пассивного состояния металлов в первом приближении используются диаграммы Пурбе Е – рН. В
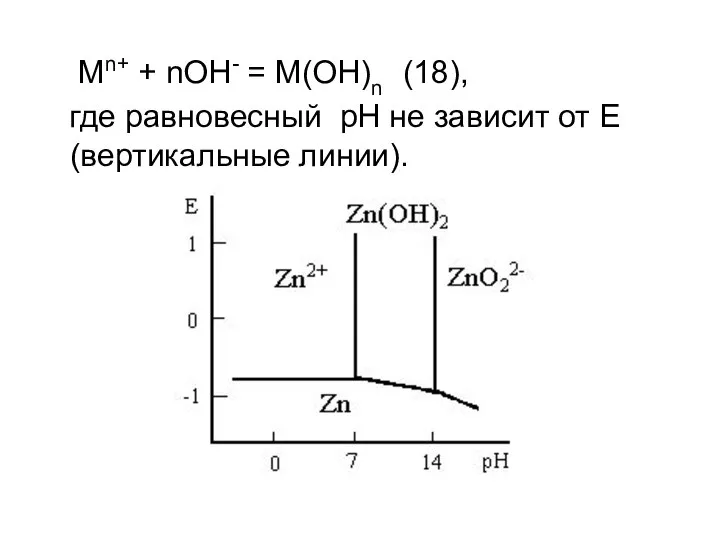
- 20. Мn+ + nOH- = M(OH)n (18), где равновесный рН не зависит от Е (вертикальные линии).
- 21. На диаграмме имеются области (иммунности) металла (Zn), активного растворения (Zn2+ и ZnO22-) и возможной пассивности (Zn(OH)2),
- 22. Формирование пленки начинается при рЕ оксидного электрода, а область устойчивого пассивного состояния начинается при ЕПП. Обычно
- 23. Адсорбционная теория Пассивность обусловлена хемосорбцией компонентов раствора (О). Растворение металла тормозится за счет блокировки активных центров
- 24. Адсорбцию можно рассматривать как первичный процесс при последующем образовании пленки. Иногда пассивация является следствием образования фазовых
- 25. Транспассивация Равномерное активное растворение металла, т.е. выход металла из пассивного состояния с ростом анодной поляризации. С
- 26. Аномальное растворение Аномальное 1. Iap ≠ f(E) 2. Скорость не зависит от природы и С неокислительных
- 27. Трактовки аномального растворения 1. Процесс электрохимический, осложненный вторичными явлениями при катодной поляризации. Снижение ipM при катодной
- 28. 2. Химический Хемосорбция компонентов раствора на М создаёт предпосылку для непосредственного взаимодействия М с Ох в
- 29. 3. Концепция химико-электрохимического растворения, по которой химическое (аномальное) и электрохимическое (активное) растворение протекают параллельно и ipM=iap+iэх
- 31. Скачать презентацию








![Для равновесной стадии (1): Е = рЕо + RT/Fln [FeOHАДС]/[OH-] (6)](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1405467/slide-11.jpg)















 Реакции горения и материальный баланс котла
Реакции горения и материальный баланс котла Викторина «Своя игра». Периодический закон и периодическая система химических элементов Д.И. Менделеева
Викторина «Своя игра». Периодический закон и периодическая система химических элементов Д.И. Менделеева Шампуни: классификация по составу и назначению
Шампуни: классификация по составу и назначению Презентация по Химии "«Подгруппа углерода»" - скачать смотреть
Презентация по Химии "«Подгруппа углерода»" - скачать смотреть  Презентация по Химии "кристаллические решетки." - скачать смотреть бесплатно_
Презентация по Химии "кристаллические решетки." - скачать смотреть бесплатно_ Презентация по Химии "Исследование содержания глюкозы в различных соках" - скачать смотреть
Презентация по Химии "Исследование содержания глюкозы в различных соках" - скачать смотреть 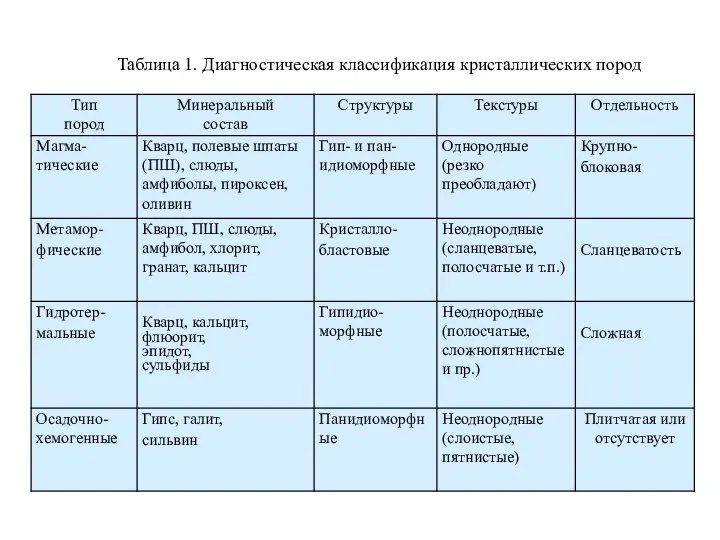 Диагностика метаморфических и гидротермальных горных пород
Диагностика метаморфических и гидротермальных горных пород Взаимное влияние атомов в молекулах органических соединений
Взаимное влияние атомов в молекулах органических соединений Аттестационная работа. Образовательная программа внеурочной деятельности «Химия красок»
Аттестационная работа. Образовательная программа внеурочной деятельности «Химия красок» Азотные удобрения
Азотные удобрения Крекінг нафти Виконав учень 11-Б класу Кравець Дмитро
Крекінг нафти Виконав учень 11-Б класу Кравець Дмитро  An introduction to bonding
An introduction to bonding Свойства металлов и сплавов
Свойства металлов и сплавов Полімери. Будова і властивості полімерів
Полімери. Будова і властивості полімерів Растворы. Гетерогенные равновесия растворов с осадком
Растворы. Гетерогенные равновесия растворов с осадком Углерод и его соединения
Углерод и его соединения Химическая связь. Электроотрицательность. Ковалентная связь
Химическая связь. Электроотрицательность. Ковалентная связь Введение в химию. Теоретические основы химии
Введение в химию. Теоретические основы химии Аминокислоты и их производные
Аминокислоты и их производные Строение вещества. Строение атома и периодическая система элементов
Строение вещества. Строение атома и периодическая система элементов Особенности соединений углерода, их многообразие, роль в живой природе и практической деятельности человека
Особенности соединений углерода, их многообразие, роль в живой природе и практической деятельности человека Пластмаси. Пластичні маси
Пластмаси. Пластичні маси Основные классы неорганических соединений
Основные классы неорганических соединений Циклоалканы
Циклоалканы Сплави металів
Сплави металів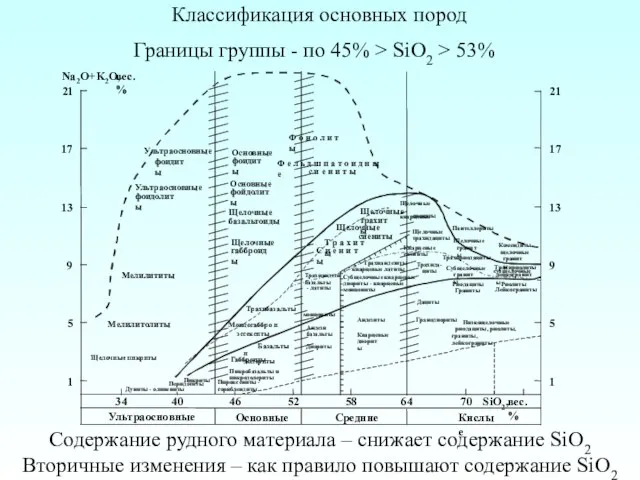 Классификация основных пород
Классификация основных пород ПЕРИОДИЧЕСКАЯ СИСТЕМА ХИМИЧЕСКИХ ЭЛЕМЕНТОВ Д. И. МЕНДЕЛЕЕВА
ПЕРИОДИЧЕСКАЯ СИСТЕМА ХИМИЧЕСКИХ ЭЛЕМЕНТОВ Д. И. МЕНДЕЛЕЕВА S-,p-,d-элементтердің медициналы-биологиялық маңызы
S-,p-,d-элементтердің медициналы-биологиялық маңызы