Содержание
- 2. Характеристика элемента С С* 1s22s22p2 1s22s12p3 Основное состояние + Е Возбужденное состояние Степени окисления: -4, 0,
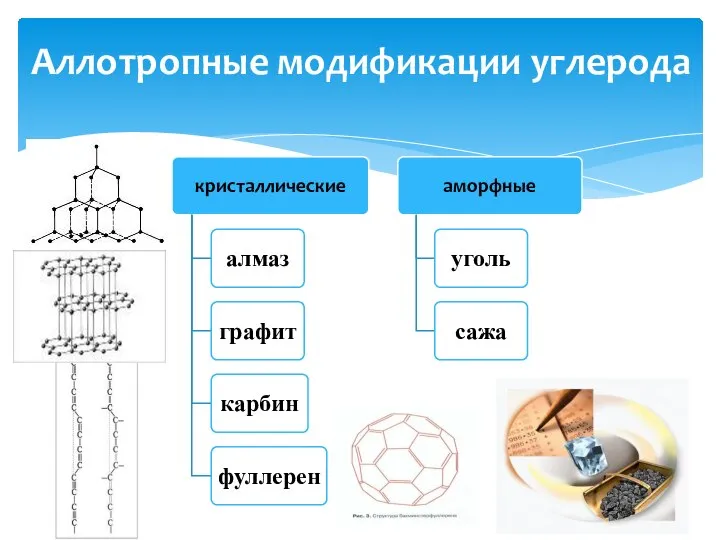
- 3. Аллотропные модификации углерода
- 4. При разложении древесины без доступа воздуха и при обугливании органических соединений образуется углерод (сажа). конц.Н2SO4 C6Н12О6
- 5. 1) с металлами образует карбиды 4Al+3C=Al4C3 (при нагревании) Из карбида алюминия получают метан Al4C3 +12H2O =4Al(OH)3+
- 6. 3) горит в кислороде с выделением большого количества тепла 2C + O2 = 2CO + Q
- 7. C + 4 НNO3 = CO2 + 4NО2 + 2Н2O конц. C + 2 Н2SO4 =
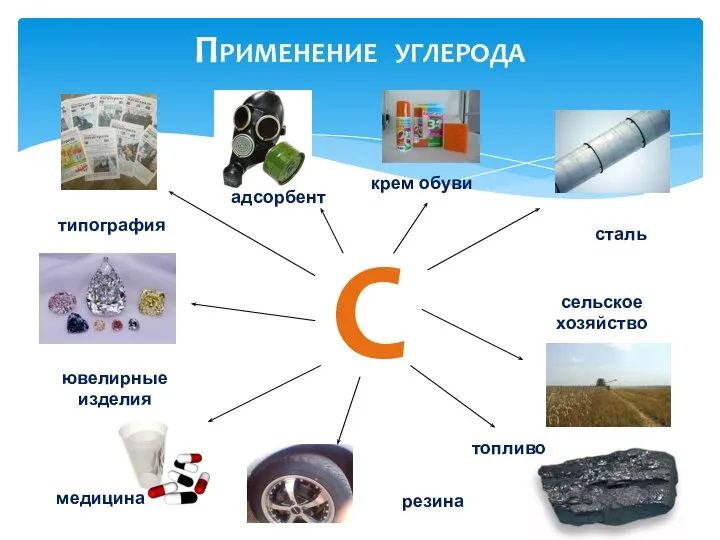
- 8. С сталь сельское хозяйство топливо медицина типография ювелирные изделия адсорбент резина крем обуви Применение углерода
- 9. Метан СН4
- 11. несолеобразующий кислотный СО2 + 2 NaОН = Na2CO3 + H2O СО2 + СаО = СаСО3 восстановитель
- 12. H2CO3 – очень слабая и неустойчивая кислота, разлагается при кипячении. Диссоциация: H2CO3 Н+ + HCO3 -
- 13. Соли: средние – карбонаты Nа2СО3, СаСО3 и кислые – гидрокарбонаты NаНСО3, Са(НСО3)2 1) разлагаются при нагревании:
- 14. Карбонаты и гидрокарбонаты легко превращаются друг в друга. При этом в природе образуются причудливые сталактиты и
- 15. Соли угольной кислоты Гидрокарбонат натрия – NaHCO3 , питьевая, или пищевая сода Добавляется в кондитерские изделия,
- 17. Скачать презентацию












 Полимеры
Полимеры Презентация по Химии "Белки" - скачать смотреть _
Презентация по Химии "Белки" - скачать смотреть _ Окислительно-восстановительные реакции в органической химии
Окислительно-восстановительные реакции в органической химии Значення білків, жирів та вуглеводів у харчуванні людини
Значення білків, жирів та вуглеводів у харчуванні людини  Химические элементы. Викторина
Химические элементы. Викторина Вещества, действующие на мембрану клетки и клеточную стенку. Занятие 5
Вещества, действующие на мембрану клетки и клеточную стенку. Занятие 5 Вода Самое удивительное вещество
Вода Самое удивительное вещество Обобщение знаний об углеводородах Автор Акимова Ольга Васильевна учитель химии, высшая квалификационная категория МАОУ Барыби
Обобщение знаний об углеводородах Автор Акимова Ольга Васильевна учитель химии, высшая квалификационная категория МАОУ Барыби Химическая связь. Валентность элементов в ковалентных соединениях. Степень окисления элементов
Химическая связь. Валентность элементов в ковалентных соединениях. Степень окисления элементов «Мінеральні добрива»
«Мінеральні добрива»  Электролитическая диссоциация(ЭД). Теория электролитической диссоциации (ТЭД)
Электролитическая диссоциация(ЭД). Теория электролитической диссоциации (ТЭД)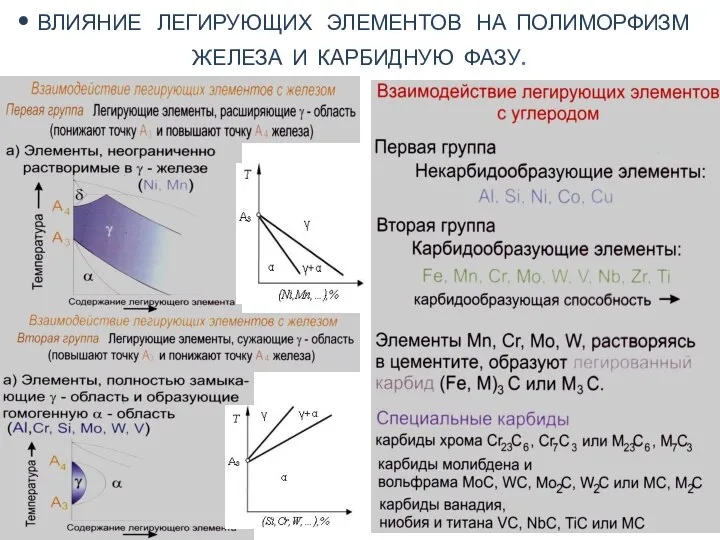 Влияние легирующих элементов на полиморфизм железа и карбидную фазу
Влияние легирующих элементов на полиморфизм железа и карбидную фазу Проектная деятельность школьников в процессе обучения химии
Проектная деятельность школьников в процессе обучения химии Dzeramā ūdens sagatavošanas shēma
Dzeramā ūdens sagatavošanas shēma Сульфаниламидные препараты. (Тема 5)
Сульфаниламидные препараты. (Тема 5) Презентация по Химии "«Кристаллические решетки»" - скачать смотреть
Презентация по Химии "«Кристаллические решетки»" - скачать смотреть  Щелочные металлы
Щелочные металлы Коррозия металлов
Коррозия металлов Хром. Роль хрома в организме человека
Хром. Роль хрома в организме человека  Аминокислоты. Номенклатура аминокислот
Аминокислоты. Номенклатура аминокислот Сложные эфиры. Жиры. Мыло
Сложные эфиры. Жиры. Мыло Презентация по Химии "Химия. Щелочные металлы" - скачать смотреть
Презентация по Химии "Химия. Щелочные металлы" - скачать смотреть  Типы изомерии 1.Историческая справка 2.Изомерия. Изомеры. 3.Типы изомерии. Классификация изомеров.
Типы изомерии 1.Историческая справка 2.Изомерия. Изомеры. 3.Типы изомерии. Классификация изомеров.  Окислительно-восстановительные реакции (ОВР)
Окислительно-восстановительные реакции (ОВР) Хімічний склад синтетичних миючих засобів та їх основні нормативно-технічні показники
Хімічний склад синтетичних миючих засобів та їх основні нормативно-технічні показники Свойства серной кислоты и солей
Свойства серной кислоты и солей Кислоты: состав, строение, классификация
Кислоты: состав, строение, классификация Системный анализ и моделирование процессов. Горение паро-газо-воздушного облака
Системный анализ и моделирование процессов. Горение паро-газо-воздушного облака