Содержание
- 2. Способы получения Аренов 1) Ароматизация Алканов с C6 и более(в главной цепи). Если углеродов 6 образуется
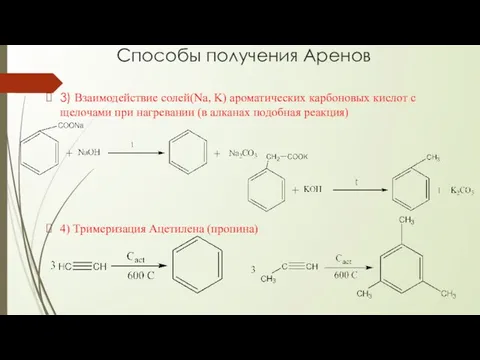
- 3. Способы получения Аренов 3) Взаимодействие солей(Na, K) ароматических карбоновых кислот с щелочами при нагревании (в алканах
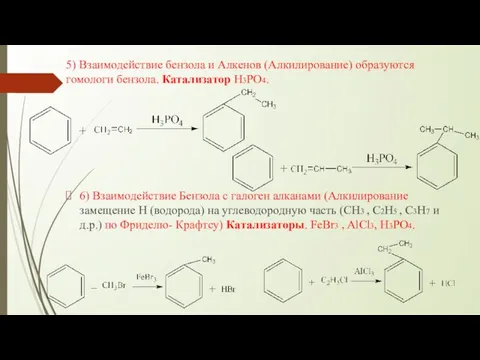
- 4. 5) Взаимодействие бензола и Алкенов (Алкилирование) образуются гомологи бензола. Катализатор H3PO4. 6) Взаимодействие Бензола с галоген
- 5. 7) Взаимодействие Бензола со спиртами kat.-H3PO4 8) Взаимодействие галоген аренов с галоген алкаными при помощи металлического
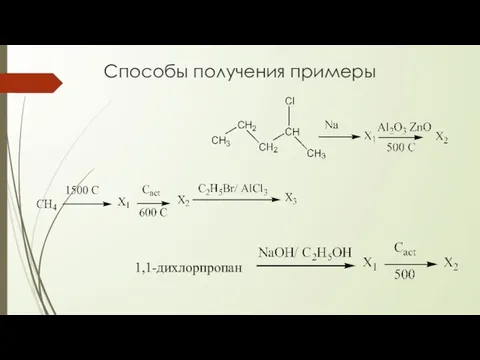
- 6. Способы получения примеры 1,1-дихлорпропан
- 7. Химические свойства Аренов Арены способны вступать в реакции Замещения так и в реакции Присоединения (в более
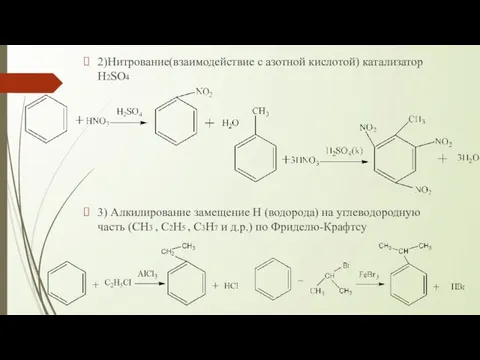
- 8. 2)Нитрование(взаимодействие с азотной кислотой) катализатор H2SO4 3) Алкилирование замещение H (водорода) на углеводородную часть (CH3 ,
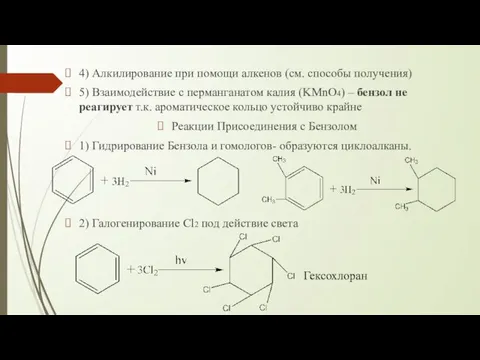
- 9. 4) Алкилирование при помощи алкенов (см. способы получения) 5) Взаимодействие с перманганатом калия (KMnO4) – бензол
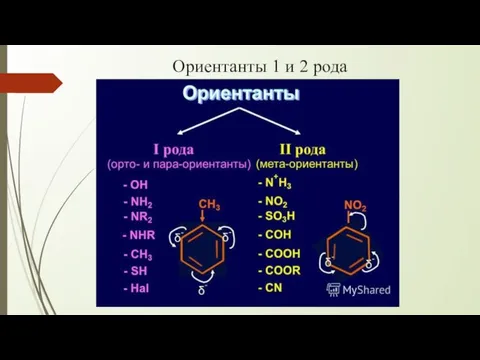
- 10. Ориентанты 1 и 2 рода
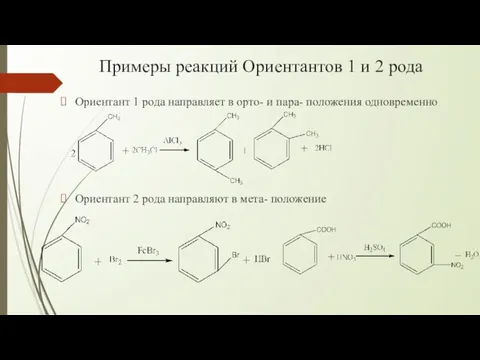
- 12. Примеры реакций Ориентантов 1 и 2 рода Ориентант 1 рода направляет в орто- и пара- положения
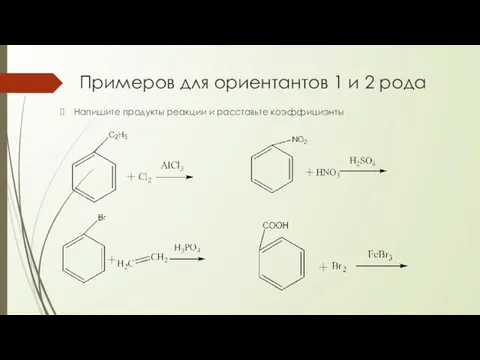
- 13. Примеров для ориентантов 1 и 2 рода Напишите продукты реакции и расставьте коэффициэнты
- 14. Хим свойства для гомологов Бензола 1) Галогенирование по действием света (как в Алканах) Замещается водород у
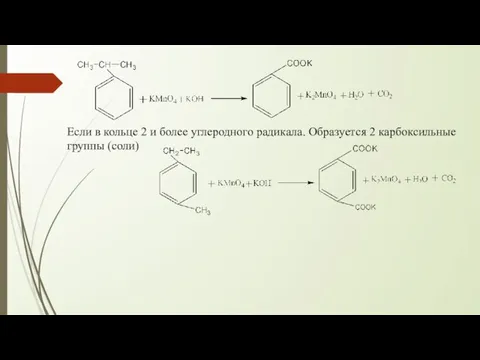
- 15. Если в кольце 2 и более углеродного радикала. Образуется 2 карбоксильные группы (соли)
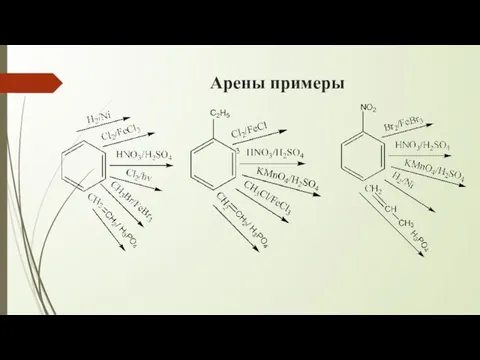
- 16. Арены примеры
- 17. Арены примеры Толуол: 1) Гидрирование 2) Галогенирование (Br2) с кат. 3) Нитрование (разбавленной азотной) 4)Алкилирование по
- 19. Скачать презентацию






 Углеводы. Карбоновые кислоты и их производные
Углеводы. Карбоновые кислоты и их производные Урок химии в 9-ом классе Тема урока "Сера"
Урок химии в 9-ом классе Тема урока "Сера" Пространственное строение органических соединений. (Лекция 2)
Пространственное строение органических соединений. (Лекция 2) Особенности химического состава клетки
Особенности химического состава клетки Каркасные силикаты
Каркасные силикаты Обмен белков и аминокислот. Азотистый баланс. (Лекция 14)
Обмен белков и аминокислот. Азотистый баланс. (Лекция 14) IVA группа С, Si, Ge, Sn, Pb (подгруппа титана)
IVA группа С, Si, Ge, Sn, Pb (подгруппа титана) Минерал как химическое соединение
Минерал как химическое соединение Тест по неорганической химии
Тест по неорганической химии Никель Ni
Никель Ni солі в природі Солі препарати замінення атомів водної кислоти
солі в природі Солі препарати замінення атомів водної кислоти  Камень, скользящий на льду
Камень, скользящий на льду Defect in solid
Defect in solid Элемент № 24 периодической таблицы. Хром
Элемент № 24 периодической таблицы. Хром Химическая термодинамика и биоэнергетика. Второй закон термодинамики
Химическая термодинамика и биоэнергетика. Второй закон термодинамики КУБАНСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ КАФЕДРА ФУНДАМЕНТАЛЬНОЙ И КЛИНИЧЕСКОЙ БИОХИМИИ Лекция по теме: «Матричные б
КУБАНСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ КАФЕДРА ФУНДАМЕНТАЛЬНОЙ И КЛИНИЧЕСКОЙ БИОХИМИИ Лекция по теме: «Матричные б Основные классы неорганических и органических соединений
Основные классы неорганических и органических соединений Реакция обменного разложения веществ водой - гидролиз
Реакция обменного разложения веществ водой - гидролиз Ресурсы и энергоснабжение
Ресурсы и энергоснабжение Газообразное состояние вещества
Газообразное состояние вещества Презентация по Химии "Алюминий (11 класс)" - скачать смотреть
Презентация по Химии "Алюминий (11 класс)" - скачать смотреть  Типы изомерии 1.Историческая справка 2.Изомерия. Изомеры. 3.Типы изомерии. Классификация изомеров.
Типы изомерии 1.Историческая справка 2.Изомерия. Изомеры. 3.Типы изомерии. Классификация изомеров.  Органическая химия и важнейшие органические соединения углевода
Органическая химия и важнейшие органические соединения углевода Состав, структура, свойства ДНК. (Лекция 2)
Состав, структура, свойства ДНК. (Лекция 2) Логическая структура модуля по дисциплине "Аналитическая химия"
Логическая структура модуля по дисциплине "Аналитическая химия" Мило
Мило  Роль микро- и макроэлементов в здоровье человека
Роль микро- и макроэлементов в здоровье человека Кремний и его «родственники»
Кремний и его «родственники»