Содержание
- 2. Цели и задачи Познакомить учащихся с эволюцией научных взглядов на строение атома Показать взаимодействие наук физики
- 3. Представления о строении атома Атом – «неделимая» частица химического элемента Доказательства сложности строения атома Открытие катодных
- 4. СЛОВО «АТОМ» ПРИДУМАЛ БОЛЕЕ 2500 ЛЕТ НАЗАД ДРЕВНЕГРЕЧЕСКИЙ ФИЛОСОФ ДЕМОКРИТ АТОМ – ЭТО МЕЛЬЧАЙШАЯ ХИМИЧЕСКИ НЕДЕЛИМАЯ
- 5. Представления о строении атома Классическая теория строения атома Модели строения атома: 1. «Пудинг с изюмом» (1902-1904
- 6. МОДЕЛЬ АТОМА ТОМСОНА Атом, по мысли Дж. Томсона, очень похож на пудинг с изюмом: электроны, как
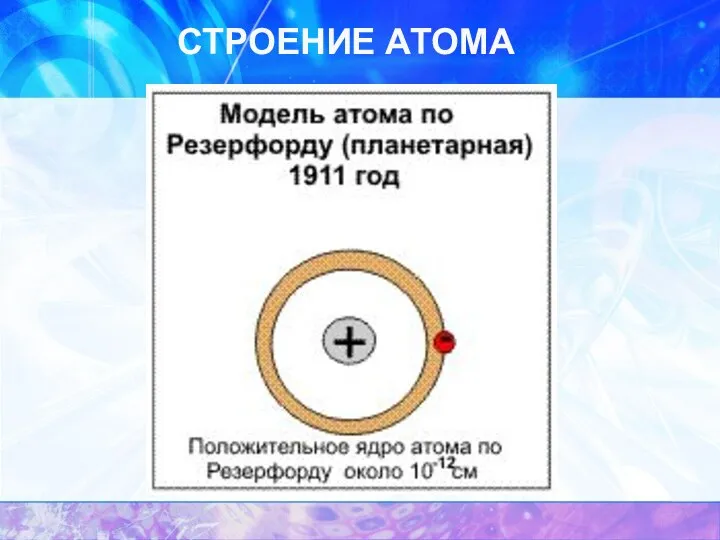
- 7. СТРОЕНИЕ АТОМА
- 8. Постулаты Н. Бора электроны в атоме вращаются по строго определённым замкнутым орбитам, не испуская и не
- 9. Современная квантовая модель Н. Бор - создатель первой квантовой теории атомаН. Бор - создатель первой квантовой
- 10. Современная модель атома
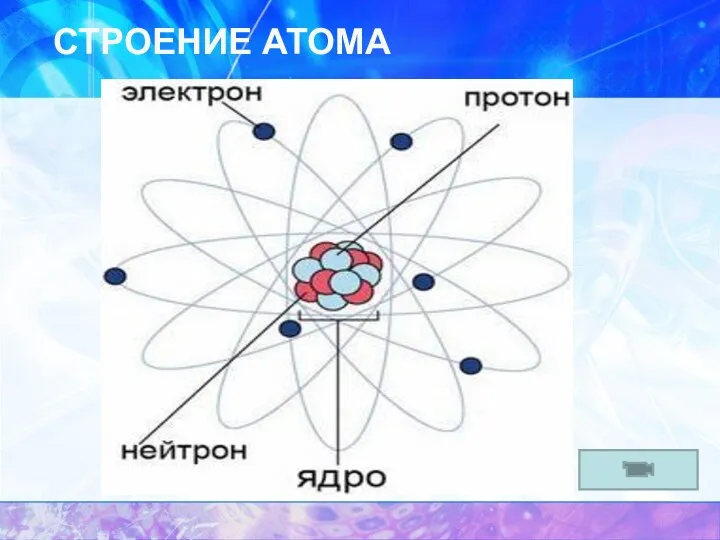
- 11. СТРОЕНИЕ АТОМА
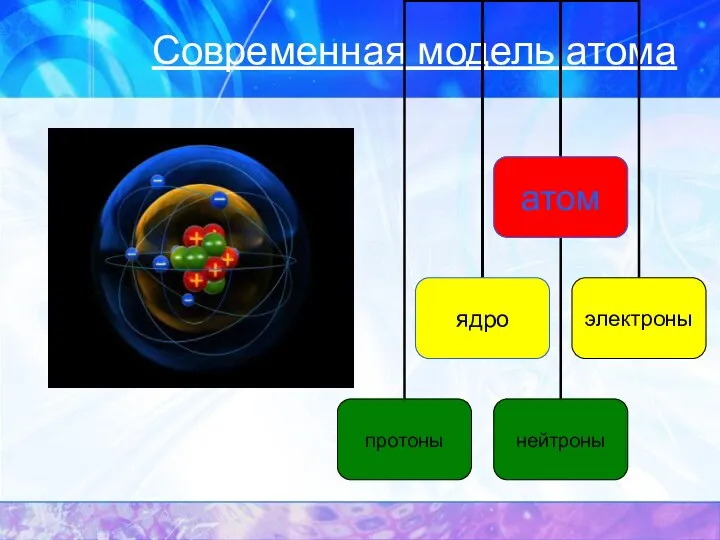
- 12. СТРОЕНИЕ АТОМА протоны нейтроны электроны атом ядро электронная оболочка
- 13. Z – порядковый номер химического элемента A – массовое число, A=Ar N – число нейтронов
- 14. Число p Z p = Z (порядковому номеру химического элемента) Число ē Z ē = Z
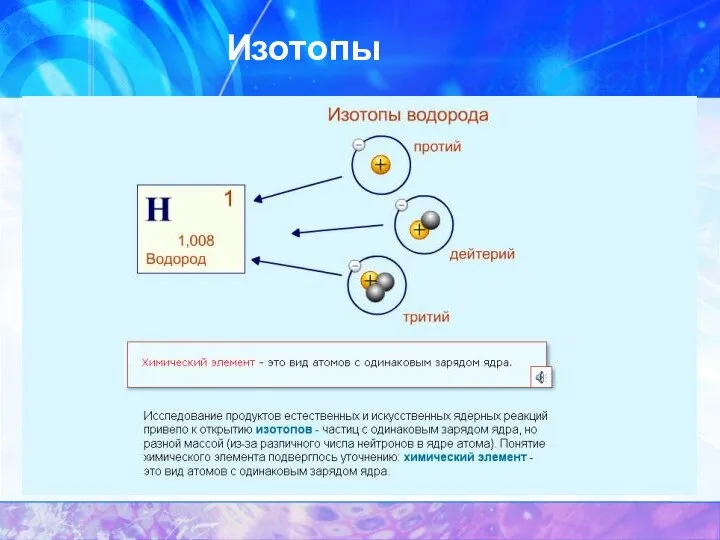
- 15. Изотопы
- 16. Нуклиды - различные виды атомов. Нуклиды характеризуются массовым числом А и зарядом ядра Z. Изотопы -
- 17. Задание 1. Запишите для 2-3 элементов (по вашему выбору). Элемент Порядковый номер Относительная атомная масса Заряд
- 18. Задание 2. Выполните следующие упражнения Назовите элемент, содержащий 23 протона. Назовите элементы II периода, содержащие 8
- 19. Задание 3. Определить состав изотопов 35Cl и 37Cl 28Si , 29Si, 30Si 39Ar, 40Ar Проверяем знания
- 21. Скачать презентацию














 Производные пиримидина. Производные пиримидин-2,4,6-триона (Барбитураты)
Производные пиримидина. Производные пиримидин-2,4,6-триона (Барбитураты) Химия вокруг нас Работа учеников 9 класса «В» МБОУ «СОШ №25» г.Набережные Челны Давлиев Камиль и Юманьков Антон
Химия вокруг нас Работа учеников 9 класса «В» МБОУ «СОШ №25» г.Набережные Челны Давлиев Камиль и Юманьков Антон  Игра «Химические элементы» (формулы и названия)
Игра «Химические элементы» (формулы и названия) Алюминий, его физические и химические свойства
Алюминий, его физические и химические свойства Производство бензина
Производство бензина Окислительно – восстановительные реакции. Раева Анна Семеновна Учитель химии МОБУ СОШ № 24 имени С. И. Климакова, г. Якутск
Окислительно – восстановительные реакции. Раева Анна Семеновна Учитель химии МОБУ СОШ № 24 имени С. И. Климакова, г. Якутск Алкены. Пропилен
Алкены. Пропилен Молярный объём газов
Молярный объём газов Тема урока: Сложные эфиры. Цель урока: Рассказать учащимся о строении, получении и свойствах сложных эфиров. Познакомить с примен
Тема урока: Сложные эфиры. Цель урока: Рассказать учащимся о строении, получении и свойствах сложных эфиров. Познакомить с примен Промышленные аварии с выбросом опасных химических веществ
Промышленные аварии с выбросом опасных химических веществ Шампунь для волосся
Шампунь для волосся  Товароведенье продовольственных товаров
Товароведенье продовольственных товаров Кислоты. Серная кислота-H₂SO₄
Кислоты. Серная кислота-H₂SO₄ Катализ в органическом синтезе
Катализ в органическом синтезе Валентність хімічних елементів
Валентність хімічних елементів Превращение (S)-бутанол-2 в другие соединения
Превращение (S)-бутанол-2 в другие соединения Двовимірний ямр. Основні принципи
Двовимірний ямр. Основні принципи Ароматические углеводороды
Ароматические углеводороды ВВЕДЕНИЕ В ЭКОЛОГИЧЕСКУЮ ХИМИЮ АНТРОПОГЕННОЕ ЗАГРЯЗНЕНИЕ ПРИРОДНОЙ СРЕДЫ ФАРМПОЛЛЮТАНТЫ
ВВЕДЕНИЕ В ЭКОЛОГИЧЕСКУЮ ХИМИЮ АНТРОПОГЕННОЕ ЗАГРЯЗНЕНИЕ ПРИРОДНОЙ СРЕДЫ ФАРМПОЛЛЮТАНТЫ  Соли и классы химических веществ
Соли и классы химических веществ Аттестационная работа. Методическая разработка занятия клуба «Я – исследователь» по теме «Волшебное вещество ‒ соль»
Аттестационная работа. Методическая разработка занятия клуба «Я – исследователь» по теме «Волшебное вещество ‒ соль» Колообіг нітрогену в природі
Колообіг нітрогену в природі Угольная кислота H2CO3
Угольная кислота H2CO3 Презентация по Химии "Свойства неньютоновских жидкостей" - скачать смотреть
Презентация по Химии "Свойства неньютоновских жидкостей" - скачать смотреть  Нитраты в продуктах
Нитраты в продуктах Излучение и поглощение света атомами. Виды спектров, спектральный анализ
Излучение и поглощение света атомами. Виды спектров, спектральный анализ Оборотные средства предприятия по переработке пластических масс и эластомеров
Оборотные средства предприятия по переработке пластических масс и эластомеров Acizii nucleici
Acizii nucleici