Содержание
- 2. Мета Розширити знання учнів про періодичну систему елементів; закріпити знання про хімічний елемент, хімічну символіку. Ознайомити
- 3. Кожен атом хімічного елемента має певну масу. Наприклад, маса атома найлегшого з хімічних елементів – атома
- 4. Зрозуміло, що подібними числами, навіть записаними у стандартному вигляді, користуватися незручно. Тому на практиці замість абсолютних
- 5. Нині за одиницю порівняння вибрано 1/12 частину маси атома Карбону. Вона називається атомною одиницею маси –
- 6. Зрозуміло, що відносна маса атома Карбону, виражена в атомних одиницях маси, дорівнює 12 а.о.м. Отже, Відносна
- 7. Відносна атомна маса позначається символом Ar. А – перша літера слова “атомна”, r – перша літера
- 8. Наприклад, маса атома Флуору F дорівнює 3,15481·10 -23г. Якщо її поділити на 1/12 маси атома Карбону,
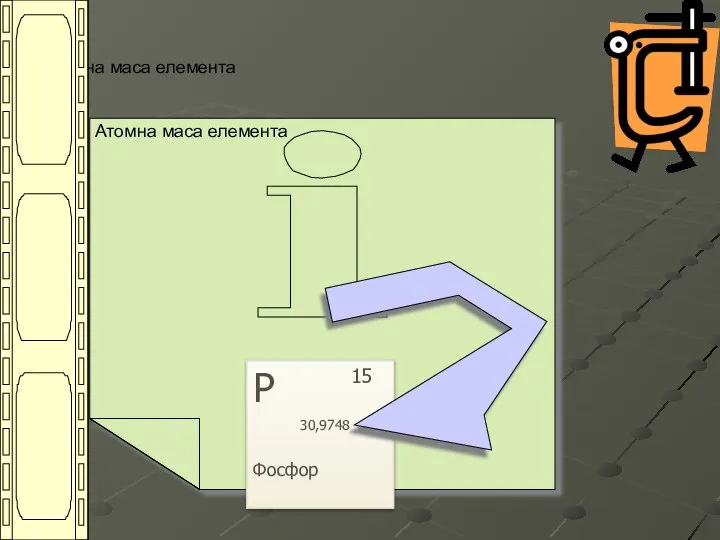
- 9. Атомна маса елемента Атомна маса елемента
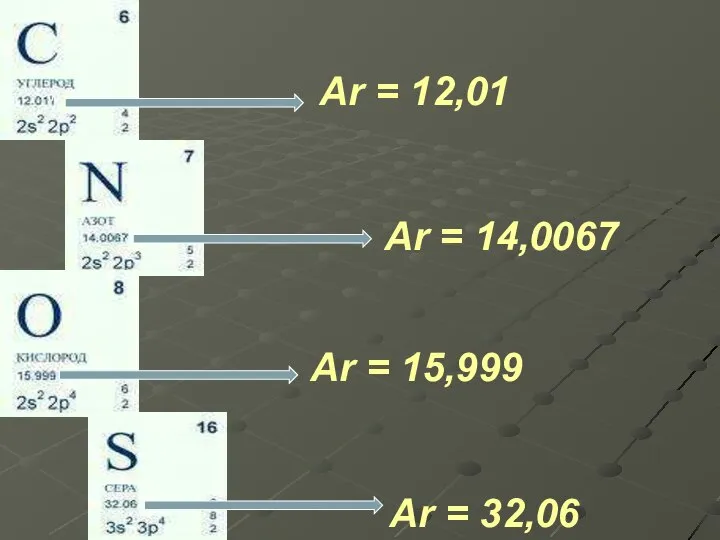
- 10. Ar = 12,01 Ar = 32,06 Ar = 14,0067 Ar = 15,999
- 11. Висновки Відносна атомна маса елемента – безрозмірна величина, що дорівнює відношенню маси атома даного елемента до
- 13. Скачать презентацию








 Окислительно-восстановительные процессы. Лекция 8
Окислительно-восстановительные процессы. Лекция 8 Составление уравнений ОВР
Составление уравнений ОВР Агрегатные состояния вещества
Агрегатные состояния вещества Химия в продуктах питания
Химия в продуктах питания Полимерные материалы и изделия. (Лекция 16)
Полимерные материалы и изделия. (Лекция 16) Презентация по Химии "КАРБОНОВЫЕ КИСЛОТЫ-СТРОЕНИЕ И НОМЕНКЛАТУРА" - скачать смотреть бесплатно
Презентация по Химии "КАРБОНОВЫЕ КИСЛОТЫ-СТРОЕНИЕ И НОМЕНКЛАТУРА" - скачать смотреть бесплатно Оксиды. Оксиды металлов и оксиды неметаллов
Оксиды. Оксиды металлов и оксиды неметаллов Алкены - Презентация по Химии_
Алкены - Презентация по Химии_ Катенаны. Ротаксаны (лекция 6)
Катенаны. Ротаксаны (лекция 6) Химия, 8 класс УЧИТЕЛЬ Краснова Оксана Владимировна
Химия, 8 класс УЧИТЕЛЬ Краснова Оксана Владимировна  Презентация по Химии "АЗОТНАЯ КИСЛОТА И ЕЕ СВОЙСТВА" - скачать смотреть бесплатно
Презентация по Химии "АЗОТНАЯ КИСЛОТА И ЕЕ СВОЙСТВА" - скачать смотреть бесплатно Гликогенді және кетогенді аминқышқылдары. Биологиялық рөлі
Гликогенді және кетогенді аминқышқылдары. Биологиялық рөлі Показатель активности водородных ионов. Лабораторная работа №4
Показатель активности водородных ионов. Лабораторная работа №4 Леция 1. Природа сил взаимодействия. Методы исследования комплексообразования:
Леция 1. Природа сил взаимодействия. Методы исследования комплексообразования: Історія відкриття періодичної системи хімічних елементів Д. І. Меделєєва
Історія відкриття періодичної системи хімічних елементів Д. І. Меделєєва Физические явления в химии НЕОРГАНИЧЕСКАЯ ХИМИЯ 8 КЛАСС УЧИТЕЛЬ ХИМИИ: Т.А. КОМАРОВА
Физические явления в химии НЕОРГАНИЧЕСКАЯ ХИМИЯ 8 КЛАСС УЧИТЕЛЬ ХИМИИ: Т.А. КОМАРОВА Химическое равновесие в газах и растворах
Химическое равновесие в газах и растворах Химия элементов VIA группы
Химия элементов VIA группы Физические и химические явления
Физические и химические явления Торжество периодического закона К 175-летию со дня рождения Д. И. Менделеева К 140-летию со дня создания Периодического закона
Торжество периодического закона К 175-летию со дня рождения Д. И. Менделеева К 140-летию со дня создания Периодического закона Электролитическая диссоциация(ЭД). Теория электролитической диссоциации (ТЭД)
Электролитическая диссоциация(ЭД). Теория электролитической диссоциации (ТЭД) Фосфаттардағы байланыс теориясы
Фосфаттардағы байланыс теориясы Ионная химическая связь
Ионная химическая связь Особенности строения, реакционной способности и методы синтеза карбоновых кислот и функциональных производных
Особенности строения, реакционной способности и методы синтеза карбоновых кислот и функциональных производных Откуда ты, химия ?
Откуда ты, химия ? Ненасыщенные углеводороды этиленового ряда
Ненасыщенные углеводороды этиленового ряда Как сохранить жизнь букету
Как сохранить жизнь букету Химиялық реакциялардың типтері
Химиялық реакциялардың типтері