Содержание
- 2. Цели урока: •Знать строение одноосновных карбоновых кислот, их определение, изомеры, гомологи, название по систематической номенклатуре. •Уметь
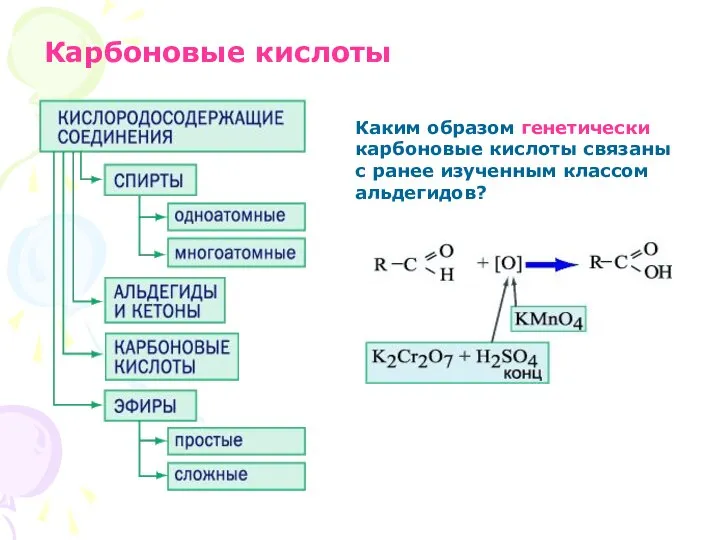
- 3. Карбоновые кислоты Каким образом генетически карбоновые кислоты связаны с ранее изученным классом альдегидов?
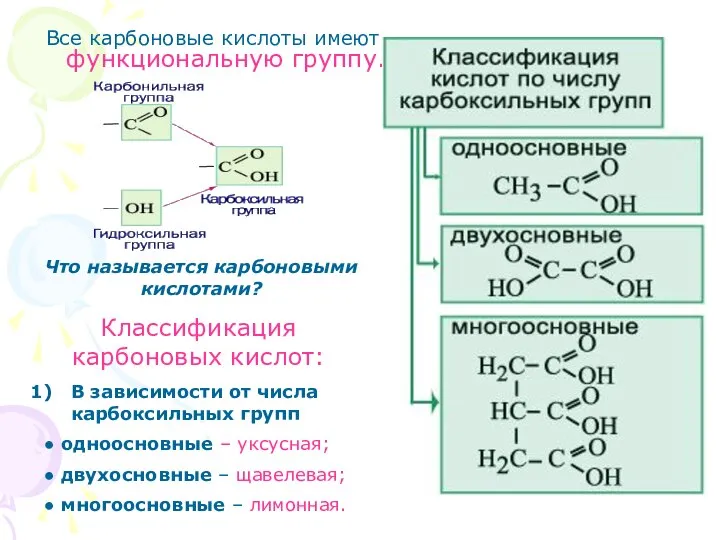
- 4. Все карбоновые кислоты имеют функциональную группу. Что называется карбоновыми кислотами? Классификация карбоновых кислот: В зависимости от
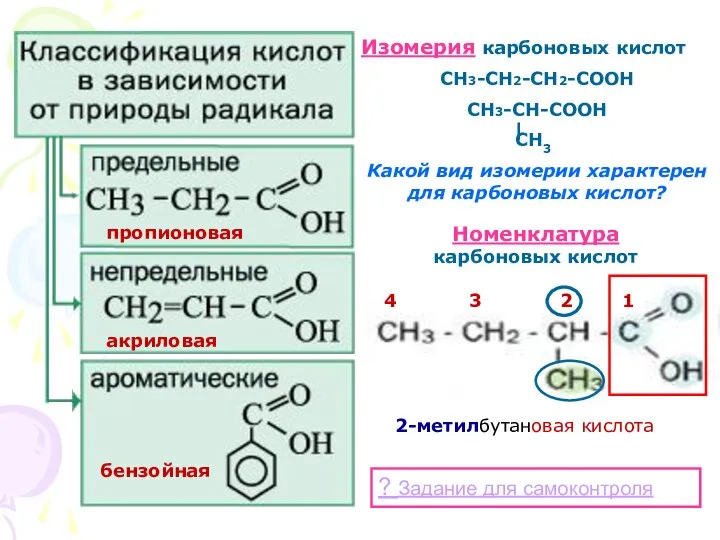
- 5. Изомерия карбоновых кислот СН3-СН2-СН2-СООН СН3-СН-СООН СН3 Какой вид изомерии характерен для карбоновых кислот? Номенклатура карбоновых кислот
- 6. Многие кислоты имеют исторически сложившиеся или тривиальные названия, связанные главным образом с источником их получения. Карбоновые
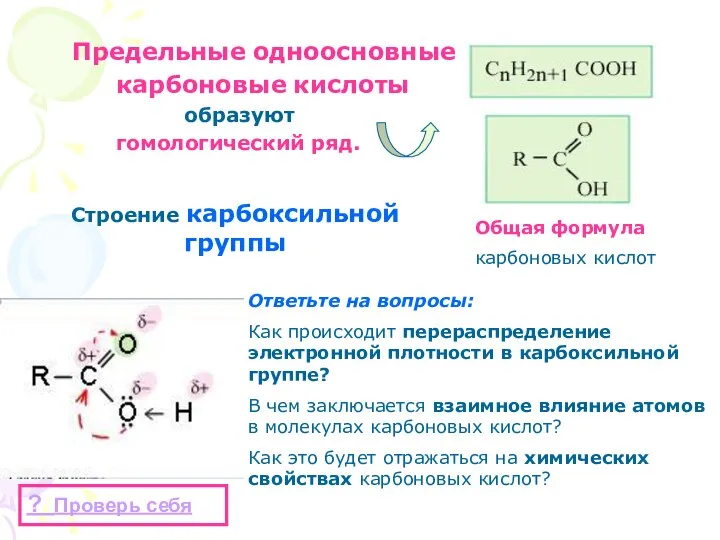
- 7. Предельные одноосновные карбоновые кислоты образуют гомологический ряд. Общая формула карбоновых кислот Строение карбоксильной группы Ответьте на
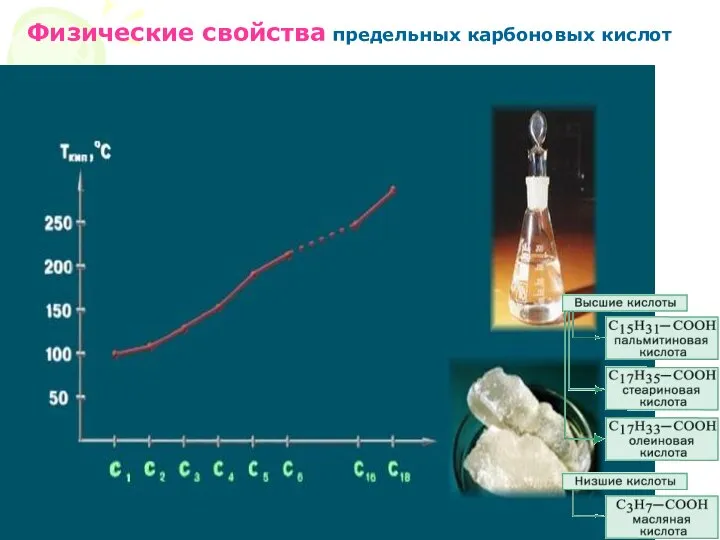
- 8. Физические свойства карбоновых кислот Физические свойства предельных карбоновых кислот
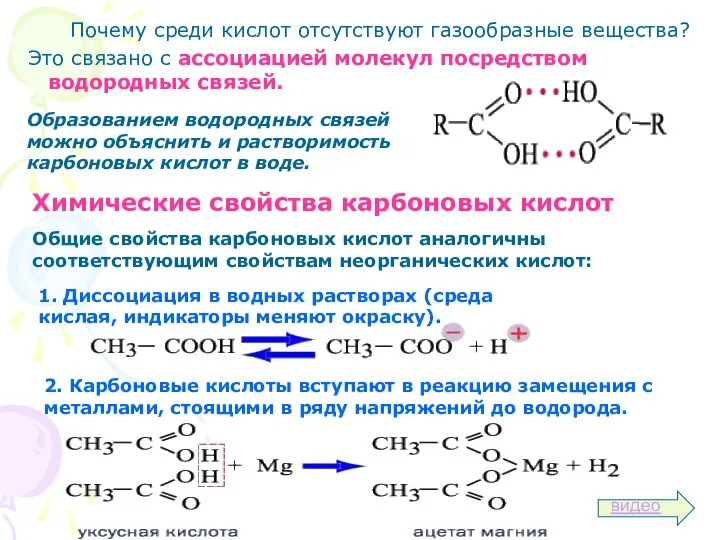
- 9. Почему среди кислот отсутствуют газообразные вещества? Это связано с ассоциацией молекул посредством водородных связей. Образованием водородных
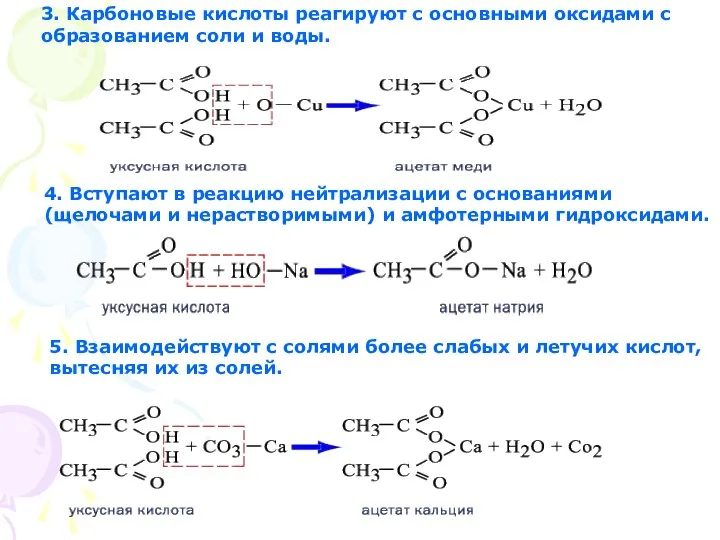
- 10. 3. Карбоновые кислоты реагируют с основными оксидами с образованием соли и воды. 4. Вступают в реакцию
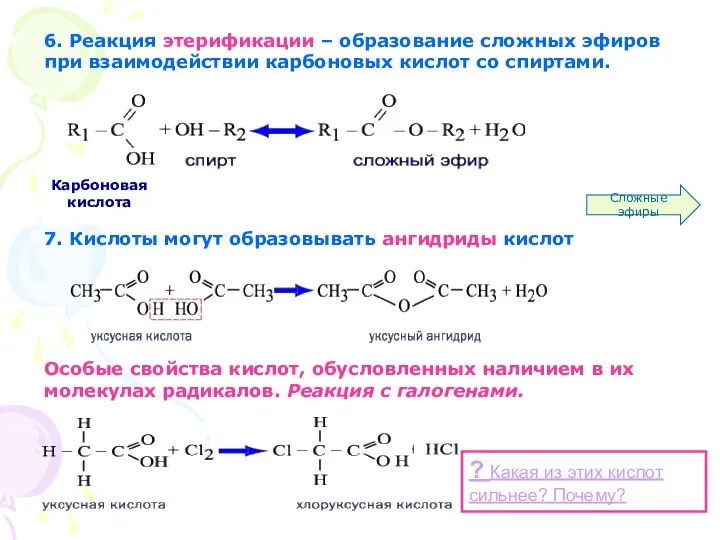
- 11. 6. Реакция этерификации – образование сложных эфиров при взаимодействии карбоновых кислот со спиртами. 7. Кислоты могут
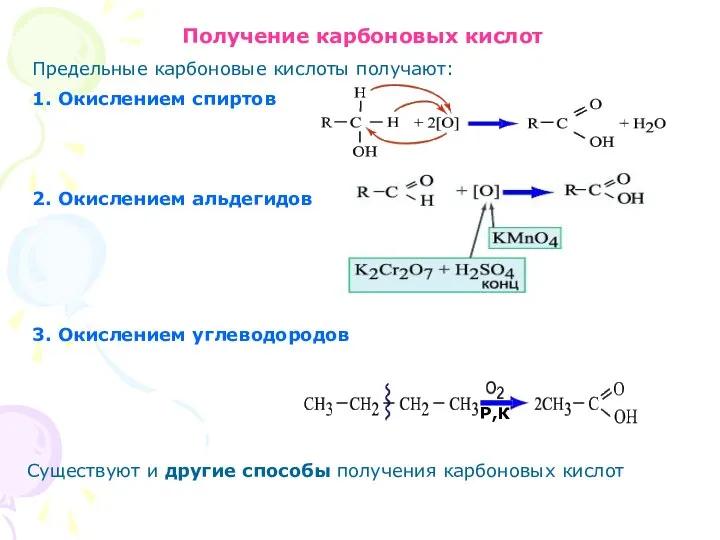
- 13. Получение карбоновых кислот Предельные карбоновые кислоты получают: 1. Окислением спиртов 2. Окислением альдегидов 3. Окислением углеводородов
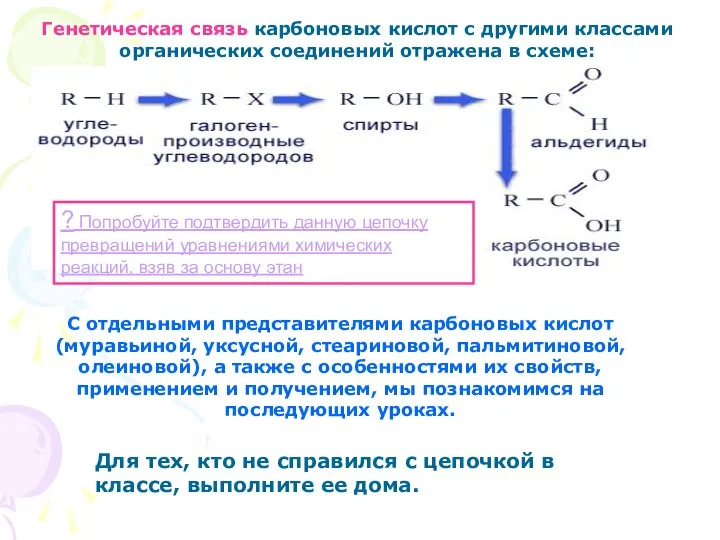
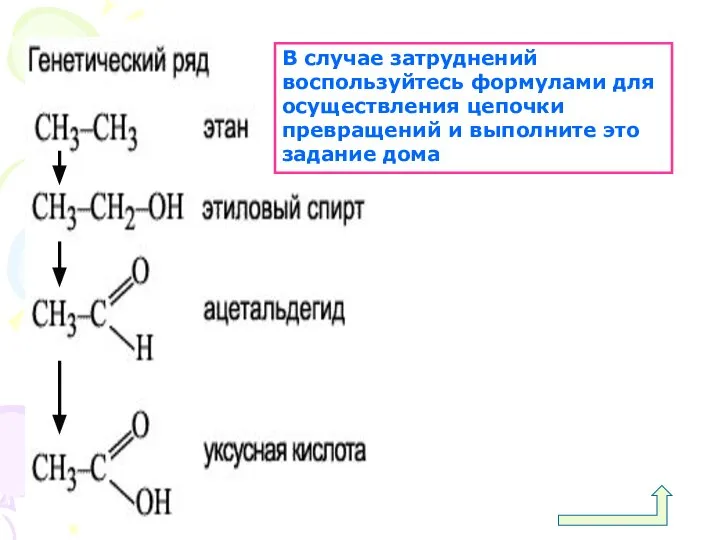
- 14. Генетическая связь карбоновых кислот с другими классами органических соединений отражена в схеме: ? Попробуйте подтвердить данную
- 15. Выводы: Карбоновыми кислотами называются органические вещества, молекулы которых содержат одну или несколько карбоксильных групп, соединенных с
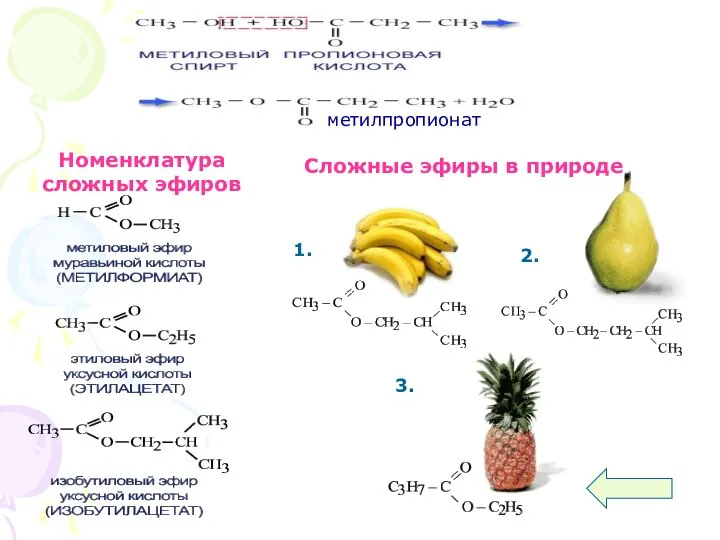
- 16. Номенклатура сложных эфиров Сложные эфиры в природе 1. 2. 3. метилпропионат
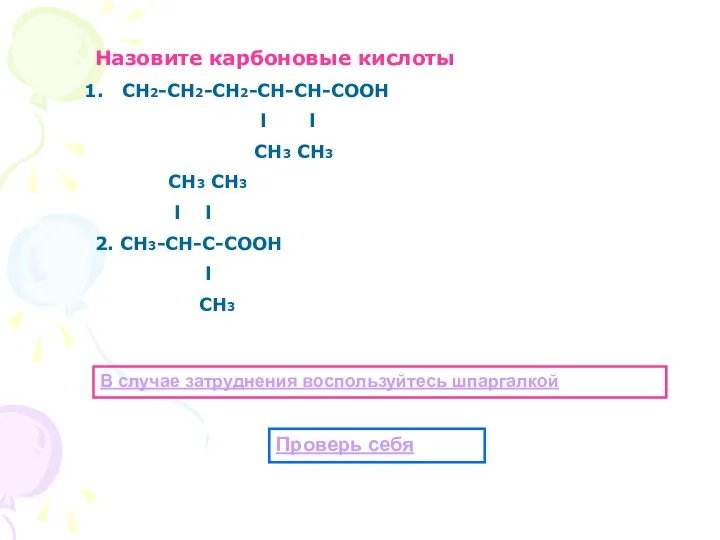
- 17. Назовите карбоновые кислоты СН2-СН2-СН2-СН-СН-СООН l l СН3 СН3 СН3 СН3 l l 2. СН3-СН-С-СООН l СН3
- 18. Проверь себя: 3,4 – диметилгексановая кислота 2,2,3 – триметилбутановая кислота
- 19. В случае затруднений воспользуйтесь формулами для осуществления цепочки превращений и выполните это задание дома
- 20. Для определения названия кислоты в соответствии с номенклатурой IUPAC нужно придерживаться следующего порядка: Главную цепь выбирают
- 21. Ответы на вопросы ● Электронная плотность в карбонильной группе (особенно σ-связи) смещена в сторону кислорода, как
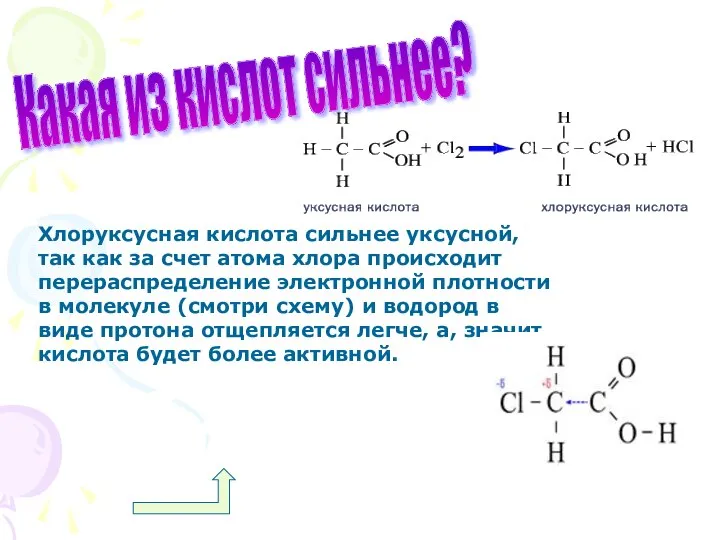
- 22. Какая из кислот сильнее? Хлоруксусная кислота сильнее уксусной, так как за счет атома хлора происходит перераспределение
- 23. Проверь свои знания по карбоновым кислотам Реши задачу Реши кроссворд
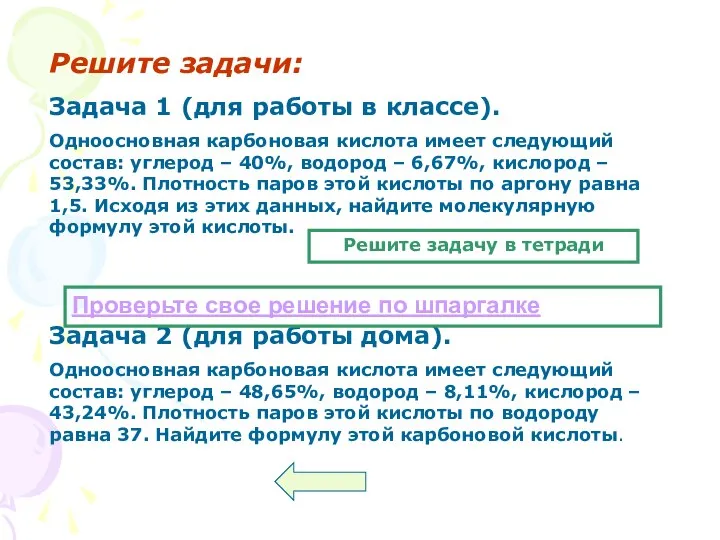
- 24. Решите задачи: Задача 1 (для работы в классе). Одноосновная карбоновая кислота имеет следующий состав: углерод –
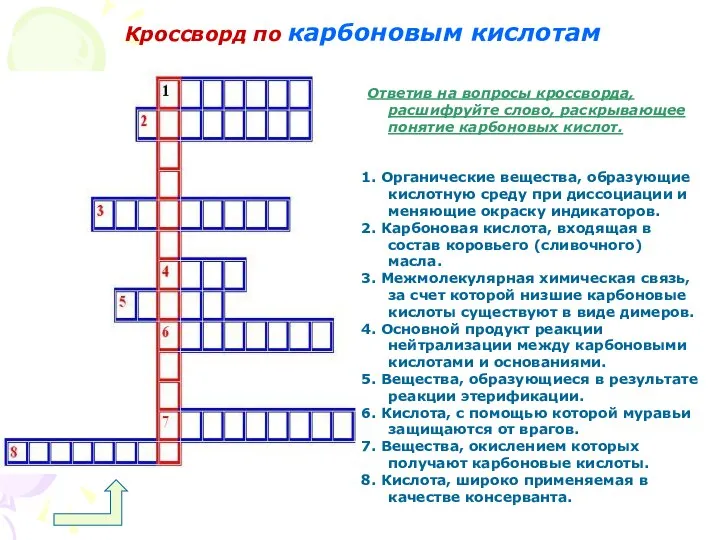
- 25. Кроссворд по карбоновым кислотам Ответив на вопросы кроссворда, расшифруйте слово, раскрывающее понятие карбоновых кислот. 1. Органические
- 26. Решение задачи 1. По данному образцу реши дома задачу 2. Простейшая формула: СН2О Находим истинную формулу:
- 27. Домашнее задание Глава 8, §2; Решить задачу №2 со слайда; Выполнить цепочку превращений со слайда (для
- 29. Скачать презентацию









 Презентация по Химии "кристаллические решетки." - скачать смотреть бесплатно_
Презентация по Химии "кристаллические решетки." - скачать смотреть бесплатно_ Показники якості води Онуфреїв Оленка Слухач МАН Секція біологія.
Показники якості води Онуфреїв Оленка Слухач МАН Секція біологія. Оксид азота(2) NO
Оксид азота(2) NO Классификация кислот
Классификация кислот Жидкостная хроматография
Жидкостная хроматография Воздух. Постоянные компоненты воздуха
Воздух. Постоянные компоненты воздуха Тест
Тест Диффузия золота и свинца
Диффузия золота и свинца Синтетические волокна (продолжение)
Синтетические волокна (продолжение) Основи, їх склад, назви, класифікація.
Основи, їх склад, назви, класифікація.  Презентация по Химии "Химия нефти" - скачать смотреть бесплатно
Презентация по Химии "Химия нефти" - скачать смотреть бесплатно Альдегиды и кетоны
Альдегиды и кетоны Электронные представления в химии
Электронные представления в химии Методы выращивания GaAs. Сравнение
Методы выращивания GaAs. Сравнение Химия - основы общей химии (теория)
Химия - основы общей химии (теория) Общие закономерности адсорбции из растворов на поверхности твердого тела. Лекция 05
Общие закономерности адсорбции из растворов на поверхности твердого тела. Лекция 05 Аргентум, или серебро
Аргентум, или серебро Презентация Воздух, его состав и значение.
Презентация Воздух, его состав и значение.  Получение Н2, О2, щелочей
Получение Н2, О2, щелочей Фосфор Материал для повторения и подготовки к ГИА Учитель химии МОУ «Гимназия №1» г. Саратов Шишкина И.Ю.
Фосфор Материал для повторения и подготовки к ГИА Учитель химии МОУ «Гимназия №1» г. Саратов Шишкина И.Ю.  Магний. Магний алудың электролиттік жолы. Магний алудың термиялық жолдары
Магний. Магний алудың электролиттік жолы. Магний алудың термиялық жолдары Калий. Общая информация
Калий. Общая информация ОКИСЛИТЕЛЬНО – ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ Элективный специальный курс углублённого изучения темы для учащихся 11 классов естеств
ОКИСЛИТЕЛЬНО – ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ Элективный специальный курс углублённого изучения темы для учащихся 11 классов естеств Аминокислотный спектр плазмы крови у пациентов с острым миелобластным лейкозом
Аминокислотный спектр плазмы крови у пациентов с острым миелобластным лейкозом Гелий
Гелий Химия. Основные понятия и законы
Химия. Основные понятия и законы Презентация по Химии "Нафта" - скачать смотреть бесплатно
Презентация по Химии "Нафта" - скачать смотреть бесплатно Сероводород. Польза или вред
Сероводород. Польза или вред