Содержание
- 2. Функції білків Каталітична – ферменти Пластична – структурні білки Регуляторна – гормони, ферменти Скорочувальна – білки
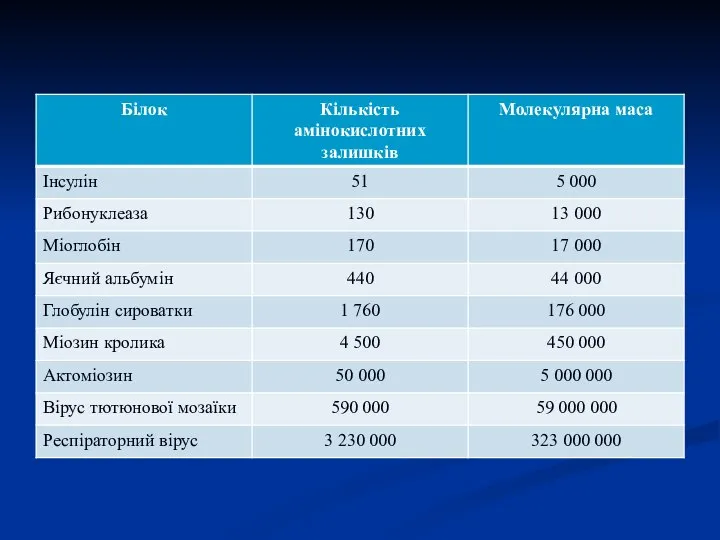
- 3. Вміст білків у тканинах, % Тварини Організм – 18-21 М'язи – 19-23 Печінка – 18-19 Нирки
- 4. Елементарний склад білків, % Карбон – 49-55 Оксиген – 21-23 Нітроген – 16,5 Гідроген – 6-8
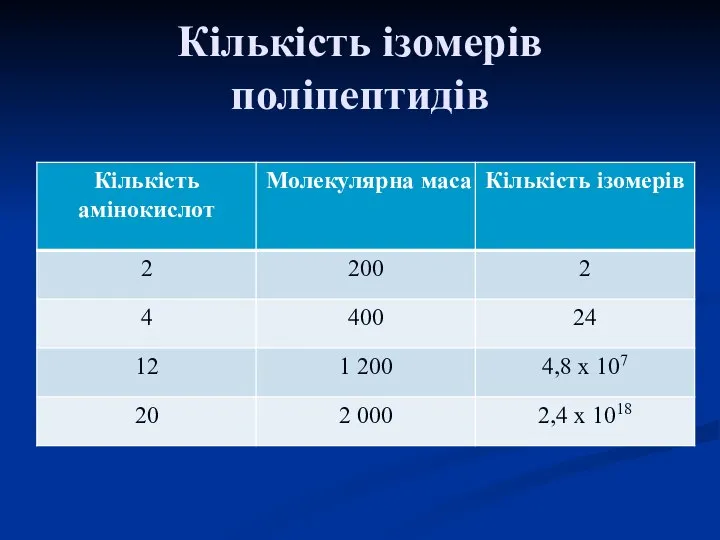
- 6. Кількість ізомерів поліпептидів
- 7. Структура білків Пептидні ланцюги містять десятки, сотні та тисячі амінокислотних залишків, з'єднаних міцними пептидними зв'язками. За
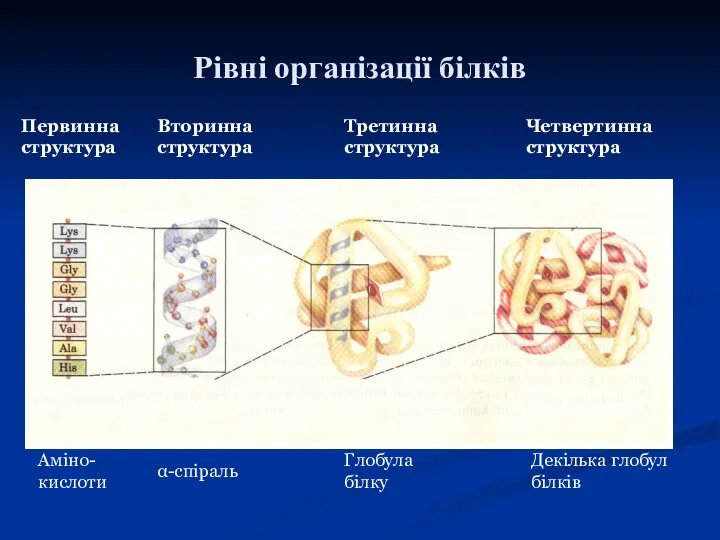
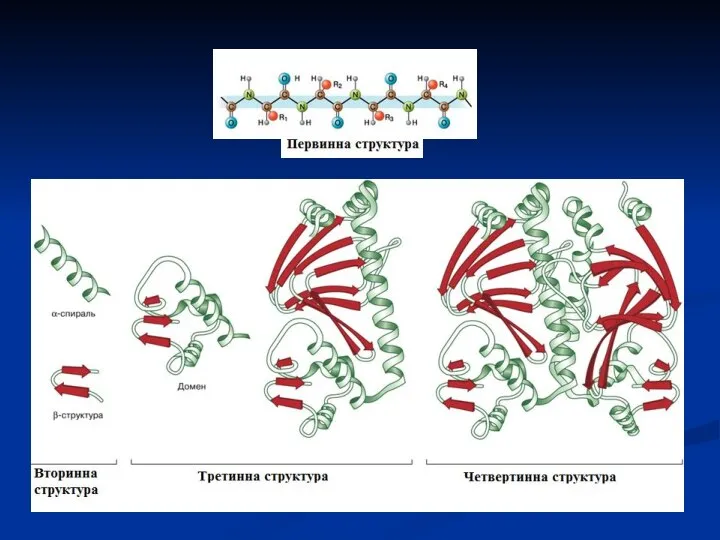
- 8. Первинна структура Вторинна структура Аміно- кислоти α-спіраль Третинна структура Четвертинна структура Глобула білку Декілька глобул білків
- 9. • Первинна структура: порядок розташування амінокислот у поліпептидному ланцюзі білка (зв'язки – ковалентні пептидні). • Вторинна
- 11. Первинна структура білків Класифікація амінокислот: 1. Структурна. - циклічні: а) гетероциклічні б) ароматичні - ациклічні: а)
- 12. На даний час у природі виявлено більше 300 різних АК. В організмі людини і тварин міститься
- 13. Амінокислоти Замінні Гліцин Аланін Серин Цистеїн Аспарагінова кислота Глутамінова кислота Тирозин Пролін Аспарагін Глутамін Незамінні Треонін
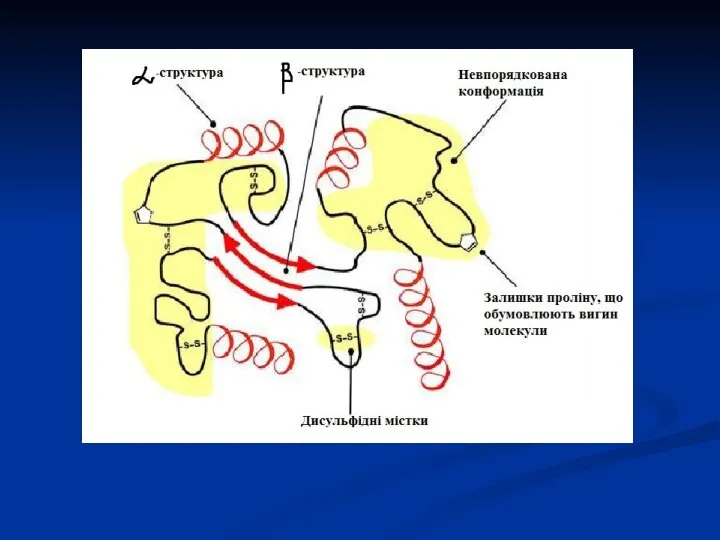
- 14. Вторинна структура білків α-спіраль β-структура (складчастий шар або лист) β-вигин Отже, вторинна структура – це форма
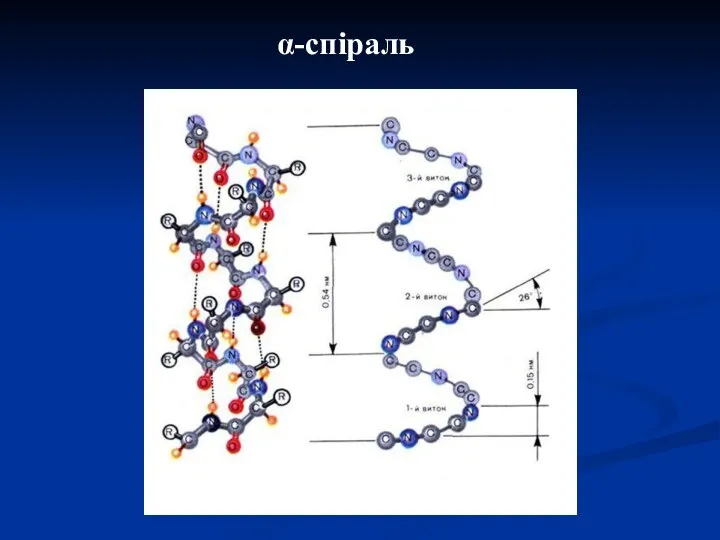
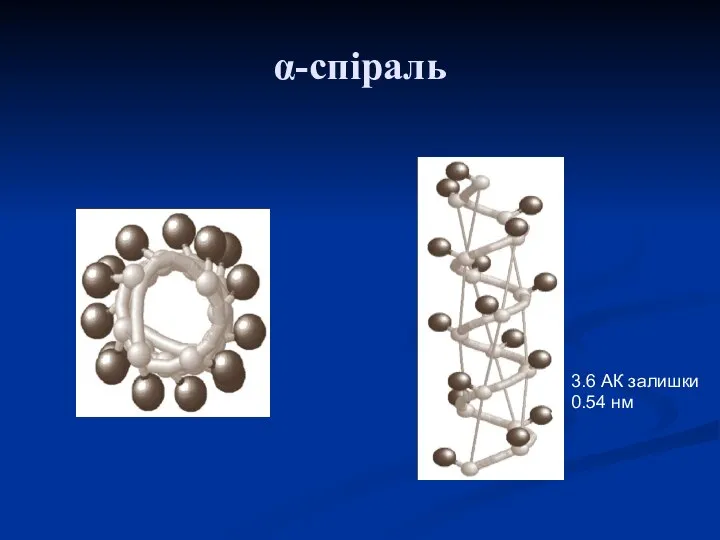
- 15. α-спіраль
- 16. Американські вчені Л. Полінг та Р. Корі (1950 р.) установили, що для пептидів найвигіднішою конформацією є
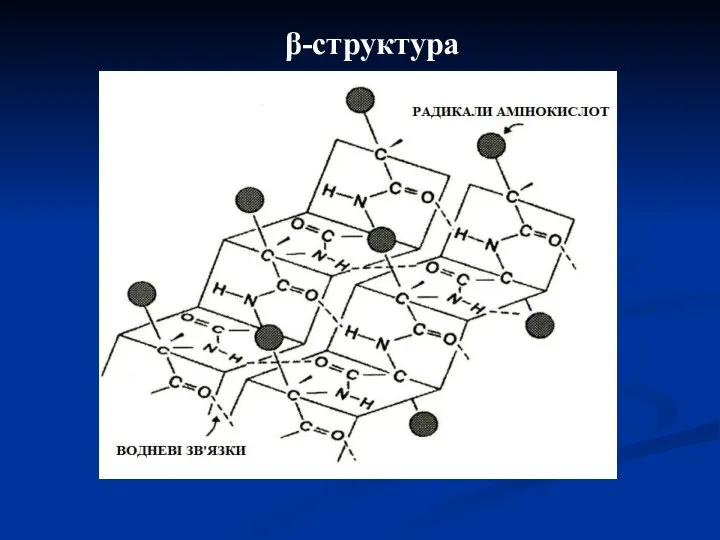
- 17. β-структура
- 18. Цей різновид вторинної структури має слабко вигнуту конфігурацію поліпептидного ланцюга. Вона формується за допомогою міжпептидних водневих
- 19. α-спіраль 3.6 АК залишки 0.54 нм
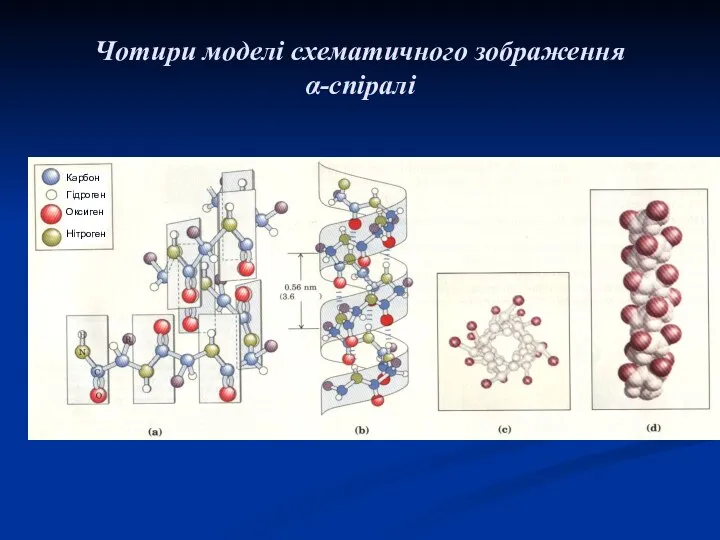
- 20. Чотири моделі схематичного зображення α-спіралі Карбон Гідроген Оксиген Нітроген
- 21. β-лист
- 22. Надвторинна структура і доменні білки Методом рентгеноструктурного аналізу доведене існування ще двох рівней організації білкової молекули:
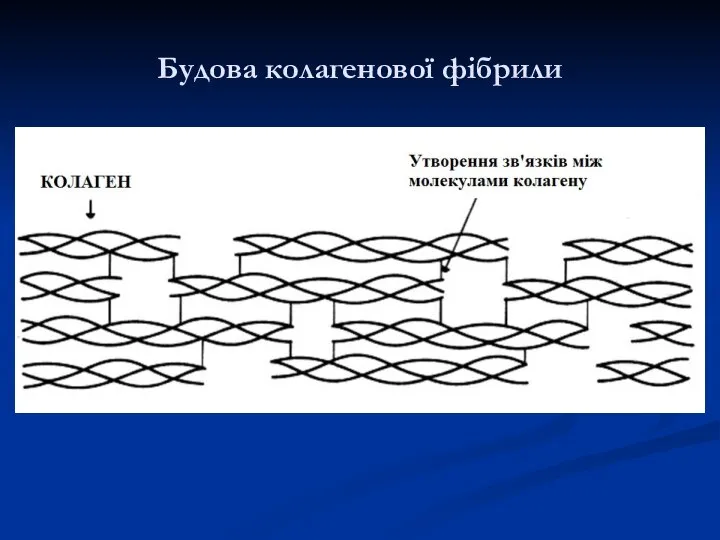
- 23. Плоскі кільця проліну і гідроксипроліну, які регулярно чергуються вздовж ланцюга, як і міжланцюгові зв'язки між α-ланцюгами
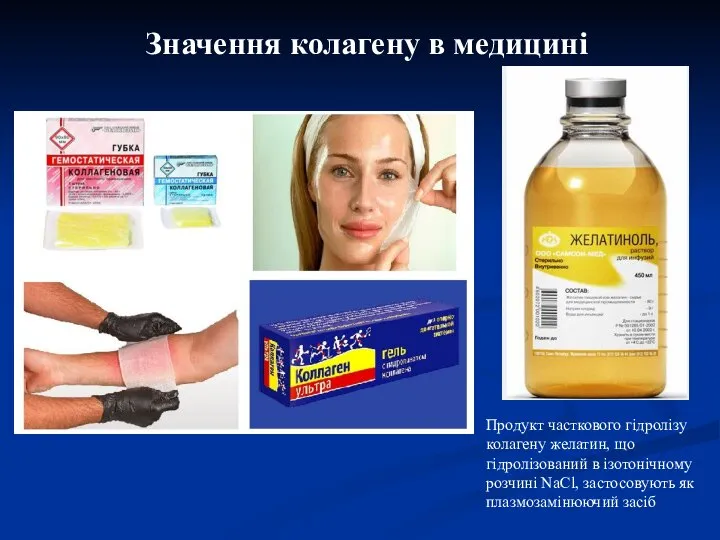
- 24. Значення колагену в медицині Продукт часткового гідролізу колагену желатин, що гідролізований в ізотонічному розчині NaCl, застосовують
- 25. Доменні білки У молекулі доменних білків ділянки, що містять фрагменти вторинної структури (α-спіралі, β-структури та їх
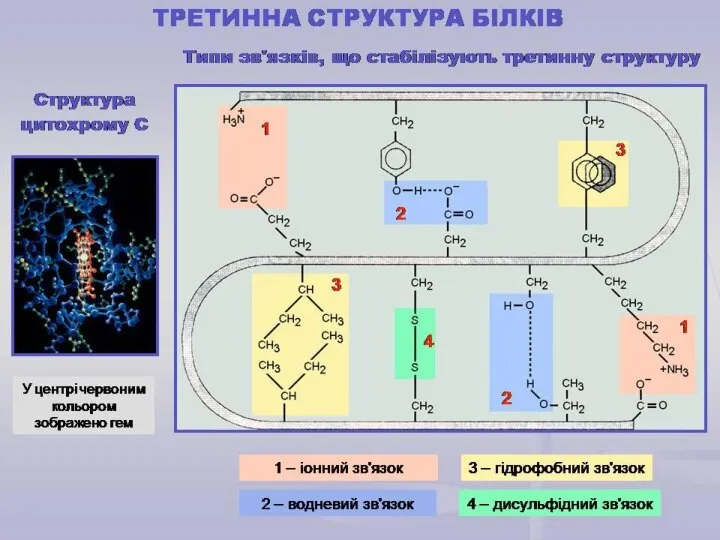
- 26. Третинна структура білків Це спосіб укладання поліпептидного ланцюга з елементами вторинної структури у просторі, який досягається
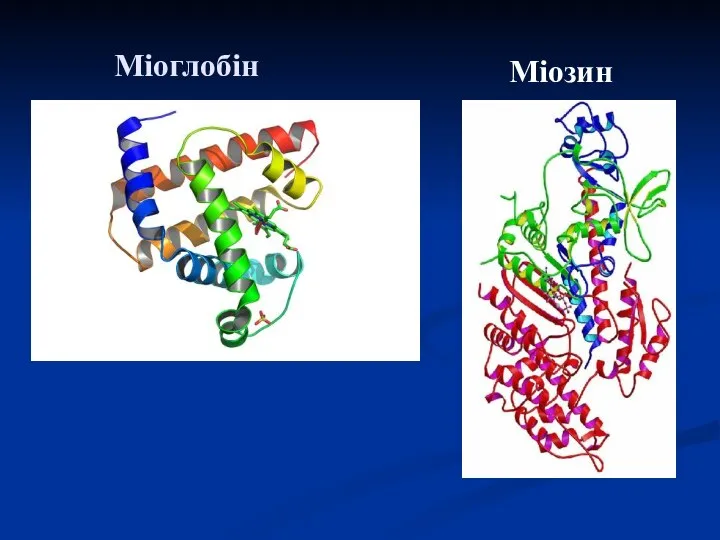
- 29. Міоглобін Міозин
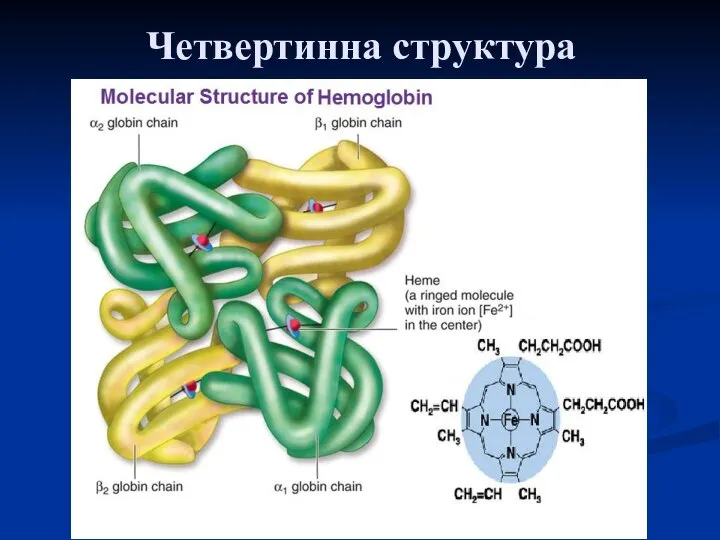
- 30. Четвертинна структура
- 31. Класичним прикладом білків із четвертинною структурою є гемоглобін, молекула якого побудована з 4 субодиниць: двох α-
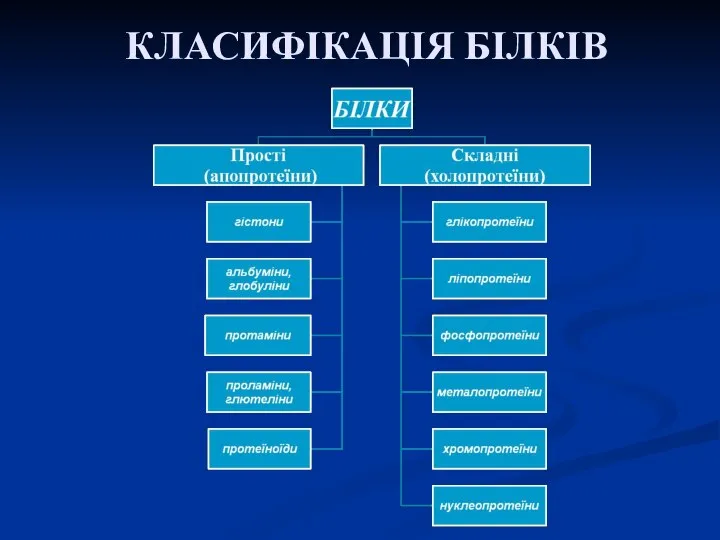
- 33. КЛАСИФІКАЦІЯ БІЛКІВ
- 34. Альбуміни Молекулярна маса – 35-70 тис. Да ІЕТ – 4,7 (кислі) Багато лейцину (15%), мало амінокислоти
- 35. Глобуліни Молекулярна маса – 0,9-1,5 млн. Да ІЕТ - 5,5 – 7,3 Містять більше гліцину (≈
- 36. Гістони Білки ядра. Маса – 12 – 30 тис. Да ІЕТ – 8 – 9 (основні,
- 37. Протаміни Молекулярна маса – до 12 тис. Да Вміст диаміномонокарбонових кислот (аргінін, лізин) близько 80%, розчиняються
- 38. Білки рослинного походження Глютеліни Білки зерен. ІЕТ - 6-8 До їх складу входить велика кількість глутамінової
- 39. Проламіни Білки зерен злаків. Маса – 28 -50 тис. Да. ІЕТ – 4-5. До складу входить
- 40. Протеїноїди (склеропротеїни) Білки опорних тканин (кістки, хрящі, сухожилля, шерсть, копита). Нерозчинні у воді, розчинах солей, кислот
- 41. Клітини Поперечный разрез волоса Макрофібрила Мікрофібрила КЕРАТИН Протофібрила α-спіраль Структура волосини
- 42. Будова колагенової фібрили
- 43. Складні протеїни Простий білок + небілкова речовина (простетична група) а) нуклеопротеїни (простий білок + нуклеїнова кислота)
- 44. Нуклеопротеїни ↓ складаються з ↓ Протеїни Нуклеїнові кислоти гістони ДНК негістонові білки (ДезоксирибоНуклеоПротеїни – ДНП) протаміни
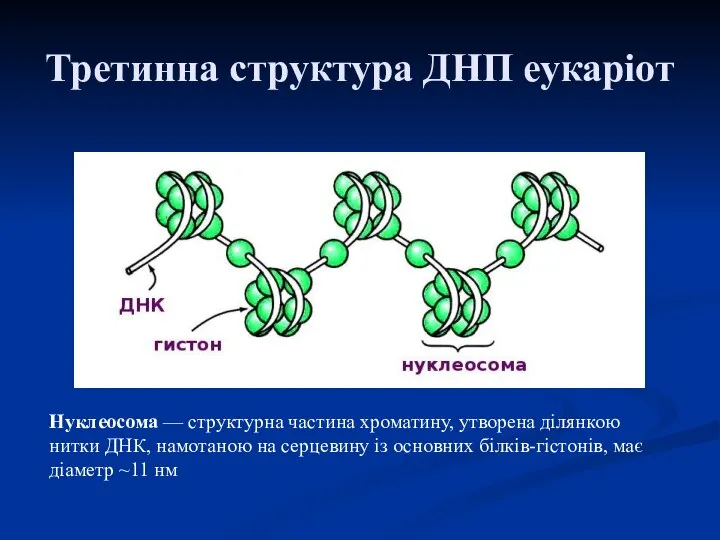
- 45. Третинна структура ДНП еукаріот Нуклеосома — структурна частина хроматину, утворена ділянкою нитки ДНК, намотаною на серцевину
- 46. Хромопротеїни ↓ ↓ Протеїн Небілкова речовина, що надає забарвлення а) гемвмісні - гемоглобін - міоглобін -
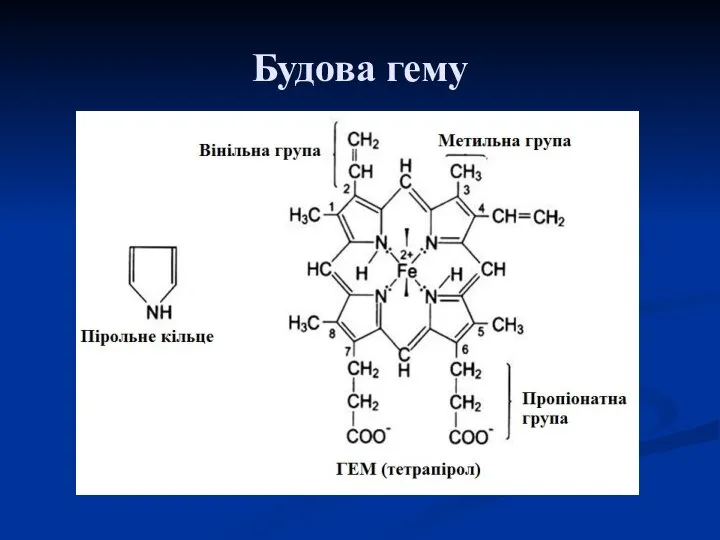
- 47. Будова гему
- 48. Гемоглобін Структура розшифрована Дж. Кендрью і М. Перутц (Нобелевська премія 1962р.) Маса – 67 - 70
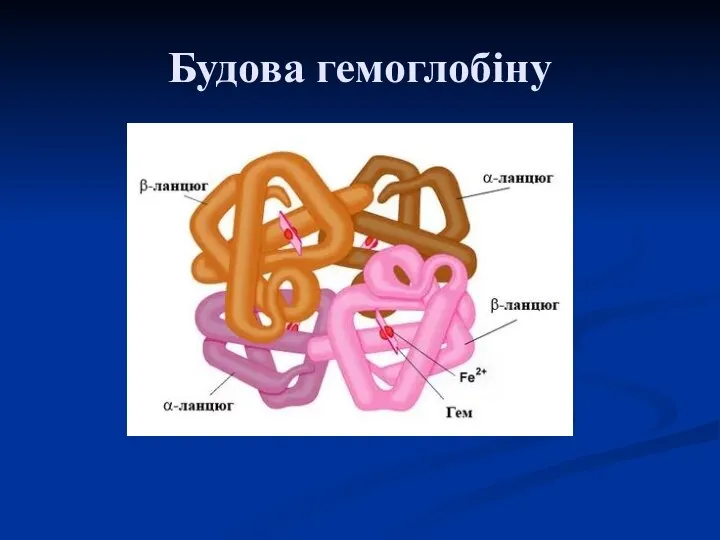
- 49. Будова гемоглобіну
- 50. Види гемоглобіну HbО2 - оксигемоглобін (Fe2+); HbСО2 - карбгемоглобін (Fe2+); HbСО - карбоксигемоглобін (Fe3+); HbF3+ -
- 51. Міоглобін Велика кількість міститься в червоних скелетних м'язах та міокарді. Маса 17 тис., складається з одного
- 52. Третинна структура міоглобіну
- 53. Гемвмісні ферменти Цитохроми Переносники електронів у дихальному ланцюгу мітохондрій. Розрізняють сімейства (групи): а, b, с, а
- 54. Цитохромоксидаза (цитохром а3) Кінцевий компонент дихального ланцюгу. Переносить електрони на кисень. Маса – 12 -14 тис.
- 55. Фосфопротеїни (Білок + залишок фосфатної кислоти) Представники: - Казеїн (молока) - Ововітелін жовтка - Фосвітин -
- 56. Глікопротеїни (простий білок + вуглевод) Білкова частина складає 80 - 90% від м.м. молекул Вуглеводний компонент
- 57. Функції глікопротеїнів Фактори згортання крові – протромбін, фібриноген. Змащувальні та захисні речовини – муцини, слизові секрети.
- 58. Протеоглікани Якщо білкова частина складає менше 50% маси молекули, а вуглеводна частина більше 50% - це
- 59. Протеоглікани Протеоглікани (мукополісахариди, глікозаміноглікани) – високомолекулярні вуглеводно-білкові сполуки. Утворюють основну масу міжклітинного матриксу сполучної тканини. Складають
- 60. Ліпопротеїни (простий білок + ліпід) Ліпіди у водному середовищі (а значить, і в крові) нерозчинні, тому
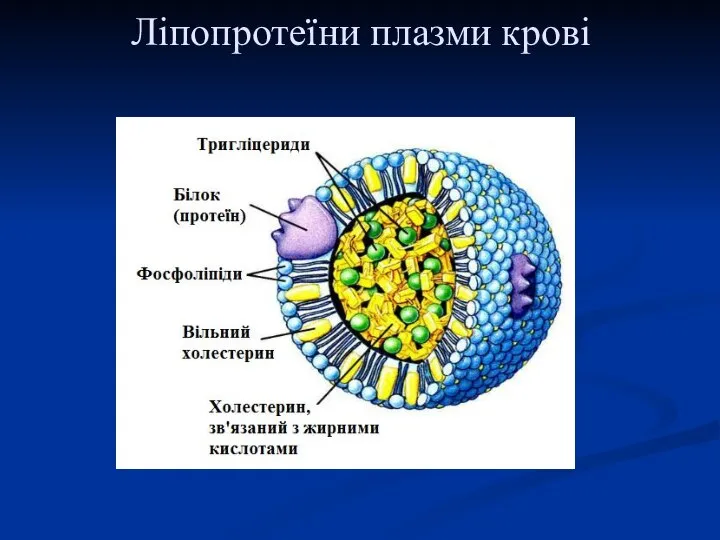
- 61. Ліпопротеїни плазми крові
- 62. Ліпопротеїни В організмі синтезуються наступні типи ліпопротеїнів: 1. хіломікрони (ХМ), 2. ліпопротеїни дуже низької щільності (ЛПДНЩ)
- 64. Скачать презентацию










































 Химическая кинетика, химическое равновесие и катализ
Химическая кинетика, химическое равновесие и катализ Водородная связь
Водородная связь Взаимосвязь между классами неорганических веществ
Взаимосвязь между классами неорганических веществ Адсорбция из раствора на твердом адсорбенте
Адсорбция из раствора на твердом адсорбенте Сахароза
Сахароза Химические реакции. Скорость химической реакции
Химические реакции. Скорость химической реакции Матричные биосинтезы
Матричные биосинтезы Химические вещества и материалы в живописи
Химические вещества и материалы в живописи Патология углеводного обмена. (Тема 4)
Патология углеводного обмена. (Тема 4) ХІМІЯ В КОСМЕТИЦІ
ХІМІЯ В КОСМЕТИЦІ  Альдегиды и кетоны
Альдегиды и кетоны Будова атома
Будова атома Пищевые добавки
Пищевые добавки Сорбционные процессы
Сорбционные процессы Количество вещества
Количество вещества Резина и каучук
Резина и каучук Перспективы использования оксигенатов в моторных топливах
Перспективы использования оксигенатов в моторных топливах Природа активності та кислотності цеолітних каталізаторів
Природа активності та кислотності цеолітних каталізаторів ,
,  Алюминий, его физические и химические свойства
Алюминий, его физические и химические свойства Газовые смеси
Газовые смеси Нанопористые материалы
Нанопористые материалы Презентация по химии Металлы
Презентация по химии Металлы  Применение солей
Применение солей  Основные классы химических соединений
Основные классы химических соединений Нефть и способы ее переработки
Нефть и способы ее переработки Высокомолекулярные соединения (ВМС)
Высокомолекулярные соединения (ВМС) Газы, применяемые при сварке
Газы, применяемые при сварке