Содержание
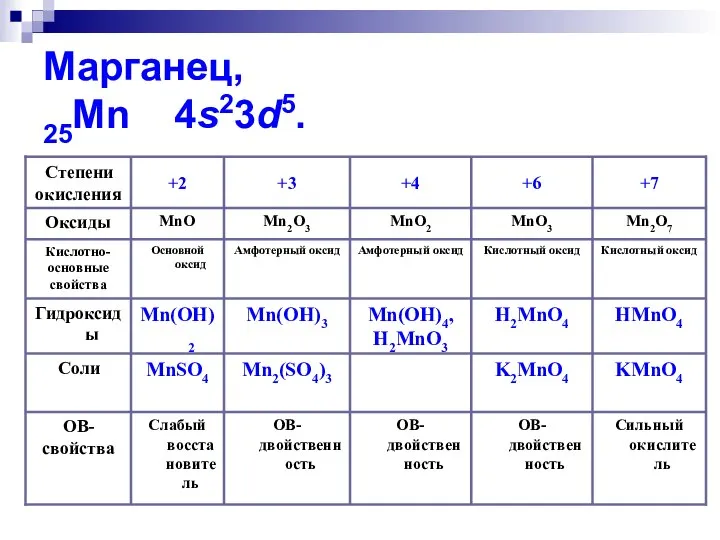
- 2. Марганец, 25Mn 4s23d5.
- 3. Основные и восстановительные свойства Mn2+ MnO+H2SO4+5H2O=[Mn(H2O)6]SO4 MnSO4+2NaOH=Mn(OH)2↓+Na2SO4 Mn(OH)2+O2+H2O→Mn(OH)4→MnO2↓+H2O Качественная реакция на Mn2+ : 2Mn(NO3)2+5NaВiO3+16HNO3= 2HMnO4+5Вi(NO3)3+5NaNO3+7H2O фиолетовое
- 4. MnO2 - окислительно-восстановительная двойственность: 2MnO2+3NaВiO3+12HNO3 => 2HMnO4+3Вi(NO3)3+3NaNO3+5H2O восстановительные свойства; MnO2+4HCl=>MnCl2+Cl2+2H2O окислительные свойства.
- 5. KМnO4 - сильный окислитель при отравлениях обезвреживание идет за счет окислительно-восстановительной реакции: 2KMnO4+5H2O2+6CH3COOH => 2Mn(CH3COO)2+2CH3COOK+5O2+8H2O
- 6. Зависимость ОВР от pH: в кислой среде ϕ0MnO4-/Mn2+ = 1,52В 2KMnO4+5K2SO3+3H2SO4=2MnSO4+6K2SO4+3H2O в нейтральной среде ϕ0MnO4-/MnO2 =
- 7. Mn in vivo В организме человека содержится около 12мг марганца, ω(Mn) = 10-5 %, микроэлемент. Топография:
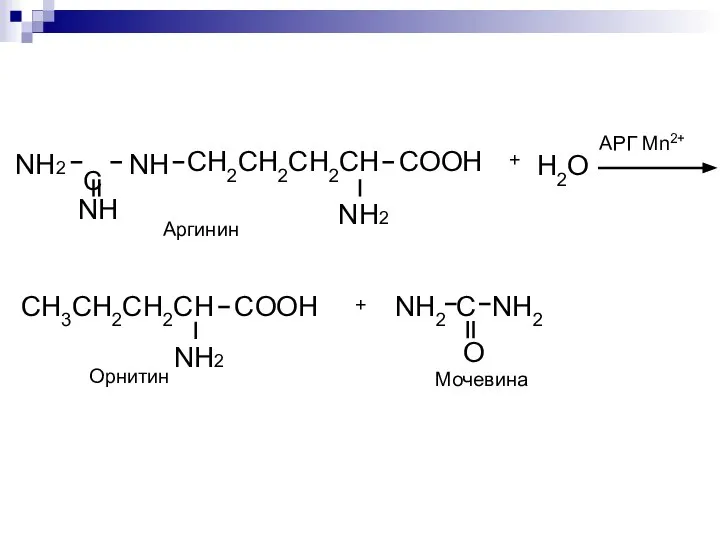
- 8. Биороль В составе фермента аргиназы марганец участвует в цикле мочевинообразования. На последнем этапе синтеза мочевины аргиназа
- 9. АРГ Mn2+
- 10. Биороль В составе фосфоглюкомутазы участвует в углеводном обмене. фосфоглюкомутаза Глюкоза – 1 – фосфат Глюкоза –
- 11. Установлено влияние марганца на образование гемоглобина. Mn+2, подобно Mg+2, в составе активных форм АТФ и АДФ
- 12. Избыток и недостаток: Суточная потребность 5-7мг. Марганец содержится в печени, красной свекле, томатах, моркови, сое, горохе,
- 13. Лекарственные препараты: MnCl2, MnSO4 в сочетании с солями железа, меди, кобальта используют для лечения анемии и
- 14. Железо 26Fe 4s23d6 с.о. +2 и +3 координационное число в комплексных соединениях 6.
- 15. Химические превращения (Fe2+) Fe+2HCl=FeCl2+H2↑; FeCl2+2NaOH=Fe(OH)2↓+2NaCl; Fe(OH)2 проявляет основные и восстановительные свойства: Fe(OH)2+H2SO4=FeSO4+2H2O; Fe(OH)2+O2+H2О→Fe(OH)3. Fe(OH)2 разлагается при
- 16. Химические превращения (Fe3+) Fe(OH)3 проявляет амфотерные свойства, т.е. реагирует и с кислотами, и с основаниями: Fe(OH)3+3HCl=FeCl3+3H2O;
- 17. Соли Fe3+ легко гидролизуются с образованием малорастворимых основных солей, поэтому для перорального приема назначают препараты Fe2+:
- 18. Fe in vivo Содержание железа в организме около 5г, ω(Fe) ≈ 10-2 %, микроэлемент. Топография: большая
- 19. Биороль Транспортные биокомплексы: а) гемоглобин (Hb) обратимо связывает кислород и переносит его от лёгких к тканям:
- 20. б) миоглобин (Mb) осуществляет обратимый перенос кислорода в мышцах: [MbFe+2] + O2 [MbFe+2O2]; дезоксиформа оксиформа
- 21. в) трансферрин – железосодержащий белок, легко проходит через клеточную мембрану и доставляет Fe+3 от ферритина в
- 22. Ферритин – является аккумуляторным биокластером, в его полости депонируется Fe+3, которое организм использует по мере необходимости.
- 23. Ферментативные комплексы железа: а) цитохромы(ЦХ) катализируют перенос электронов в дыхательной цепи за счёт изменения степени окисления
- 24. б) каталаза, активный центр которой содержит Fe+3, ускоряет процесс разложения токсичного пероксида водорода: каталаза 2Н2О2 2Н2О
- 25. Избыток и недостаток Суточная потребность железа составляет 1мг, но из пищи усваивается только 10-20%, поэтому должно
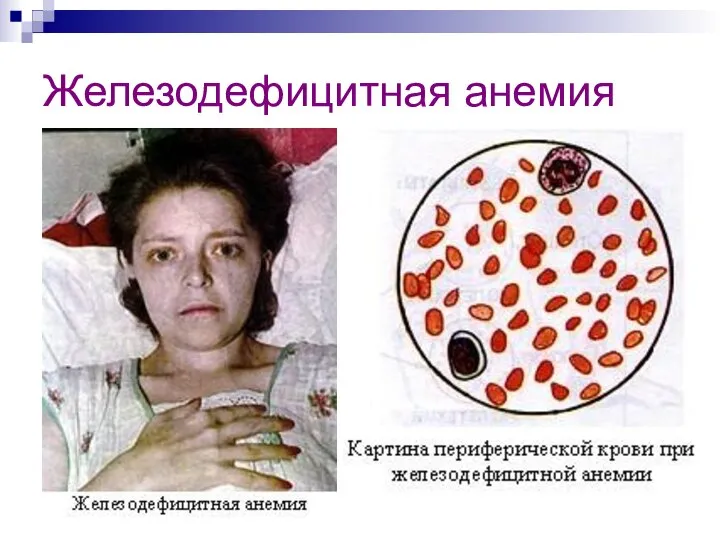
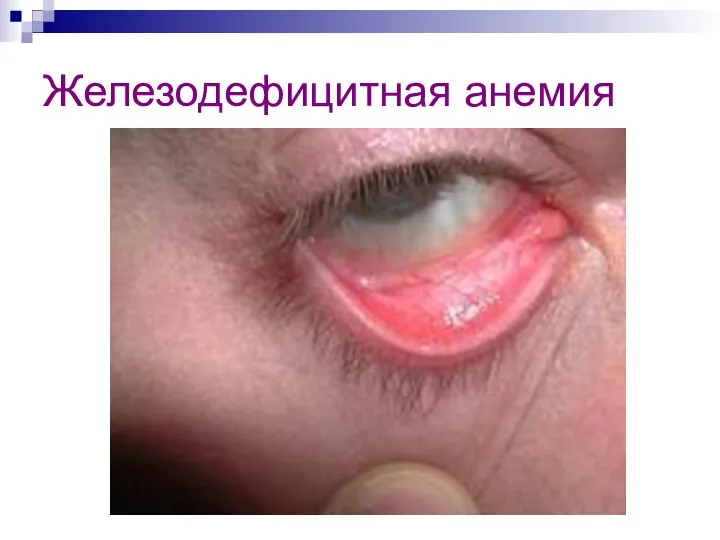
- 26. При недостатке железа в организме (или большой его потере) развивается железодефицитная анемия (малокровие). У беременных женщин
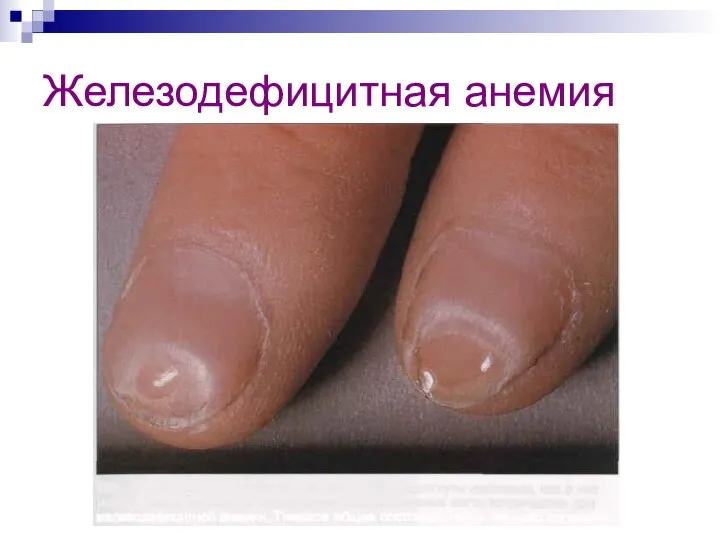
- 27. Железодефицитная анемия
- 28. Железодефицитная анемия
- 29. Железодефицитная анемия
- 30. Лекарственные препараты: FeCl2, FeSO4 ·7H2O, “феррамид” (комплекс Fe с никотиновой кислотой), аскорбинат железа (II), лактат железа
- 31. FeCl3 (слабый окислитель) – применяют наружно как дезинфицирующее и кровоостанавливающее средство
- 32. Кобальт 27Co 4s2 3d7 с.о. +2 и +3 координационное число в комплексных соединениях 6.
- 33. Co in vivo Содержание в организме 1,2мг кобальта, микроэлемент. Топография: мышцы (43%), кости (14%), печень.
- 34. Биороль Биороль кобальта связана с витамином В12, который является порфириновым комплексом Со+³ и в организме выполняет
- 35. Осуществляет перенос Н+, кобальт при этом восстанавливается: +ē HR · Со+3 R· Со+2+ H+ Кобальт в
- 36. Избыток и недостаток Суточная потребность составляет 0,3 мг кобальта. Витамин В12 содержится в мясе, печени, почках,
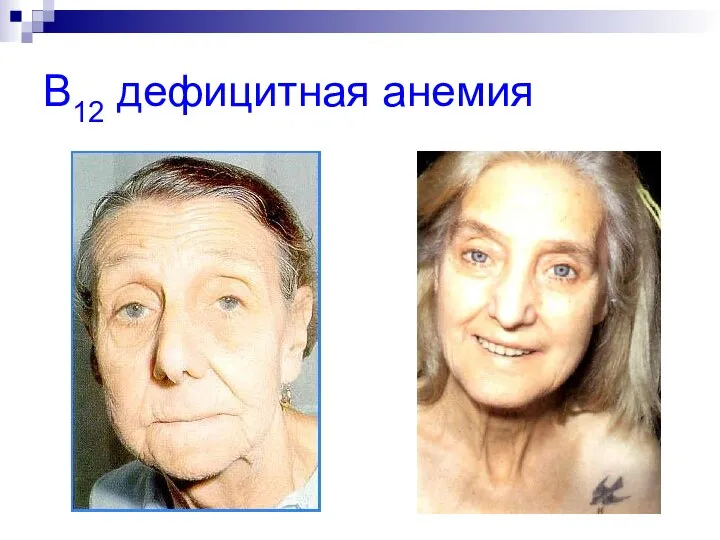
- 37. B12 дефицитная анемия
- 38. Лекарственные препараты: Витамин В12 – для лечения анемии, нервных заболеваний Коамид (комплекс кобальта с никотиновой кислотой)
- 39. Медь Электронная формула: 29Сu 4s13d10, с.о. +1 , +2 координационные числа 2 и 4.
- 40. Химические свойства 2Сu+O2=2CuO CuO+Cu=Cu2O Cu2O+2HCl=2CuCl↓ CuCl+2NH3=[Cu(NH3)2]Cl
- 41. CuO+H2SO4=CuSO4+H2O CuSO4+2NaOH=Cu(OH)2↓+2NaCl.
- 42. Химические свойства Cu(OH)2 обладает амфотерными свойствами, т.е. реагирует и с кислотами, и с основаниями, образует комплексные
- 43. Все соединения Cu ядовиты, даже сама металлическая Cu, т.к. на ее поверхности образуется ядовитый зеленый налет
- 44. Cu in vivo В организме взрослого человека содержится около 100 мг меди, микроэлемент. Топография: печень, головной
- 45. Биороль В биохимических процессах медь участвует в виде комплексов Сu+ и Сu2+ с биолигандами. Известно около
- 46. Медьсодержащие ферменты оксигеназы [ОКГ Сu+] активируют молекулу кислорода в процессе окисления органических соединений: O [ОКГ Сu+]
- 47. Биороль Фермент супероксиддисмутаза [СОД Сu2+] ускоряет реакцию разложения токсичного супероксид-иона ·О2- [СОД Сu2+] +·О2- → [СОД
- 48. Фермент цитохромоксидаза [Fe2+ЦХОСu+], катализирует перенос электронов на кислород на конечном этапе тканевого дыхания: 2[Fe2+ЦХОСu+] + О2
- 49. Биороль Медьсодержащий белок плазмы крови церулоплазмин [ЦП]: а)катализирует окисление Fe+2 в Fe+3 в процессе кроветворения: Fe+2
- 50. б)восстановленная форма церулоплазмина [ЦПСu+] катализирует восстановление кислорода в воду: О2+4[ЦПСu+] +4H+ → 2H2O + 4 [ЦПСu2+]
- 51. в)осуществляет транспорт меди в органы, регулирует баланс меди и обеспечивает выведение её избытка из организма: [ЦПСu2+]→[органы
- 52. Избыток и недостаток Суточная потребность 4-5 мг. Медь содержится в печени телят и ягнят, белых грибах,
- 53. Дефицит меди может привести к разрушению эритроцитов (медная анемия), а также нарушению остеогенеза с изменениями в
- 54. Избыток меди возможен при нарушении синтеза церулоплазмина. Медь накапливается в печени, нервных клетках, разрушая их (болезнь
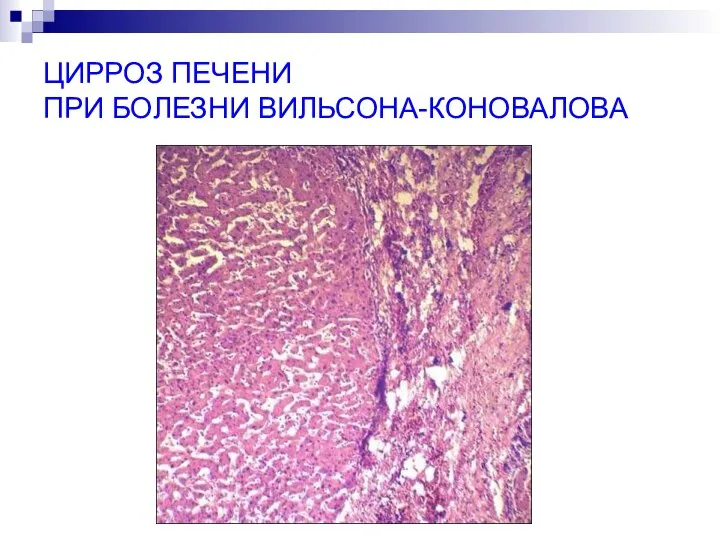
- 55. ЦИРРОЗ ПЕЧЕНИ ПРИ БОЛЕЗНИ ВИЛЬСОНА-КОНОВАЛОВА
- 56. Лекарственные препараты: CuSO4 - наружно как антисептик, вяжущее, прижигающие CuSO4 - в микродозах для лечения анемии.
- 57. Цинк Электронная формула: 30Zn 4s23d10 с.о. +2 координационное число 4.
- 58. Химические свойства: 2Zn+O2=2ZnO ZnO+H2SO4=ZnSO4+H2O Качественная реакция на ион Zn2+ - образование белого осадка сульфида цинка ZnS:
- 59. Амфотерность Zn(OH)2 Zn(OH)2 является амфотерным гидроксидом, реагирует и с кислотами, и с основаниями: Zn(OH)2+2HCl=ZnCl2+2H2O Zn(OH)2+2NaOH=Na2[Zn(OH)4].
- 60. Zn in vivo В организме взрослого человека содержится 1,4 – 2,3 г цинка, микроэлемент. Топография: мышцы
- 61. Биороль Цинк входит в состав более 40 металлоферментов: а) карбоангидраза в эритроцитах катализирует обратимую гидратацию СО2,
- 62. б) карбоксипептидаза КОПZn2+ участвует в гидролизе пептидной связи белков: КОП Zn2+ R1CO-NH R2 + H2O R1COOH
- 63. Биороль Известное влияние цинк оказывает на углеводный обмен, входит в состав активной формы инсулина. Активирует биосинтез
- 64. Участвует в формировании спиральной структуры РНК. Цинк влияет на рост, половое развитие, размножение, способствует делению клеток,
- 65. Избыток и недостаток Суточная потребность цинка около 20 мг компенсируется продуктами, которые употребляют в пищу. Наиболее
- 66. Лекарственные препараты: ZnCl2 – вяжущее, прижигающее и антисептическое действие – для лечения воспаления слизистых. ZnSO4 –
- 67. Токсическое действие Cd, Hg: Наиболее токсична метилртуть (CH3Hg+). Она образуется в водоемах из неорганических соединений ртути
- 68. Метилртуть накапливается в рыбе, а затем с пищей попадает в организм человека, растворяется в липидах мембран
- 69. Постепенно концентрируясь, она вызывает необратимые разрушения в организме и смерть. Отравление метилртутью вызывает болезнь Минамата (нервно-психические
- 70. Болезнь Минамата
- 71. Механизм токсического действия ртути и кадмия: 1. Ионы Cd2+ и Hg2+ могут замещать Ca2+ в соединениях,
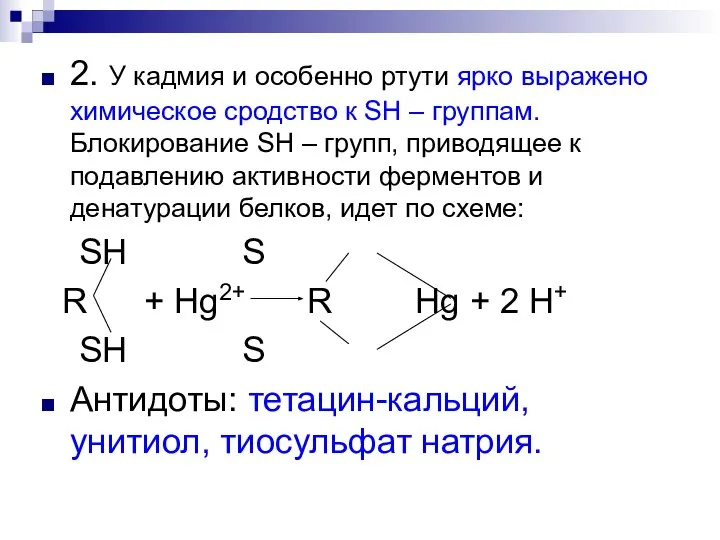
- 72. 2. У кадмия и особенно ртути ярко выражено химическое сродство к SH – группам. Блокирование SH
- 73. Лекарственные препараты: HgСl2 – в концентрации 1 : 1000 для дезинфекции и как антисептик. HgО –
- 75. Скачать презентацию
![Основные и восстановительные свойства Mn2+ MnO+H2SO4+5H2O=[Mn(H2O)6]SO4 MnSO4+2NaOH=Mn(OH)2↓+Na2SO4 Mn(OH)2+O2+H2O→Mn(OH)4→MnO2↓+H2O Качественная реакция на](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1396249/slide-2.jpg)















![б) миоглобин (Mb) осуществляет обратимый перенос кислорода в мышцах: [MbFe+2] + O2 [MbFe+2O2]; дезоксиформа оксиформа](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1396249/slide-19.jpg)















![Химические свойства 2Сu+O2=2CuO CuO+Cu=Cu2O Cu2O+2HCl=2CuCl↓ CuCl+2NH3=[Cu(NH3)2]Cl](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1396249/slide-39.jpg)





![Медьсодержащие ферменты оксигеназы [ОКГ Сu+] активируют молекулу кислорода в процессе окисления](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1396249/slide-45.jpg)
![Биороль Фермент супероксиддисмутаза [СОД Сu2+] ускоряет реакцию разложения токсичного супероксид-иона ·О2-](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1396249/slide-46.jpg)
![Фермент цитохромоксидаза [Fe2+ЦХОСu+], катализирует перенос электронов на кислород на конечном этапе](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1396249/slide-47.jpg)
![Биороль Медьсодержащий белок плазмы крови церулоплазмин [ЦП]: а)катализирует окисление Fe+2 в](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1396249/slide-48.jpg)
![б)восстановленная форма церулоплазмина [ЦПСu+] катализирует восстановление кислорода в воду: О2+4[ЦПСu+] +4H+ → 2H2O + 4 [ЦПСu2+]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1396249/slide-49.jpg)







![Амфотерность Zn(OH)2 Zn(OH)2 является амфотерным гидроксидом, реагирует и с кислотами, и с основаниями: Zn(OH)2+2HCl=ZnCl2+2H2O Zn(OH)2+2NaOH=Na2[Zn(OH)4].](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1396249/slide-58.jpg)













 Излучение и поглощение света атомами. Виды спектров, спектральный анализ
Излучение и поглощение света атомами. Виды спектров, спектральный анализ Физико-химические методы анализа
Физико-химические методы анализа Лекция 3. Разновидности химических связей
Лекция 3. Разновидности химических связей Соединения алифатического ряда
Соединения алифатического ряда Механизмы нейропротекторного действия уабаина при эксайтотоксическом стрессе в нейронах коры крыс
Механизмы нейропротекторного действия уабаина при эксайтотоксическом стрессе в нейронах коры крыс Презентация по Химии "Теория химического строения органических веществ" - скачать смотреть
Презентация по Химии "Теория химического строения органических веществ" - скачать смотреть  Практическая работа по разделению смесей
Практическая работа по разделению смесей Презентация по Химии "Альдегиды, свойства, получение, применение" - скачать смотреть
Презентация по Химии "Альдегиды, свойства, получение, применение" - скачать смотреть  Дыхательная функция крови
Дыхательная функция крови Хімічні властивості карбонових кислот
Хімічні властивості карбонових кислот Соляная кислота и её соли
Соляная кислота и её соли Периодическая система Д.И. Менделеева
Периодическая система Д.И. Менделеева Крахмал (C6H10O5)n
Крахмал (C6H10O5)n  Органические вяжущие. (Лекция 12)
Органические вяжущие. (Лекция 12) Многоатомные спирты
Многоатомные спирты Вода - основа жизни
Вода - основа жизни Ароматические углеводороды (арены)
Ароматические углеводороды (арены) Нафта Походження,переробка, використання
Нафта Походження,переробка, використання  Зелёная химия
Зелёная химия Cинтетичні миючі засоби і їхній вплив на людину
Cинтетичні миючі засоби і їхній вплив на людину  Алюминий в природе
Алюминий в природе Характеристика металу Sr
Характеристика металу Sr Құрамында галогендер бар мономерлер. Винилхлорид пен винилфторидті алу жолдары. Поливинилхлоридты өндіру
Құрамында галогендер бар мономерлер. Винилхлорид пен винилфторидті алу жолдары. Поливинилхлоридты өндіру Презентация по Химии "Растворение. Растворимость. Типы растворов" - скачать смотреть
Презентация по Химии "Растворение. Растворимость. Типы растворов" - скачать смотреть  Творческий проект на тему химия в пище
Творческий проект на тему химия в пище Биологически важные ароматические и гетероциклические соединения
Биологически важные ароматические и гетероциклические соединения Растворы. Качественный и количественный состав растворов
Растворы. Качественный и количественный состав растворов Доказательство амфотерности аминокислот. Продукты, содержащие аминокислоты и их соли
Доказательство амфотерности аминокислот. Продукты, содержащие аминокислоты и их соли