Содержание
- 2. План лекции Функции мышц Классификация мышечных волокон Химический состав мышц Особенности обмена веществ и энергии в
- 3. Мышечная система У многоклеточных организмов генерацию движения за счет энергии АТФ осуществляют высокоспециализированные органы – мышцы.
- 4. Функции мышц Передвижение тела в пространстве поддержание позы обеспечивают работу сердечно-сосудистой, дыхательной, мочеполовой, желудочно-кишечной системы выработка
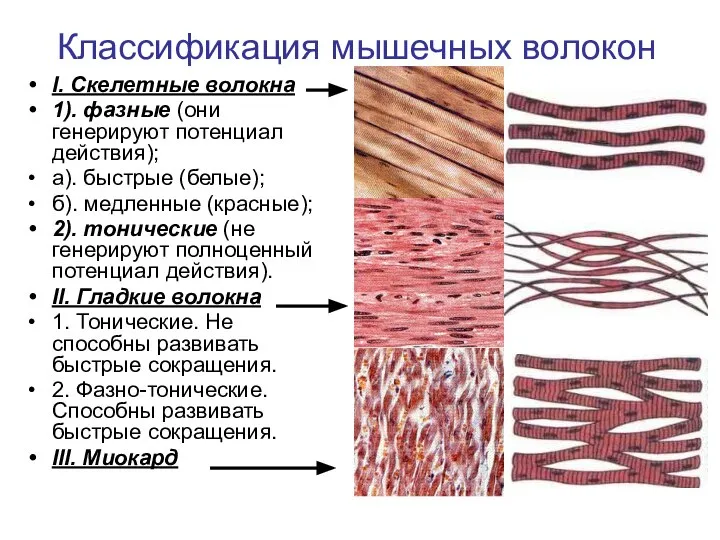
- 5. I. Скелетные волокна 1). фазные (они генерируют потенциал действия); а). быстрые (белые); б). медленные (красные); 2).
- 6. Мышечное волокно Функциональной единицей мышечной ткани является мышечное волокно Мышечное волокно поперечнополосатой мышцы- это многоядерная клетка.
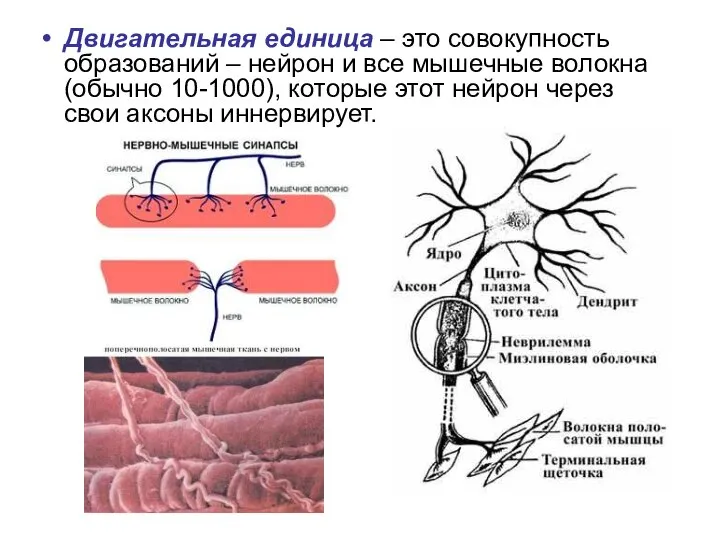
- 7. Двигательная единица – это совокупность образований – нейрон и все мышечные волокна (обычно 10-1000), которые этот
- 8. ХИМИЧЕСКИЙ СОСТАВ МЫШЕЧНОЙ ТКАНИ Вода............................................72—80 Сухой остаток …........................20—28 В том числе: Белки...........................................16,5—20,9 Гликоген......................................0,3—3,0 Фосфатиды.................................0,4—1,0 Холестерин.................................0,06—0,2 Креатин
- 9. 1. Сократительные (миофибриллярные) белки миозин 55% актин 25% тропомиозин (во всех мышцах) тропонины Т, I и
- 10. Углеводы мышечной ткани Гликоген: 0,3-3,0% ГАГ моносахариды глюкоза, фруктоза Липиды мышечной ткани Фосфолипиды (в миокарде больше)
- 11. ОСОБЕННОСТИ ОБМЕНА ВЕЩЕСТВ В МЫШЕЧНОЙ ТКАНИ Обмен белков и аминокислот Мышцы характеризуются высоким обменом белков и
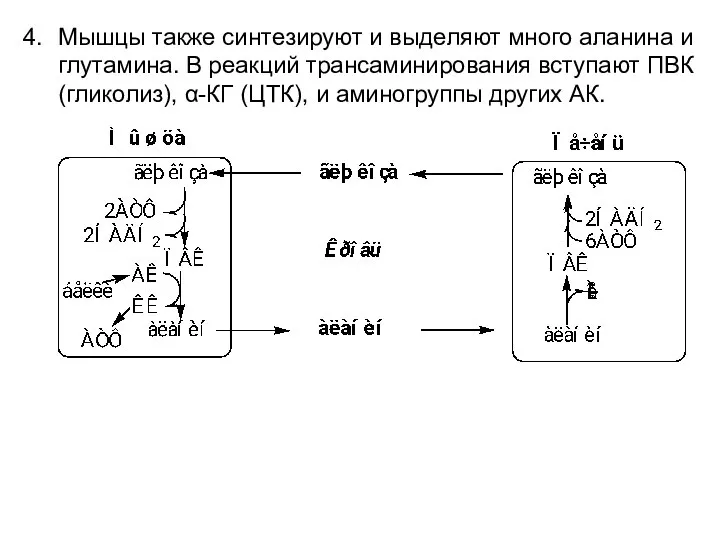
- 12. Мышцы также синтезируют и выделяют много аланина и глутамина. В реакций трансаминирования вступают ПВК (гликолиз), α-КГ
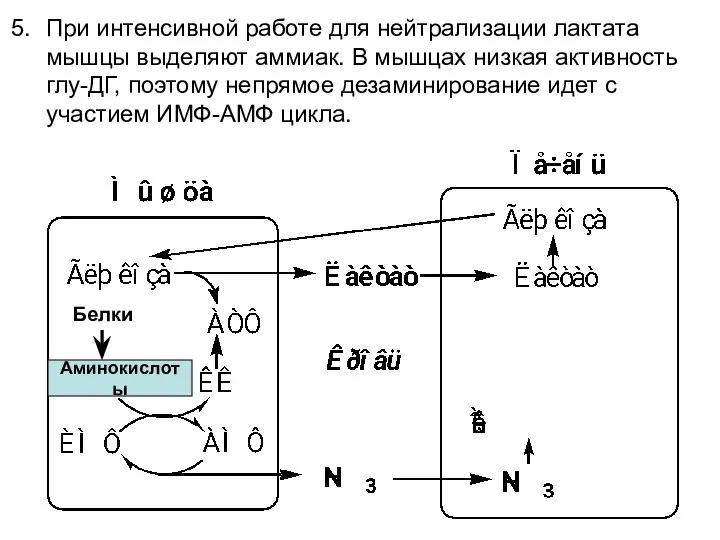
- 13. Аминокислоты Белки При интенсивной работе для нейтрализации лактата мышцы выделяют аммиак. В мышцах низкая активность глу-ДГ,
- 14. Липидный обмен преобладает катаболизм липидов. Жирные кислоты, кетоновые тела в аэробных условиях окисляются в мышцах для
- 15. Углеводный обмен преобладает катаболизм углеводов. глюкоза окисляется в аэробных или анаэробных условиях для синтеза АТФ. Из
- 16. Энергетический обмен Энергетический обмен в состоянии покоя очень низкий, при интенсивной физической нагрузке значительно возрастает. В
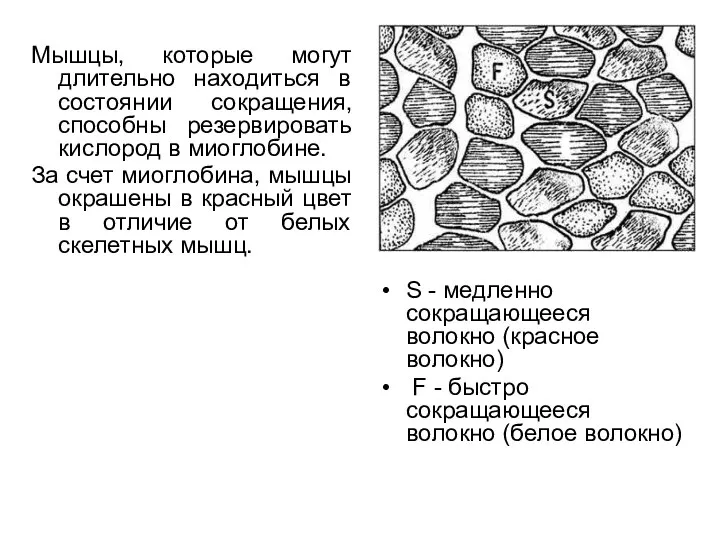
- 17. Мышцы, которые могут длительно находиться в состоянии сокращения, способны резервировать кислород в миоглобине. За счет миоглобина,
- 18. Основной потребитель АТФ - процесс мышечного сокращения. Запасы АТФ быстро истощаются. Источники АТФ: 1) классический путь
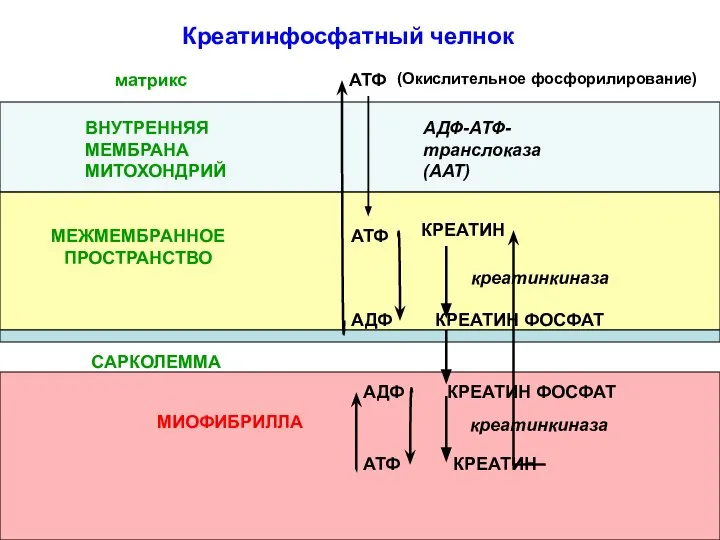
- 19. (Окислительное фосфорилирование) АТФ АДФ-АТФ-транслоказа(ААТ) ВНУТРЕННЯЯ МЕМБРАНА МИТОХОНДРИЙ КРЕАТИН КРЕАТИН ФОСФАТ АТФ АДФ САРКОЛЕММА МИОФИБРИЛЛА КРЕАТИН ФОСФАТ
- 20. Креатинфосфатный челнок предотвращает быстрое истощение запасов АТФ в мышце за счет: запаса макроэргических связей в креатинфосфате
- 21. Характеристика быстрых и медленных скелетных мышц
- 22. Миофибрилла
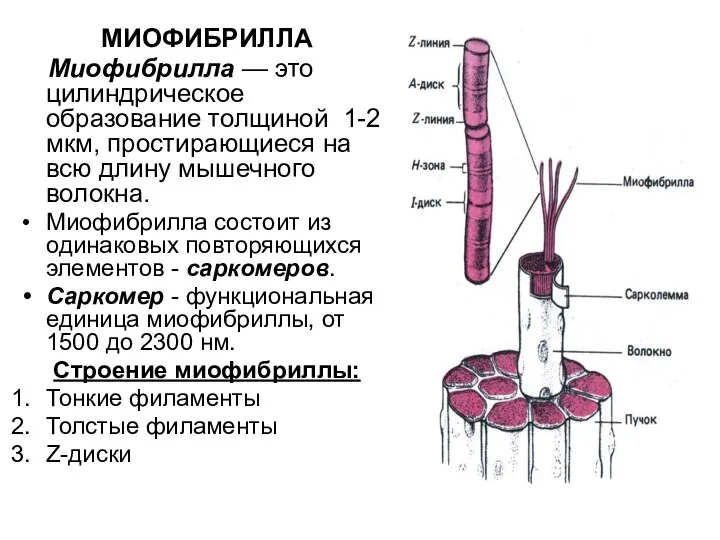
- 23. МИОФИБРИЛЛА Миофибрилла — это цилиндрическое образование толщиной 1-2 мкм, простирающиеся на всю длину мышечного волокна. Миофибрилла
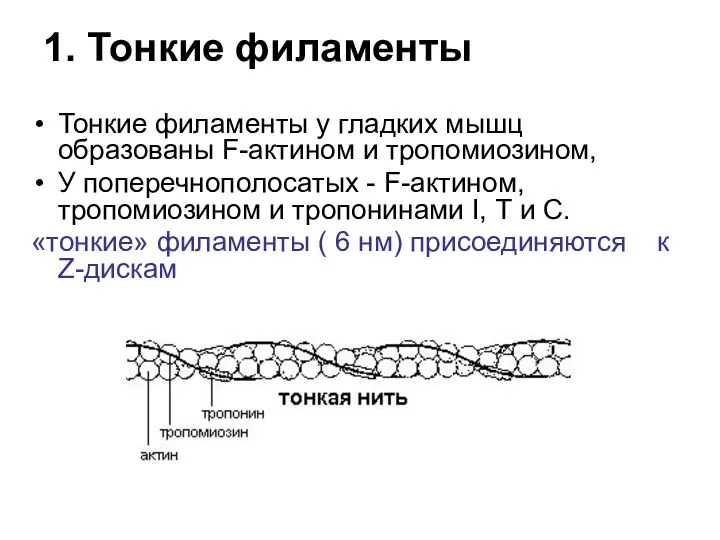
- 24. 1. Тонкие филаменты Тонкие филаменты у гладких мышц образованы F-актином и тропомиозином, У поперечнополосатых - F-актином,
- 25. Актин G-актин - мономерный (глобулярный) белок с массой 43кДа. F-актин. При физиологической величине рН и в
- 26. Тропомиозин - есть во всех мышцах: белок, состоящий из а и р цепей, располагается в щели
- 27. 2. Толстые филаменты образованы миозином, размер 16нм. располагаются в центре саркомера, между «тонкими» филаментами. На поверхности
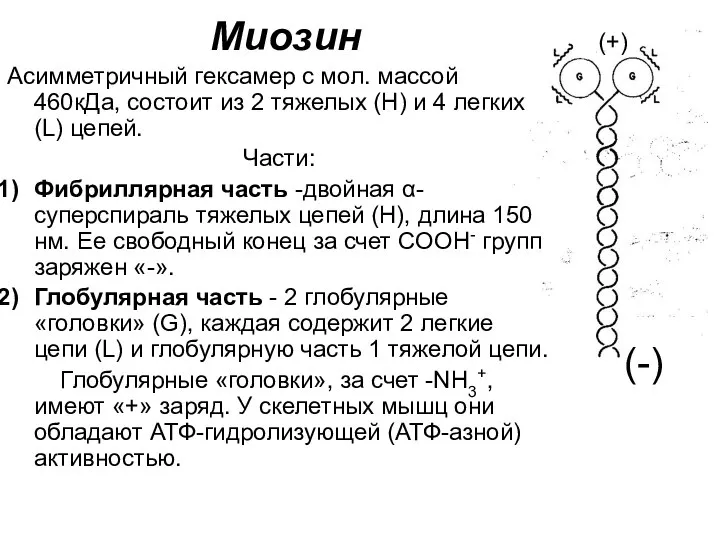
- 28. Миозин Асимметричный гексамер с мол. массой 460кДа, состоит из 2 тяжелых (Н) и 4 легких (L)
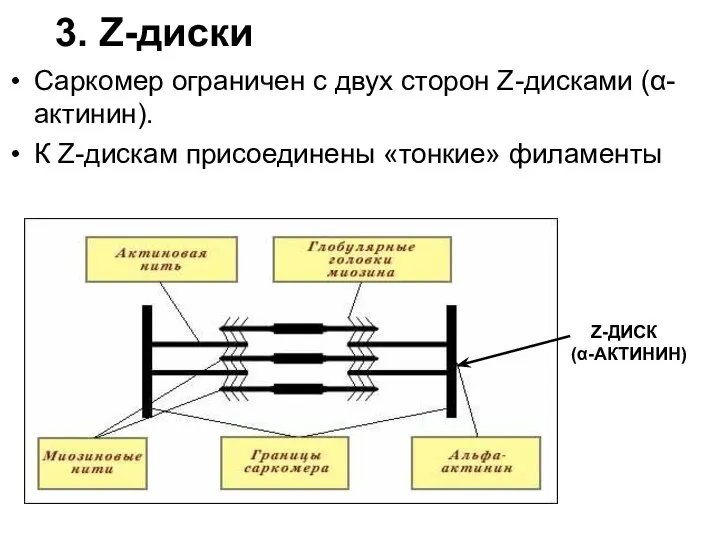
- 29. 3. Z-диски Саркомер ограничен с двух сторон Z-дисками (α-актинин). К Z-дискам присоединены «тонкие» филаменты Z-ДИСК (α-АКТИНИН)
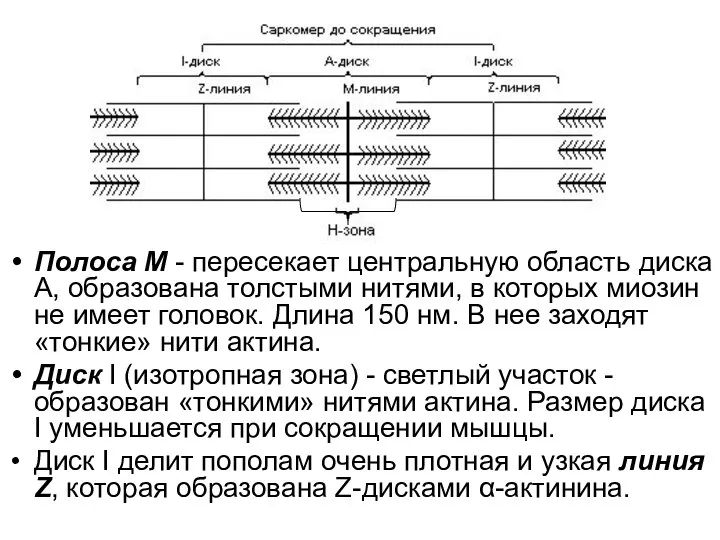
- 30. Строение саркомера Диск А (анизотропная зона)= темный участок –образован «толстыми» нитями миозина. Зона Н - центральная
- 31. Полоса М - пересекает центральную область диска А, образована толстыми нитями, в которых миозин не имеет
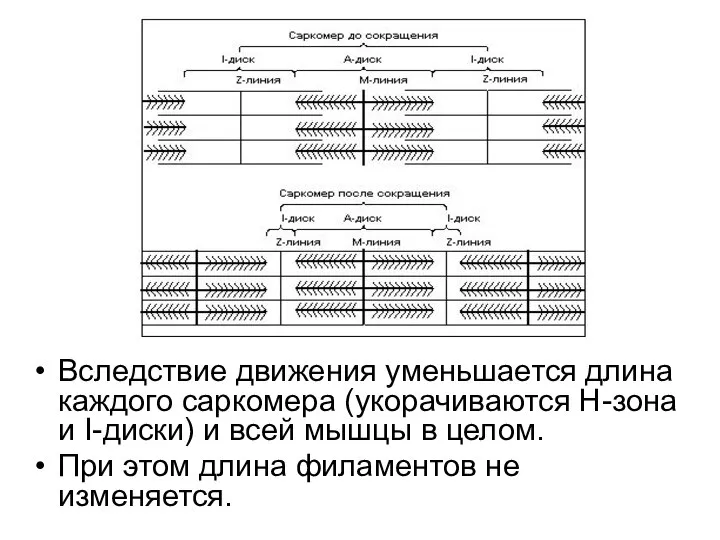
- 32. Вследствие движения уменьшается длина каждого саркомера (укорачиваются Н-зона и I-диски) и всей мышцы в целом. При
- 33. В скелетной мышечной ткани саркомеры миофибрилл располагаются параллельно. За счет этого на срезах скелетные мышцы выглядят
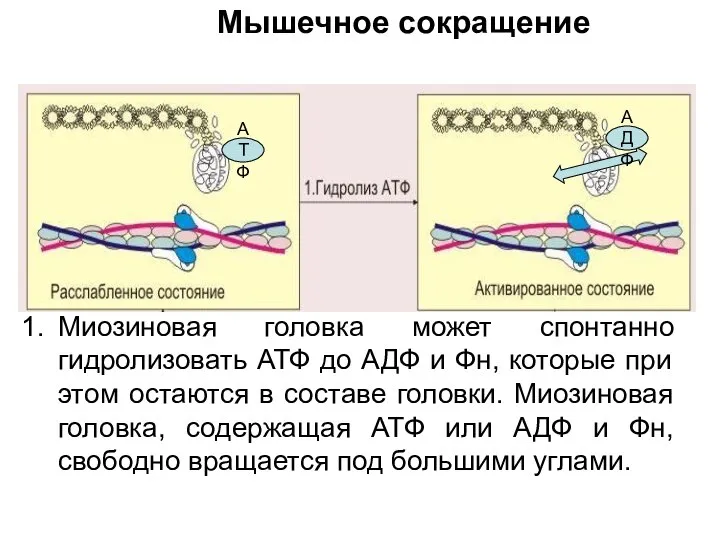
- 34. Миозиновая головка может спонтанно гидролизовать АТФ до АДФ и Фн, которые при этом остаются в составе
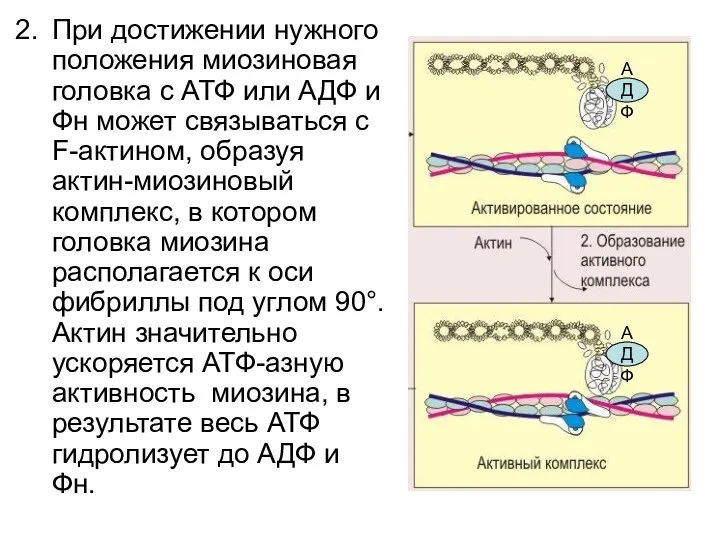
- 35. При достижении нужного положения миозиновая головка с АТФ или АДФ и Фн может связываться с F-актином,
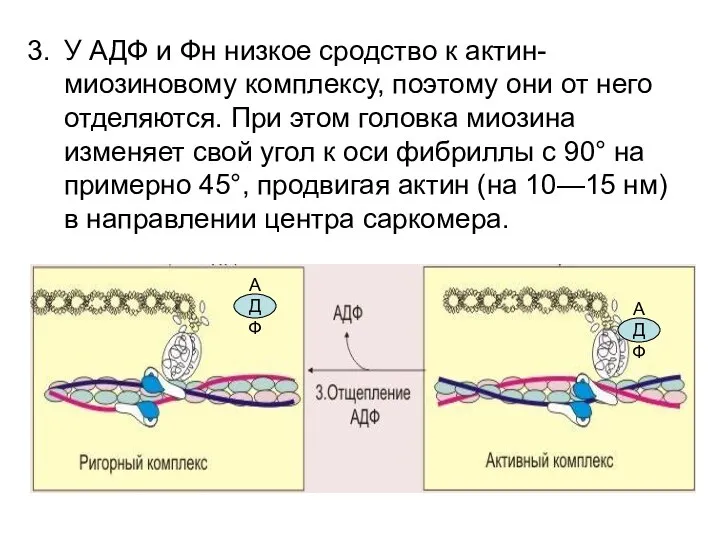
- 36. У АДФ и Фн низкое сродство к актин-миозиновому комплексу, поэтому они от него отделяются. При этом
- 37. Новая молекула АТФ присоединяется к актин-миозиновому комплексу. Комплекс актин-миозин-АТФ обладает низким сродством к актину, поэтому миозиновая
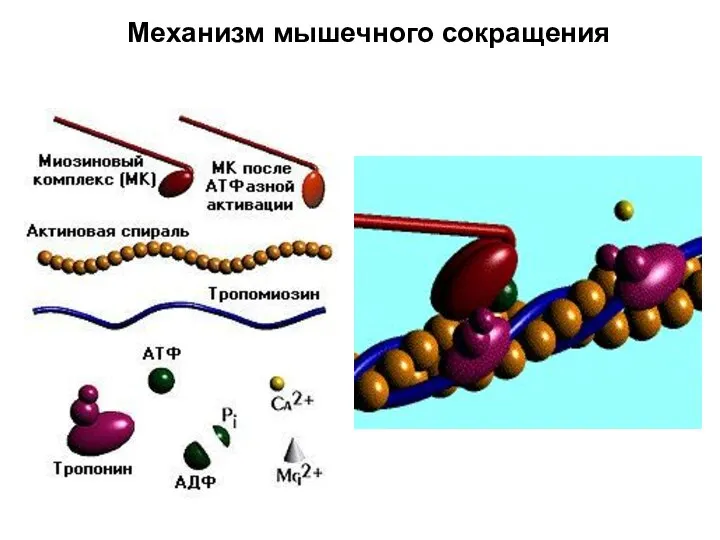
- 38. Механизм мышечного сокращения
- 39. Регуляция сокращения и расслабления мышц Любое мышечное сокращение опосредуется Са2+. Кальциевые насосы постоянно перекачивают Са2+ из
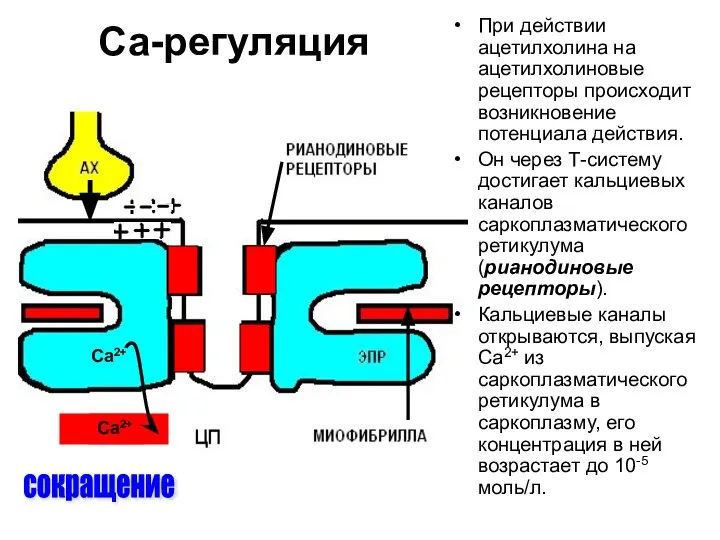
- 40. Са-регуляция сокращение При действии ацетилхолина на ацетилхолиновые рецепторы происходит возникновение потенциала действия. Он через Т-систему достигает
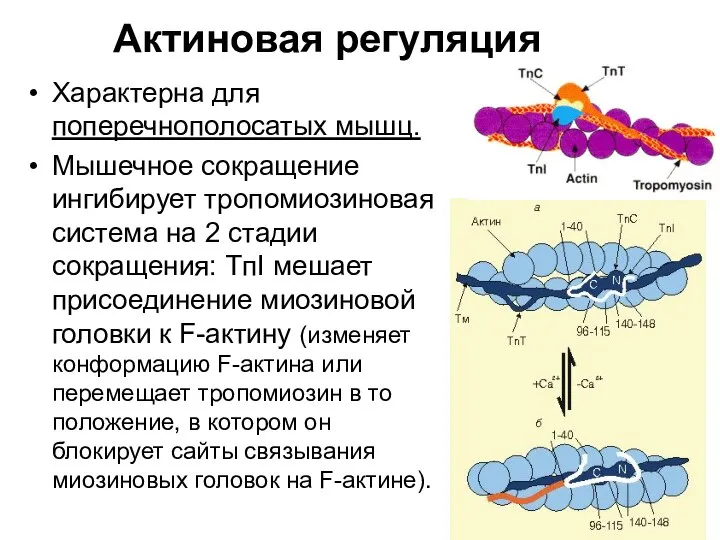
- 41. Актиновая регуляция Характерна для поперечнополосатых мышц. Мышечное сокращение ингибирует тропомиозиновая система на 2 стадии сокращения: TпI
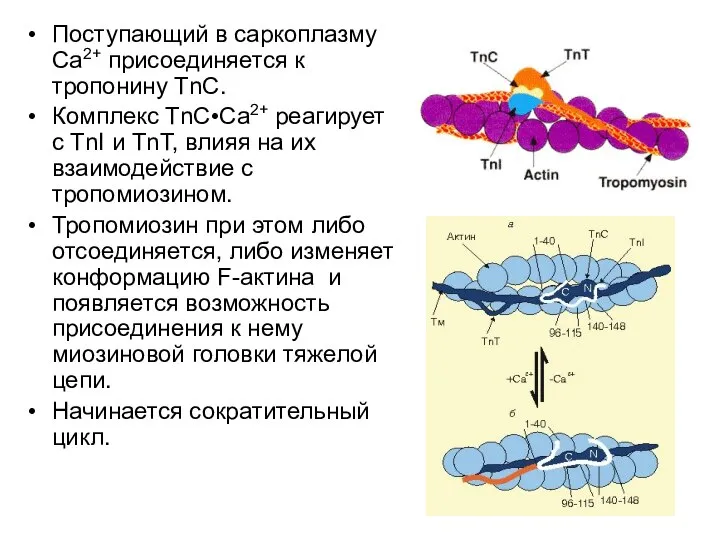
- 42. Поступающий в саркоплазму Са2+ присоединяется к тропонину ТnС. Комплекс ТnС•Са2+ реагирует с TnI и ТnТ, влияя
- 43. Расслабление происходит, когда: 1) При перекачке Са2+ в ЭПР его содержание в саркоплазме падает ниже 10-7
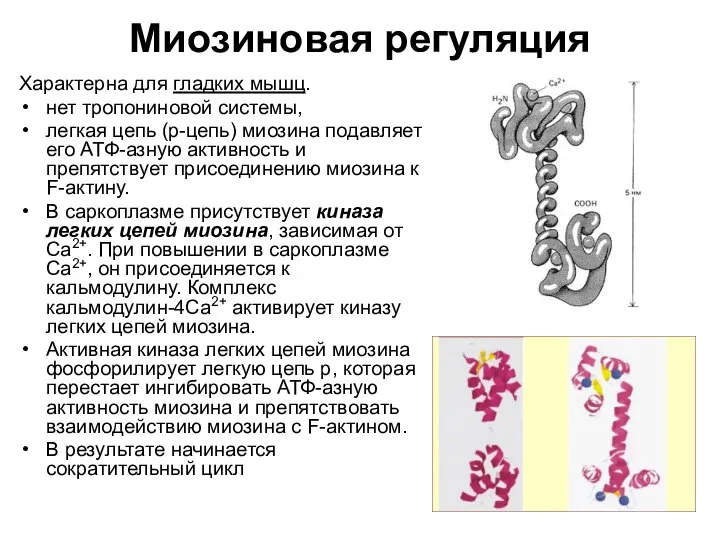
- 44. Миозиновая регуляция Характерна для гладких мышц. нет тропониновой системы, легкая цепь (р-цепь) миозина подавляет его АТФ-азную
- 45. Расслабление гладких мышц происходит, когда: 1) содержание ионов Са2+ в саркоплазме падает ниже 10-7 моль/л 2)
- 46. Биохимические показатели крови и мочи, отражающие функциональное состояние мышечной ткани Аминотрансферазы -диагностика патологии печени и миокарда.
- 47. Тропонин Т -маркер инфаркта миокарда в острой и подострой фазе. Миоглобин -маркер деструктивных изменений в мышечной
- 48. Миопатии (греч. mys, myos мышца + pathos страдание, болезнь) - нервно-мышечные заболевания, характеризующиеся развитием первичного дистрофического
- 50. БИОХИМИЧЕСКИЕ ИЗМЕНЕНИЯ В МЫШЦАХ ПРИ ПАТОЛОГИИ: снижение содержания миофибриллярных белков возрастание концентрации белков стромы и некоторых
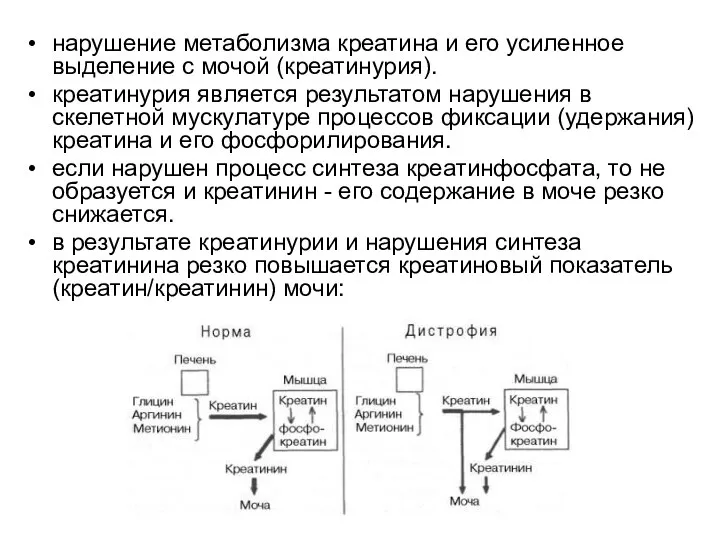
- 51. нарушение метаболизма креатина и его усиленное выделение с мочой (креатинурия). креатинурия является результатом нарушения в скелетной
- 52. Изменение активности ферментов в мышцах: уменьшается активность ферментов, локализованных в саркоплазме изменяется активность ферментов, связанных с
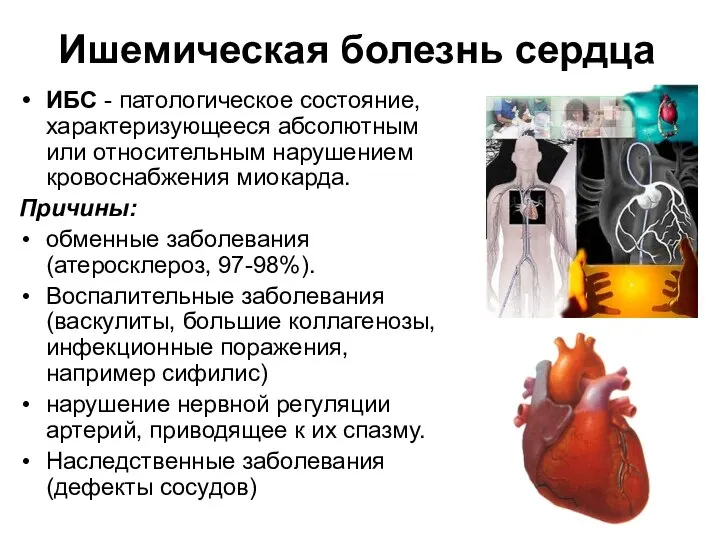
- 53. Ишемическая болезнь сердца ИБС - патологическое состояние, характеризующееся абсолютным или относительным нарушением кровоснабжения миокарда. Причины: обменные
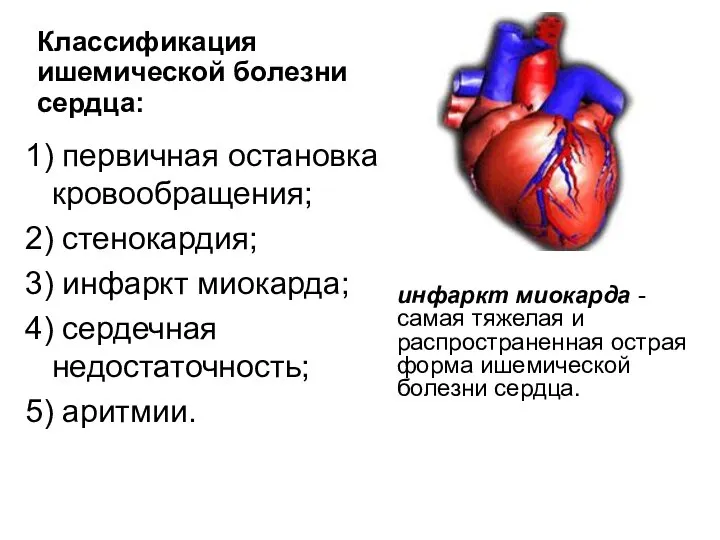
- 54. 1) первичная остановка кровообращения; 2) стенокардия; 3) инфаркт миокарда; 4) сердечная недостаточность; 5) аритмии. Классификация ишемической
- 56. Причины инфаркта миокарда Атеросклероз коронарных артерий Эмболы, тромбы коронарной артерии Спазм коронарных артерий и резко повышение
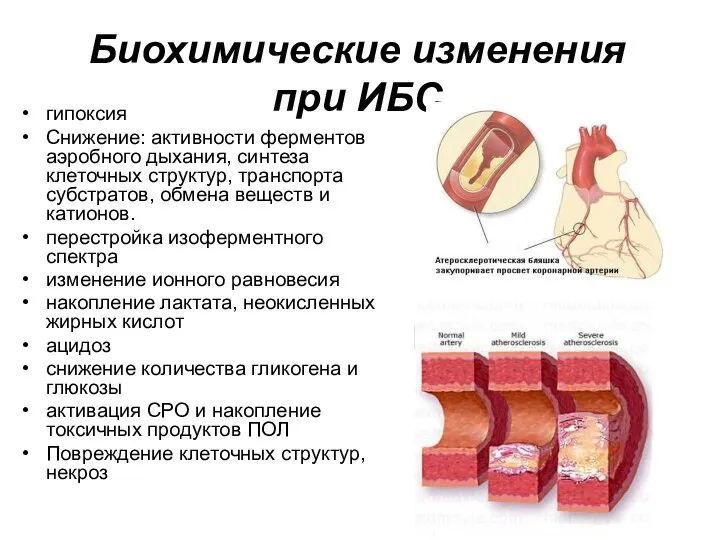
- 57. Биохимические изменения при ИБС гипоксия Снижение: активности ферментов аэробного дыхания, синтеза клеточных структур, транспорта субстратов, обмена
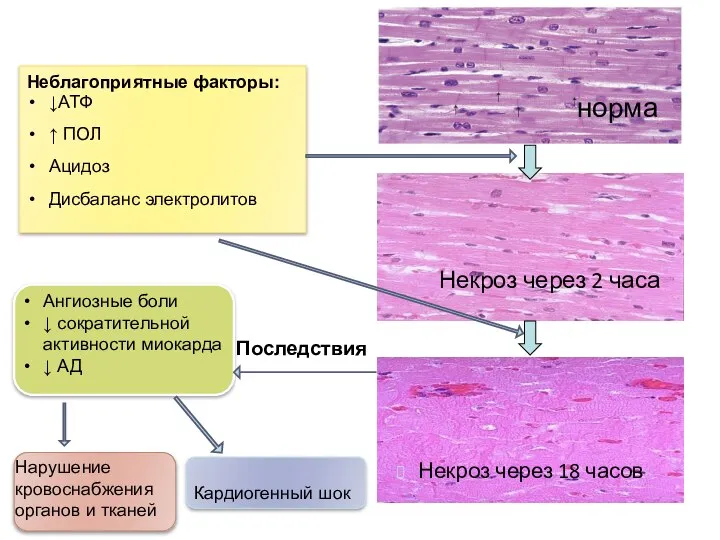
- 58. норма Некроз через 2 часа Некроз через 18 часов Неблагоприятные факторы: ↓АТФ ↑ ПОЛ Ацидоз Дисбаланс
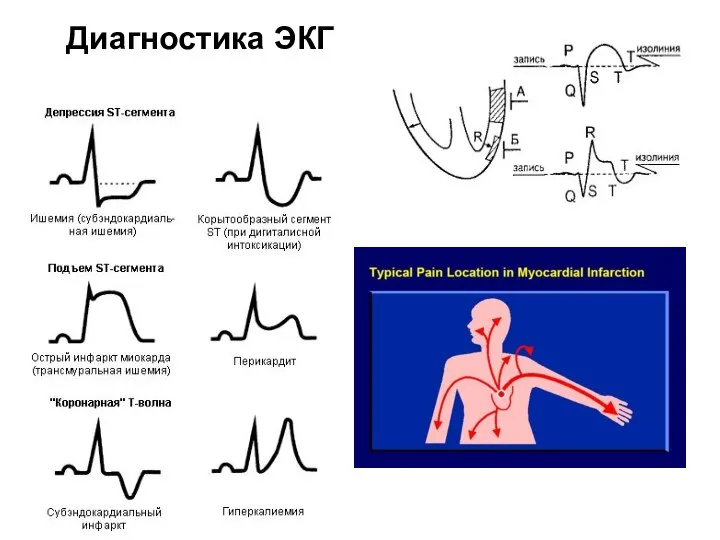
- 59. Диагностика ЭКГ
- 60. Биохимическая диагностика Аспартатаминотрансфераза (АСТ) Аланинаминотрансфераза (АЛТ) Креатинфосфокиназа (КФК, КФК-МВ) Лактатдегидрогеназа (ЛДГ1,2) Тропонины Коэффициент Де-Ритиса (АСТ/АЛТ)
- 61. При гипоксии миокард поглощает ТГ из липопротеинов, которые не используются, а накапливаются, приводя к ожирению миокарда.
- 62. Терапия
- 64. Скачать презентацию



































 Тема урока: «Классификация и свойства кислот»
Тема урока: «Классификация и свойства кислот» Энергетика химических реакций. Лекция 4
Энергетика химических реакций. Лекция 4 Аттестаионная работа. Сахар. Изучаем и исследуем
Аттестаионная работа. Сахар. Изучаем и исследуем Драгоценные камни
Драгоценные камни Великие химики
Великие химики Тепловой эффект химических реакций 8 класс
Тепловой эффект химических реакций 8 класс Учитель химии МОУ СОШ №18 Лаврик Виктория Александровна
Учитель химии МОУ СОШ №18 Лаврик Виктория Александровна 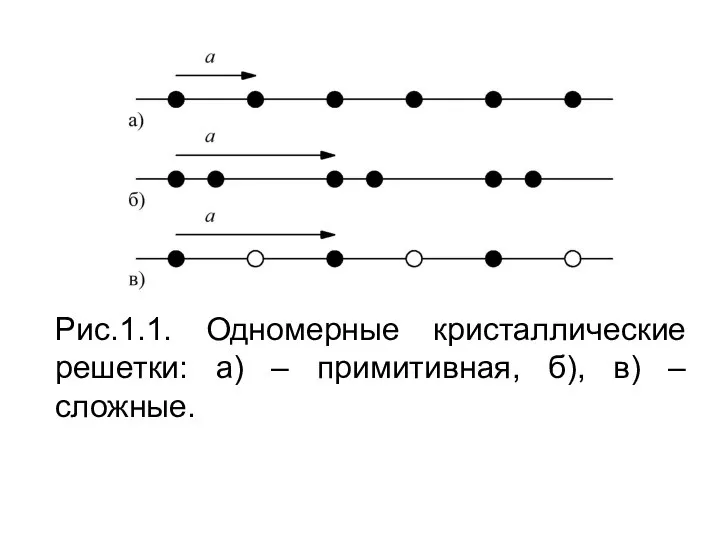 Кристаллические решётки
Кристаллические решётки Углеводы Органические соединения, содержащие в составе молекул наряду с карбонильной несколько гидроксильных групп, их пр
Углеводы Органические соединения, содержащие в составе молекул наряду с карбонильной несколько гидроксильных групп, их пр Спирты (карбинолы)
Спирты (карбинолы) Презентация по Химии "Промышленное получение аминокислот и их применение в медицыне и диетологии" - скачать смотреть бесплат
Презентация по Химии "Промышленное получение аминокислот и их применение в медицыне и диетологии" - скачать смотреть бесплат Удивительные свойства воды
Удивительные свойства воды Проблема химического элемента. Концепции структуры химических соединений
Проблема химического элемента. Концепции структуры химических соединений Химия Для студентов I курса специальностей: 2080165 — экология, 08040165 — товароведение и экспертиза товаров, 260800 — технология, конс
Химия Для студентов I курса специальностей: 2080165 — экология, 08040165 — товароведение и экспертиза товаров, 260800 — технология, конс Анализ лекарственных форм с витаминами и использование физико-химических и химических методов анализа. Вопросы стабилизации
Анализ лекарственных форм с витаминами и использование физико-химических и химических методов анализа. Вопросы стабилизации Валентность (8 класс)
Валентность (8 класс) Работу выполняла: Шумкова Елизавета. Руководитель: Шилоносова Елена Леонидовна.
Работу выполняла: Шумкова Елизавета. Руководитель: Шилоносова Елена Леонидовна. Крахмал. Физические свойства
Крахмал. Физические свойства Нанохимия
Нанохимия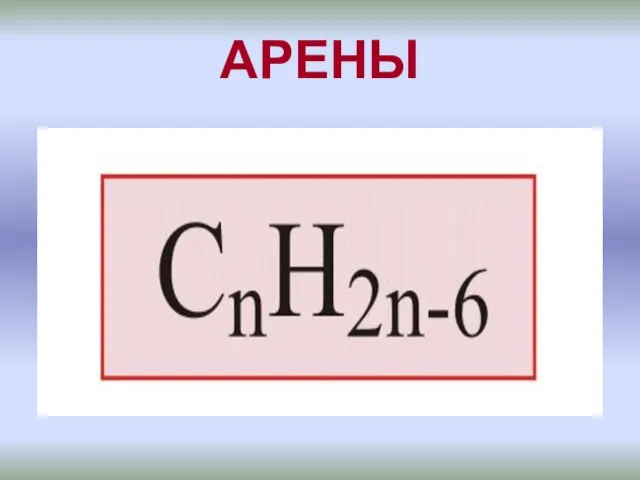 Бензоидные ароматические углеводороды - арены
Бензоидные ароматические углеводороды - арены Химия. Атомы, молекулы и ионы
Химия. Атомы, молекулы и ионы Ammonia and amines
Ammonia and amines Каучук. Применение
Каучук. Применение 5 группа элементов
5 группа элементов Аттестационная работа. Окраска ткани природными красителями
Аттестационная работа. Окраска ткани природными красителями Методы исследования и характеризации поверхностей. Поверхностное и межфазное натяжение. Тензиометрия и эллипсометрия
Методы исследования и характеризации поверхностей. Поверхностное и межфазное натяжение. Тензиометрия и эллипсометрия Растворы. Термодинамическая теория растворов
Растворы. Термодинамическая теория растворов Презентация по Химии "Синтетические материалы" - скачать смотреть
Презентация по Химии "Синтетические материалы" - скачать смотреть