Содержание
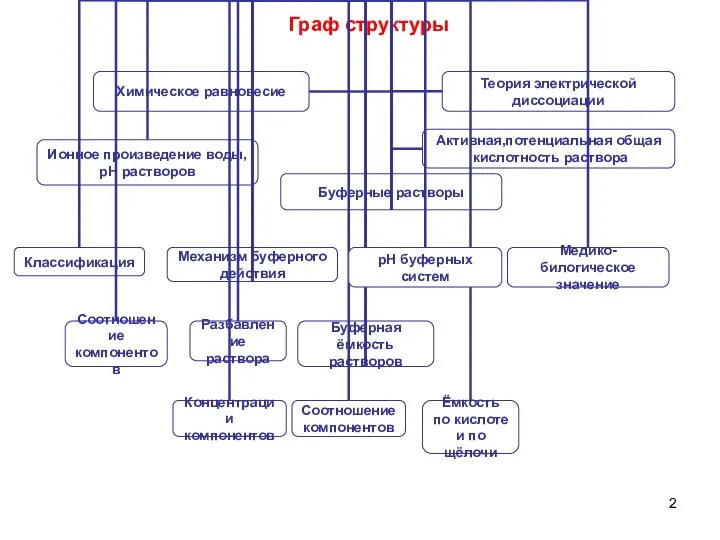
- 2. Граф структуры
- 3. Теории кислот и оснований
- 4. 1. По Аррениусу: Нобелевская премия по химии «как факт признания особого значения его теории электролитической диссоциации
- 5. Кислота тем слабее, чем меньше Кд и больше значение ее рКД.
- 6. Недостатки CН3СООН в воде – слабая кислота: CH3COOH ↔ CH3COO- + H+ в жидком HF –
- 7. 2. По Бренстеду: БРЕНСТЕД Йоханнес (22.11 1879 – 17.12 1947) Кислота (донор протонов) - вещество, молекулярные
- 8. СОПРЯЖЕННЫЕ ПАРЫ КИСЛОТА–ОСНОВАНИЕ (В ВОДНОМ РАСТВОРЕ ПРИ КОМНАТНОЙ ТЕМПЕРАТУРЕ)
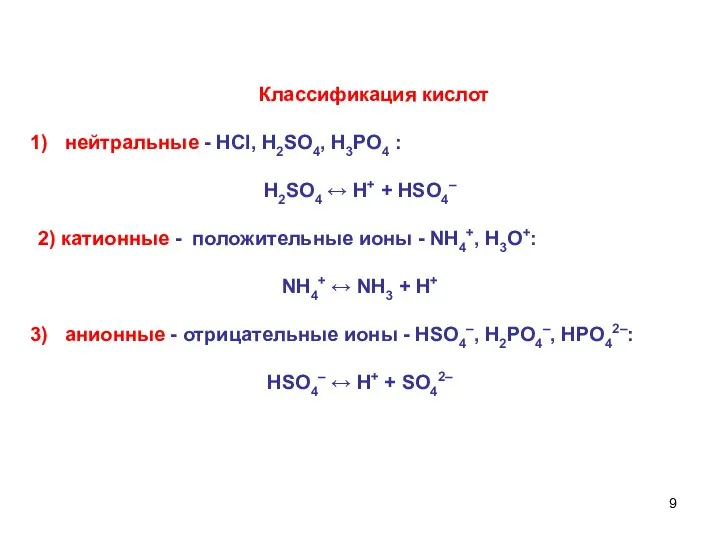
- 9. Классификация кислот нейтральные - НСl, H2SO4, Н3РО4 : H2SO4 ↔ Н+ + HSO4– 2) катионные -
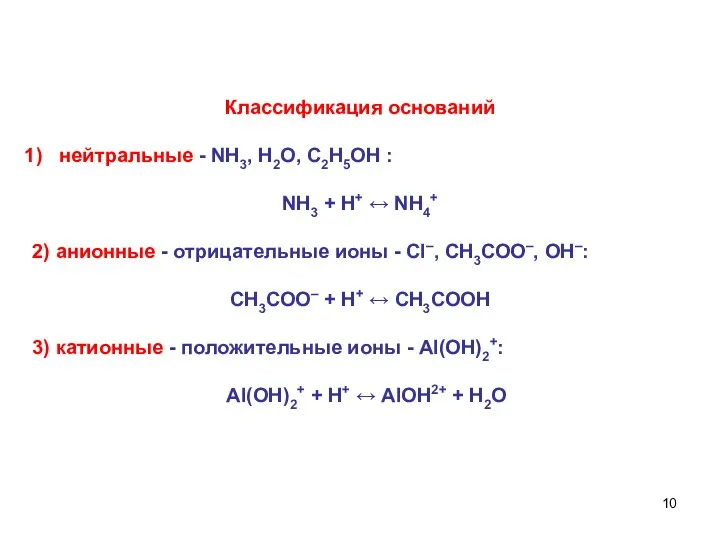
- 10. Классификация оснований нейтральные - NH3, H2O, С2Н5ОН : NH3 + Н+ ↔ NH4+ 2) анионные -
- 11. Вода, жидкий аммиак и анионы многоосновных кислот, которые могут быть и донорами и акцепторами протонов, являются
- 12. 3. По Льюису ЛЬЮИС Гилберт Ньютон (23.10 1875–23.03 1946) Во время первой мировой войны – полковник
- 13. Кислота - акцептор электронов. реакцию нейтрализации в водных растворах, взаимодействие аминов с галогениами комплексообразование. Основание -
- 14. Значение постоянства кислотности жидких сред для жизнедеятельности человеческого организма : Ионы водорода оказывают каталитическое действие на
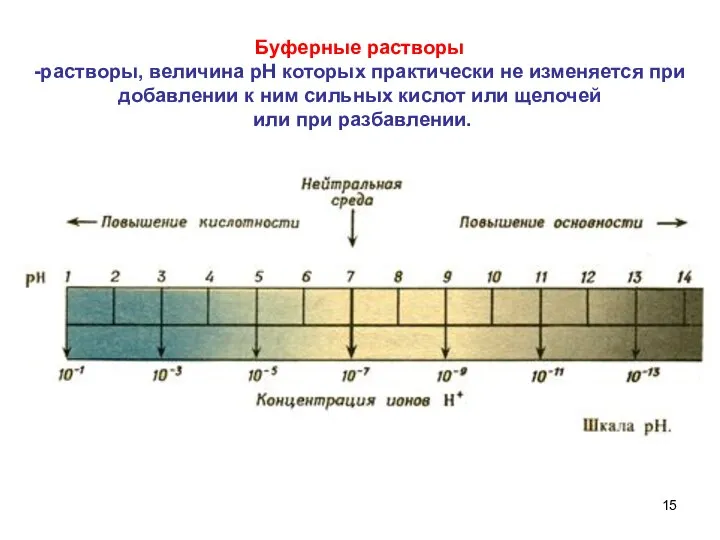
- 15. Буферные растворы -растворы, величина рН которых практически не изменяется при добавлении к ним сильных кислот или
- 16. 1. Ацетатный буфер: 3. Фосфатный буфер: 2. Бикарбонатный буфер: Аммиачный буфер: Классификация: а) кислотные б) основные
- 17. Механизм буферного действия а) + HCl СH3COOK + HCl → СH3COOH + KCl СH3COO - +
- 18. В ацетатном буферном растворе устанавливается равновесие: СH3COOH ↔ H+ + СH3COO- Можно схематически представить, что буферная
- 19. Добавим 1 каплю (0,05 мл) 1н НСl к 1л воды (безбуферный раствор, рН=7) и рассчитаем изменение
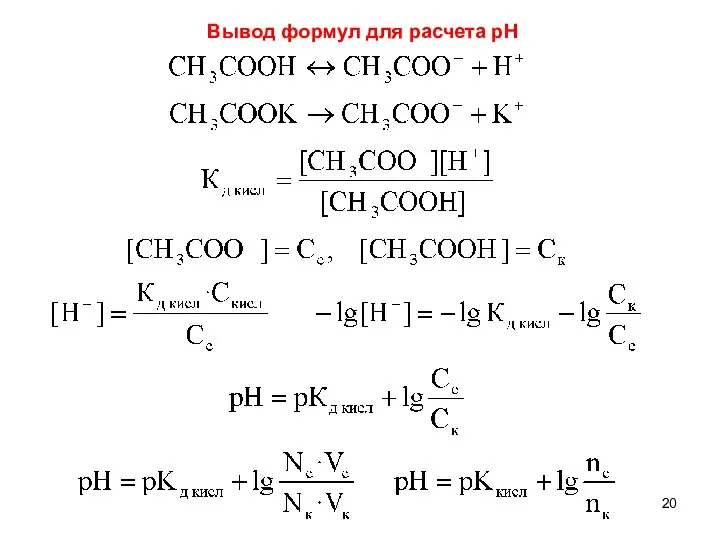
- 20. Вывод формул для расчета рН
- 21. Уравнение Гендерсона-Гассельбаха рН буферного раствора зависит от: Природы компонентов (рК слабой кислоты или основания) Соотношения концентраций
- 22. Уравнение нельзя применять : если концентрации компонентов отличаются более чем в 100 раз; если кислота (основание)
- 23. Соотношение компонентов 1:1 рН = рК Понятие «идеального» буферного раствора.
- 24. Одинаково хорошо противостоят как добавлению кислоты, так и добавлению щелочи Понятие «идеального» буферного раствора.
- 25. Влияние разбавления на рН буферного раствора (незначительно) ацетатный буферный раствор
- 26. Зона буферного действия
- 27. Приготовление буферных растворов с заданным значением рН Задача. Приготовить раствор с рН = 7,36. Необходимо изменить
- 28. Рассчитаем, во сколько раз концентрация соли должна быть больше:
- 29. Буферная ёмкость В – число моль-экв сильной кислоты или щелочи, которое нужно добавить к 1 л
- 30. От соотношения компонентов и максимальна при соотношении 1 /1
- 31. Буферные растворы, у которых рН (более кислое по отношению к рК) лучше противостоят добавлению щелочи. Буферная
- 32. Средние значения рН биологических жидкостей
- 33. Буферные системы крови Из кишечника и тканей в кровь при обмене веществ постоянно поступают различные кислоты:
- 34. Защитные функции по поддержанию постоянства рН выполняют 4 буферные системы: Бикарбонатная Фосфатная Белковая Гемоглобиновая
- 35. I. Бикарбонатная буферная система: С учётом растворенного СО2 (37oС)
- 36. Уравнение Гендерсона-Гассельбаха (для расчета рН крови) рСО2 – альвеолярное давление (парциальное давление СО2 воздуха, находящегося в
- 37. Поскольку [НСО3–]:[СО2]=20:1, а HCO3- работает против кислоты, бикарбонатная система имеет буферную емкость по кислоте значительно больше
- 38. Механизм действия бикарбонатной буферной системы При увеличении в крови концентрации ионов Н+ происходит выделение СO2, который
- 39. II. Фосфатная буферная система: К2НРО4 и КН2РО4 - в клетках Na2HPO4 и NaH2PO4- в плазме крови
- 40. Механизм действия При увеличении ионов Н+ во внутриклеточной жидкости, в результате переработки мясной пищи образующийся избыточный
- 41. Выведение тех или иных компонентов фосфатной буферной системы с мочой, в зависимости от перерабатываемой пищи, объясняет
- 42. III. Белковая буферная система: В результате ионизации аминогрупп и карбоксильных групп белки существуют в водных растворах
- 43. Механизм действия При добавлении сильной кислоты протон присоединяется к -СОO–- группе с образованием катиона R+: При
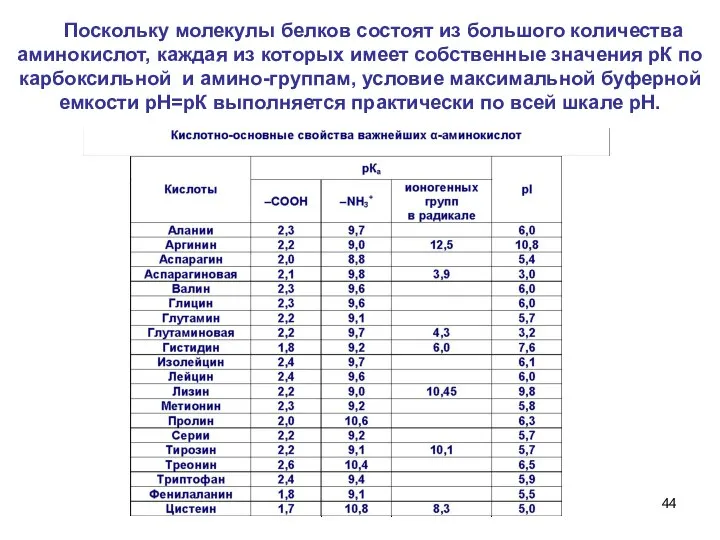
- 44. Поскольку молекулы белков состоят из большого количества аминокислот, каждая из которых имеет собственные значения рК по
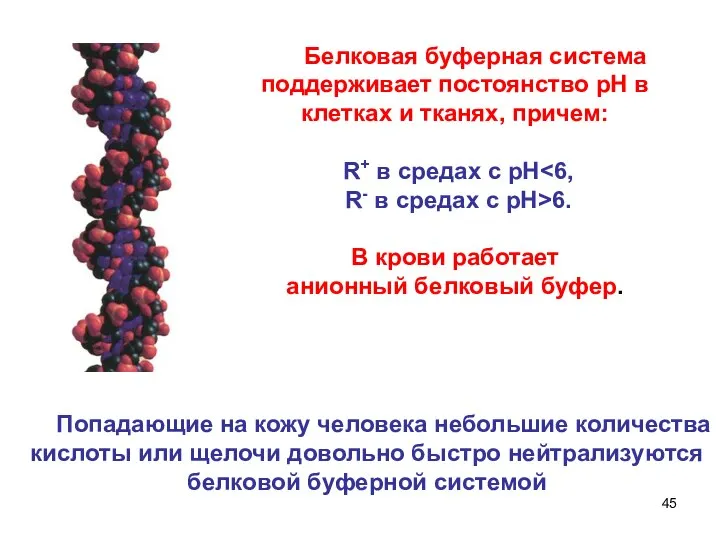
- 45. Белковая буферная система поддерживает постоянство рН в клетках и тканях, причем: R+ в средах с рН
- 46. IV. Гемоглобиновая буферная система: ~ 35 % общего буферного действия крови Гемоглобиновая H-Hb K-Hb венозная кровь
- 47. Оксигемоглобин более сильная кислота, чем гемоглобин! В легких идет процесс оксигенации: среда должна стать более кислой,
- 48. Среда должна стать более щелочной, но в реакцию вступает более сильная угольная кислота, образуя бикарбонат-ион, который
- 49. Заметим, что образование свободного СО2 при поступлении крови в легкие происходит за счет карбоангидразы эритроцитов, под
- 51. Все буферные системы организма обладают большей буферной емкостью по кислоте, чем по основанию, ( поскольку характеризуются
- 52. Ацидоз – накопление в организме кислых продуктов уменьшение рН крови в сравнении с нормой (уменьшение кислотной
- 53. норма † † † † рН≈7.40 некомпенсированный ацидоз комп. ацидоз комп. алкалоз некомпенсированный алкалоз норма Компенсированный
- 54. МЕТАБОЛИЧЕСКИЙ АЦИДОЗ Недостаток НСО3- или избыток нелетучих кислот в межклеточной жидкости Причины: введение или образование стойких
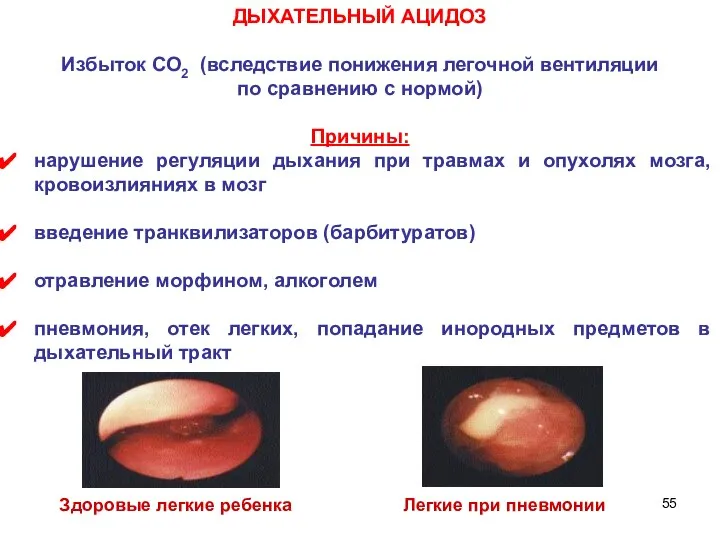
- 55. ДЫХАТЕЛЬНЫЙ АЦИДОЗ Избыток СО2 (вследствие понижения легочной вентиляции по сравнению с нормой) Причины: нарушение регуляции дыхания
- 56. ДЫХАТЕЛЬНЫЙ АЛКАЛОЗ Недостаток СО2 в связи с повышением легочной вентиляции, в сравнении с нормой. Причины: вдыхание
- 57. МЕТАБОЛИЧЕСКИЙ АЛКАЛОЗ Удаление кислот из организма или накопление НСО3- Причины: потеря Н+ при рвоте и кишечной
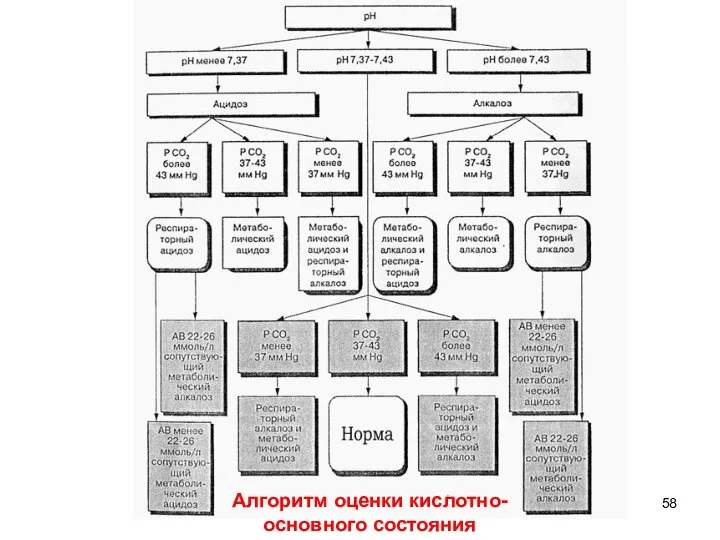
- 58. Алгоритм оценки кислотно- основного состояния
- 61. Щелочной резерв крови Число мл СО2, содержащееся в 100 мл крови (главным образом в виде гидрокарбонатов
- 62. Клинический анализ желудочного содержимого. Кислотность желудочного сока – количество мл 0,1 н раствора щелочи, необходимого для
- 64. Скачать презентацию






























![Поскольку [НСО3–]:[СО2]=20:1, а HCO3- работает против кислоты, бикарбонатная система имеет буферную](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1408512/slide-36.jpg)





















 Презентация по Химии "Методическая тема учителя химии и биологии" - скачать смотреть
Презентация по Химии "Методическая тема учителя химии и биологии" - скачать смотреть  Физические свойства металлов
Физические свойства металлов Моделирование химико-технологических процессов
Моделирование химико-технологических процессов Щелочные металлы
Щелочные металлы Основы безопасности при уничтожении химического оружия
Основы безопасности при уничтожении химического оружия Использование кинетики в фармации
Использование кинетики в фармации Нефть и ее роль в мировой экономике
Нефть и ее роль в мировой экономике Бескислородные керамические материалы
Бескислородные керамические материалы Классификация полимеров 11 класс Соловова Е.А., учитель химии высшей квалификационной категории, МОУ СОШ №15 г.Балашов, 2010
Классификация полимеров 11 класс Соловова Е.А., учитель химии высшей квалификационной категории, МОУ СОШ №15 г.Балашов, 2010 От простых правил к сложным структурам. Метод валентных связей. Принцип VSEPR
От простых правил к сложным структурам. Метод валентных связей. Принцип VSEPR Химическая лаборатрия. Химический состав растений
Химическая лаборатрия. Химический состав растений Экология микроорганизмов. (Лекция 8)
Экология микроорганизмов. (Лекция 8) Аттестационная работа. Методическая разработка программы для 5 классов: «Мир химии»
Аттестационная работа. Методическая разработка программы для 5 классов: «Мир химии» Культивирование растительных и животных клеток
Культивирование растительных и животных клеток Вакуумное фильтрование
Вакуумное фильтрование Спирты. Классификация, номенклатура, изомерия. Спирты в природе
Спирты. Классификация, номенклатура, изомерия. Спирты в природе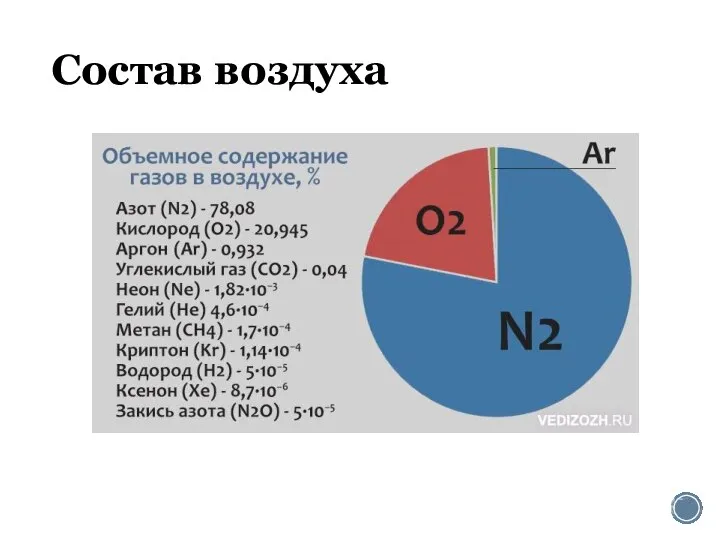 Состав воздуха. Азот
Состав воздуха. Азот Липиды. Фосфолипиды
Липиды. Фосфолипиды Химические методы определения U, Pu, Th
Химические методы определения U, Pu, Th Презентация по Химии "Оксид углерода (IV) - углекислый газ" - скачать смотреть
Презентация по Химии "Оксид углерода (IV) - углекислый газ" - скачать смотреть  «Углерод».
«Углерод». Весы. Камни Весов
Весы. Камни Весов Аналитические реакции
Аналитические реакции Химическая связь
Химическая связь Катализаторы для синтеза лекарственных препаратов и их строительных блоков
Катализаторы для синтеза лекарственных препаратов и их строительных блоков Презентация по Химии "Галогены в организме человека" - скачать смотреть
Презентация по Химии "Галогены в организме человека" - скачать смотреть 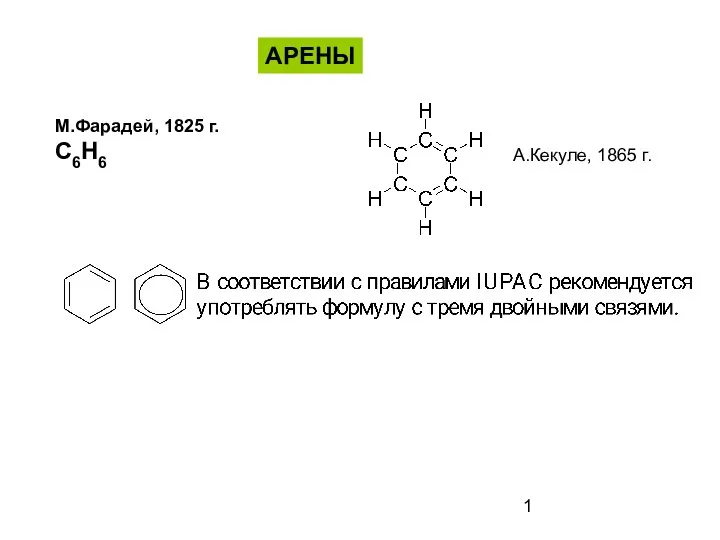 Ароматические соединения - арены
Ароматические соединения - арены Керамические материалы
Керамические материалы