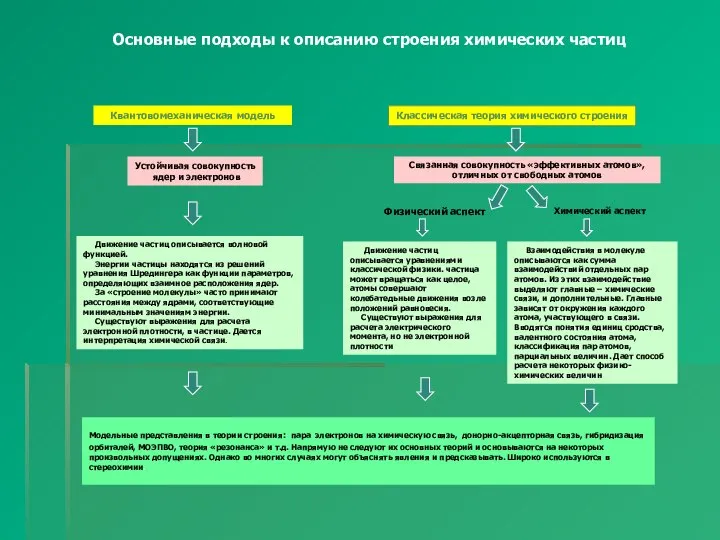
Основные подходы к описанию строения химических частиц
Квантовомеханическая модель
Классическая теория химического строения
Устойчивая
совокупность
ядер и электронов
Связанная совокупность «эффективных атомов»,
отличных от свободных атомов
Движение частиц описывается волновой функцией.
Энергии частицы находятся из решений уравнения Шредингера как функции параметров, определяющих взаимное расположения ядер.
За «строение молекулы» часто принимают расстояния между ядрами, соответствующие минимальным значениям энергии.
Существуют выражения для расчета электронной плотности, в частице. Дается интерпретация химической связи.
Физический аспект
Химический аспект
Движение частиц описывается уравнениями классической физики. частица может вращаться как целое, атомы совершают колебатедьные движения возле положений равновесия.
Существуют выражения для расчета электрического момента, но не электронной плотности
Взаимодействия в молекуле
описываются как сумма взаимодействий отдельных пар атомов. Из этих взаимодействие выделяют главные – химические связи, и дополнительные. Главные зависят от окружения каждого атома, участвующего в связи. Вводятся понятия единиц сродства, валентного состояния атома, классификация пар атомов, парциальных величин. Дает способ расчета некоторых физико-химических величин
Модельные представления в теории строения: пара электронов на химическую связь, донорно-акцепторная связь, гибридизация орбиталей, МОЭПВО, теория «резонанса» и т.д. Напрямую не следуют их основных теорий и основываются на некоторых произвольных допущениях. Однако во многих случаях могут объяснять явления и предсказывать. Широко используются в стереохимии.


 Фотометрический анализ
Фотометрический анализ Углеводы: моносахариды, дисахариды, полисахариды
Углеводы: моносахариды, дисахариды, полисахариды Мои НИОКР металлорганической химии против рака, Альцгеймера и Паркинсона
Мои НИОКР металлорганической химии против рака, Альцгеймера и Паркинсона Электродитическая диссоциация
Электродитическая диссоциация История открытия натурального каучука
История открытия натурального каучука Альдегиды и кетоны
Альдегиды и кетоны Презентация по Химии "Химия и реклама" - скачать смотреть
Презентация по Химии "Химия и реклама" - скачать смотреть  Новые требования, предъявляемые к лабораторно-минералогическим исследованиям
Новые требования, предъявляемые к лабораторно-минералогическим исследованиям Кислоты. Состав кислот
Кислоты. Состав кислот Химия и производство Химическая промышленность и химическая технология
Химия и производство Химическая промышленность и химическая технология Теория валентных связей
Теория валентных связей Общие свойства металлов МАОУ Домодедовский лицей №3 Разинькова Н.М.
Общие свойства металлов МАОУ Домодедовский лицей №3 Разинькова Н.М.  Строение атома и атомного ядра. Периодическая система химических элементов. (Часть 2)
Строение атома и атомного ядра. Периодическая система химических элементов. (Часть 2) Презентация по Химии "«Соединения бериллия»" - скачать смотреть _
Презентация по Химии "«Соединения бериллия»" - скачать смотреть _ Производные пиррола и индола. (Лекция 4)
Производные пиррола и индола. (Лекция 4) Глицерин Свойства - применение Выполнила учитель химии МОУ «Средняя школа №7» г. Балаково Саратовской области Трибунская Е
Глицерин Свойства - применение Выполнила учитель химии МОУ «Средняя школа №7» г. Балаково Саратовской области Трибунская Е Презентация по Химии "Химия элементов VIB подгруппы Cr, Mo, W" - скачать смотреть
Презентация по Химии "Химия элементов VIB подгруппы Cr, Mo, W" - скачать смотреть  Углеводы. Аэробный обмен. Глюконеогенез. Биосинтез глюкозаминогликанов. Механизмы регуляции уровня глюкозы в крови. (Тема 3)
Углеводы. Аэробный обмен. Глюконеогенез. Биосинтез глюкозаминогликанов. Механизмы регуляции уровня глюкозы в крови. (Тема 3) Наносеребрянные носки
Наносеребрянные носки ПРЕЗЕНТАЦИЯ «Химия и повседневная жизнь человека»
ПРЕЗЕНТАЦИЯ «Химия и повседневная жизнь человека»  Кислоты. Классификация кислот
Кислоты. Классификация кислот Мониторинги по химии
Мониторинги по химии ОГЭ №2, вопрос 1-16
ОГЭ №2, вопрос 1-16 Практические занятия по химии Можаев Г.М. 2008
Практические занятия по химии Можаев Г.М. 2008  Физические свойства алканов
Физические свойства алканов Ступенчатые процессы получения полимеров: полиприсоединение, поликонденсация
Ступенчатые процессы получения полимеров: полиприсоединение, поликонденсация Гидроксид натрия
Гидроксид натрия Партитуру химии надо не просто исполнить, ее надо сочинить! Жан-Мари Лен
Партитуру химии надо не просто исполнить, ее надо сочинить! Жан-Мари Лен