Содержание
- 2. Кто хочет съесть ядро ореха, должен расколоть его скорлупу плавт
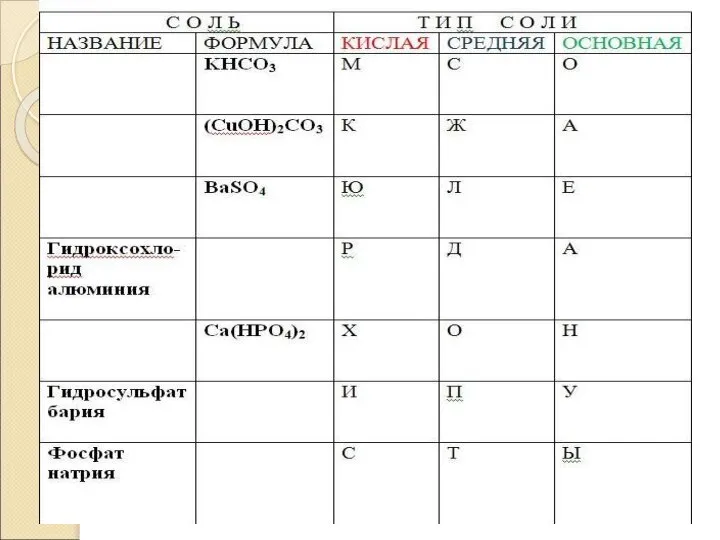
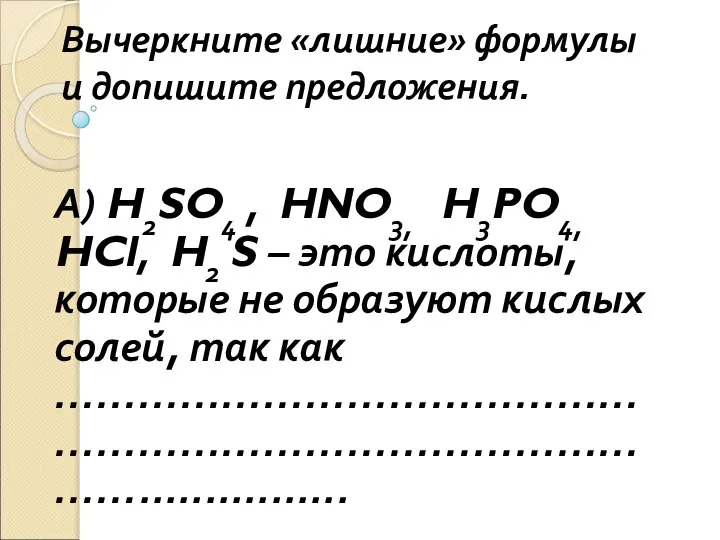
- 4. Вычеркните «лишние» формулы и допишите предложения. А) H2SO4 , HNO3, H3PO4, HCl, H2 S – это
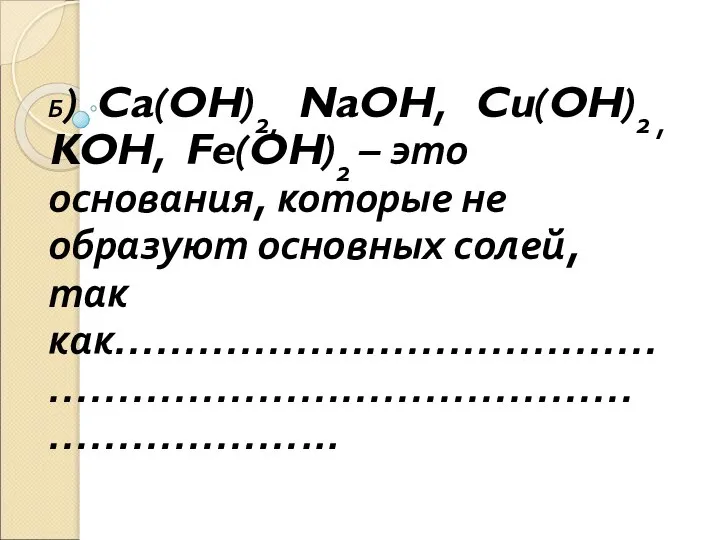
- 5. Б) Ca(OH)2, NaOH, Cu(OH)2 , KOH, Fe(OH)2 – это основания, которые не образуют основных солей, так
- 7. ХИМИЧЕСКИЕ СВОЙСТВА СОЛЕЙ
- 8. ТИПИЧНЫЕ РЕАКЦИИ СОЛЕЙ СОЛЬ+ КИСЛОТА= ДРУГАЯ СОЛЬ+ ДРУГАЯ КИСЛОТА
- 9. 2.СОЛЬ+ ЩЕЛОЧЬ= ДРУГАЯ СОЛЬ+ДРУГОЕ ОСНОВАНИЕ
- 10. 3.СОЛЬ1+СОЛЬ2=СОЛЬ3+СОЛЬ4
- 12. 4.СОЛЬ+ МЕТАЛЛ= ДРУГАЯ СОЛЬ+ ДРУГОЙ МЕТАЛЛ
- 13. эксперимент Железо + сульфат меди(II)= Железо + хлорид бария =
- 14. Н.Н БЕКЕТОВ В 1865г ИЗУЧИЛ СПОСОБНОСТЬ МЕТАЛЛОВ ВЫТЕСНЯТЬ ИЗ РАСТВОРОВ СОЛЕЙ ДРУГИЕ МЕТАЛЛЫ. НА ОСНОВЕ ЭТИХ
- 15. В 1892 Г В. НЕРНСТ ДОКАЗАЛ, ЧТО ВЫТЕСНИТЕЛЬНЫЙ РЯД ПРАКТИЧЕСКИ СОВПАДАЕТ С РЯДОМ В КОТОРОМ МЕТАЛЛЫ
- 16. ПРАВИЛА РЯДА НАПРЯЖЕНИЙ: МЕТАЛЛ ДОЛЖЕН НАХОДИТЬСЯВ РЯДУ НАПРЯЖЕНИЙ ДО МЕТАЛЛА СОЛИ; ОБЕ СОЛИ ДОЛЖНЫ БЫТЬ РАСТВОРИМЫМИ;
- 17. НАПИШИТЕ УРАВНЕНИЯ ВОЗМОЖНЫХ РЕАКЦИЙ K+ CuSO4 Cu + Hg(NO3)2 Fe + CuCl2 Al + ZnSO4 Zn
- 18. ХЛОРИД ЖЕЛЕЗА(III) + НИТРАТ СЕРЕБРА= НИТРАТ КАЛИЯ+ ХЛОРИД НАТРИЯ=
- 19. ГИДРОКСИД НАТРИЯ+ СУЛЬФИД ЖЕЛЕЗА(II)= ГИДРОКСИД КАЛИЯ + СУЛЬФАТ ЖЕЛЕЗА(III) =
- 20. Химические свойства солей с + кислоты = о + щелочи = л + соли = и
- 22. Скачать презентацию





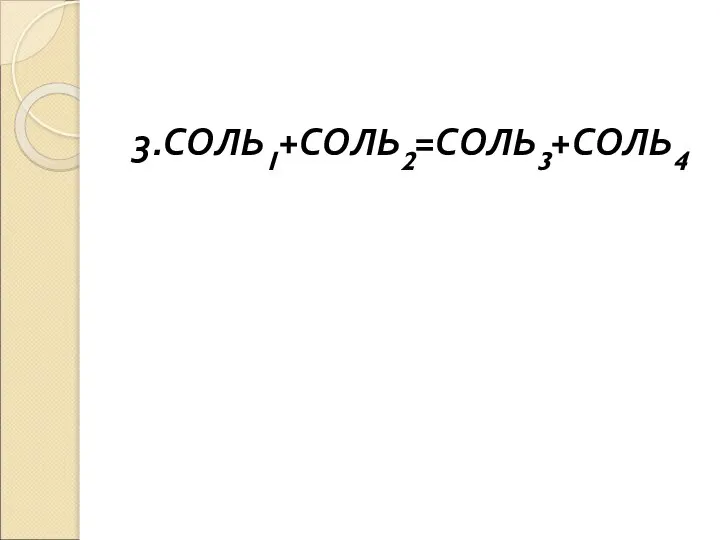










 Решение задачи №4. Старость - на радость. Команда «Карбораны»
Решение задачи №4. Старость - на радость. Команда «Карбораны» Практическое занятие по основам биохимии с методами клинико-биохимических исследований
Практическое занятие по основам биохимии с методами клинико-биохимических исследований Химия в повседневной жизни человека Подготовила: ученица 11А класса Галкина Светлана 2007г.
Химия в повседневной жизни человека Подготовила: ученица 11А класса Галкина Светлана 2007г. Бережём планету вместе. Нефть
Бережём планету вместе. Нефть Тест 1.Тип кристаллической решетки у белого фосфора…. а) молекулярный б) атомный в) ионный а) молекулярный Р4 2. У фосфора….. аллотропных модификаций а) две б) три в) четыре г) пять в) четыре – белый, черный, красный, фиолетовый 3.
Тест 1.Тип кристаллической решетки у белого фосфора…. а) молекулярный б) атомный в) ионный а) молекулярный Р4 2. У фосфора….. аллотропных модификаций а) две б) три в) четыре г) пять в) четыре – белый, черный, красный, фиолетовый 3. 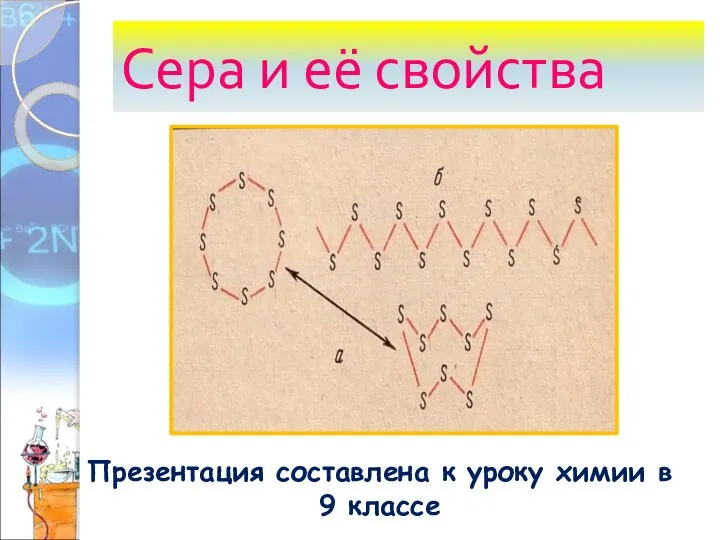 Сера и её свойства
Сера и её свойства  Аттестационная работа. Рабочая программа элективного курса по химии для 8 класса
Аттестационная работа. Рабочая программа элективного курса по химии для 8 класса Предмет термодинамики
Предмет термодинамики Оксиды (1 курс)
Оксиды (1 курс) ХИМИЧЕСКАЯ ТЕХНОЛОГИЯ ПРИРОДНЫХ ЭНЕРГОНОСИТЕЛЕЙ И УГЛЕРОДНЫХ МАТЕРИАЛОВ Преподаватель Левашова Альбина Ивановна, к.т.н. Франци
ХИМИЧЕСКАЯ ТЕХНОЛОГИЯ ПРИРОДНЫХ ЭНЕРГОНОСИТЕЛЕЙ И УГЛЕРОДНЫХ МАТЕРИАЛОВ Преподаватель Левашова Альбина Ивановна, к.т.н. Франци Оксид водорода (H2O)
Оксид водорода (H2O) Фізикохімічні характеристики фарб для волосся
Фізикохімічні характеристики фарб для волосся Электролиз. Электроды
Электролиз. Электроды Углерод и его соединения
Углерод и его соединения НЕМЕТАЛЛЫ АЗОТ
НЕМЕТАЛЛЫ АЗОТ  Нина Кара 24 группа коррозия металлов
Нина Кара 24 группа коррозия металлов Железо в периодической таблице химических элементов и строение его атома
Железо в периодической таблице химических элементов и строение его атома Классы неорганических соединений
Классы неорганических соединений Реология расплавов и растворов полимеров
Реология расплавов и растворов полимеров Презентация по Химии "Самородки." - скачать смотреть бесплатно_
Презентация по Химии "Самородки." - скачать смотреть бесплатно_ Химия: измерения
Химия: измерения Химия. Лекция 1. Термодинамика и кинетика
Химия. Лекция 1. Термодинамика и кинетика Углерод. Соединения углерода
Углерод. Соединения углерода Функции белков «Жизнь – это способ существования белковых тел». Ф.Энгельс
Функции белков «Жизнь – это способ существования белковых тел». Ф.Энгельс Хімія в житті суспульства
Хімія в житті суспульства Ионная химическая связь
Ионная химическая связь Презентация по Химии "Мышьяк – As" - скачать смотреть
Презентация по Химии "Мышьяк – As" - скачать смотреть  Выбор и назначение антибиотиков в соответствии со свойствами идентифицированного микроорганизма - возбудителя инфекции
Выбор и назначение антибиотиков в соответствии со свойствами идентифицированного микроорганизма - возбудителя инфекции