Содержание
- 2. План лекции Процессы на границе металл / вода, металл / раствор Электродный потенциал Уравнение Нернста Водородный
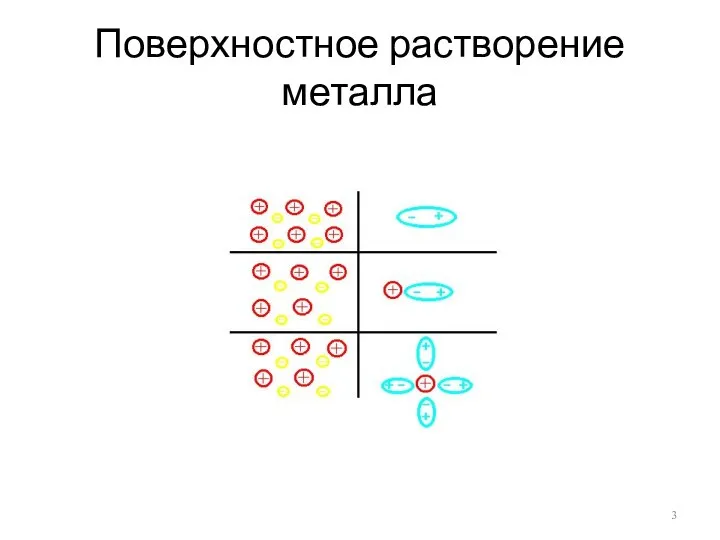
- 3. Поверхностное растворение металла
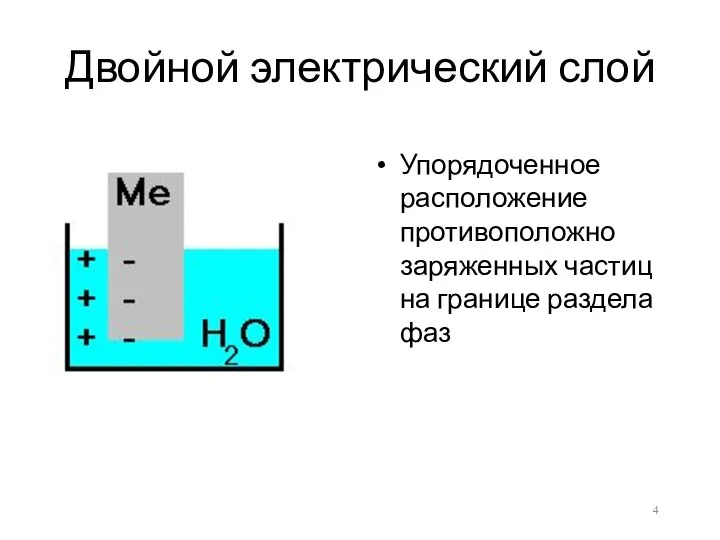
- 4. Двойной электрический слой Упорядоченное расположение противоположно заряженных частиц на границе раздела фаз
- 5. Устанавливается подвижное равновесие (скорость растворения = скорости осаждения) Образовавшаяся пограничная разность потенциалов получила название электродного потенциала
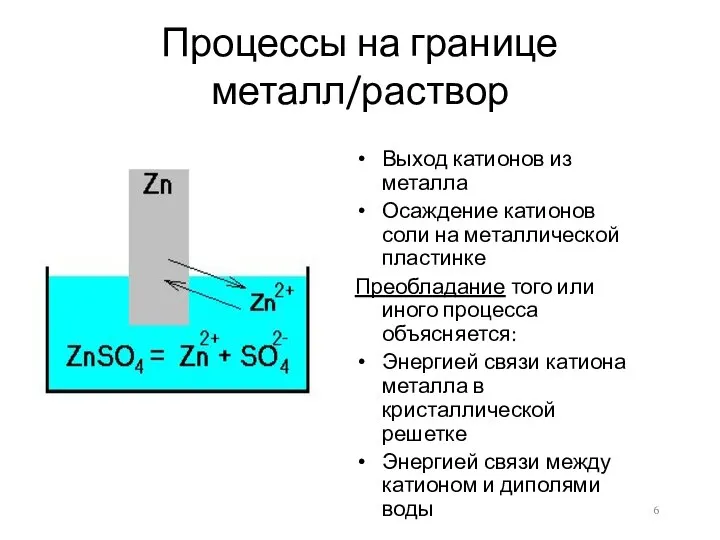
- 6. Процессы на границе металл/раствор Выход катионов из металла Осаждение катионов соли на металлической пластинке Преобладание того
- 7. Химически активные металлы (Zn, Mg, Al, Fe) характеризуются большими величинами растворимости. При любых больших концентрациях их
- 8. Уравнение Нернста 2,3RT 2,3RT E = ----------- ⋅ lgK + ---------- ⋅ lg a nF nF
- 9. Стандартный электродный потенциал (Е°) Потенциал, возникающий на границе металл / раствор при активности катионов металла в
- 10. Ряд напряжений Расположение металлов в порядке возрастания их стандартных электродных потенциалов
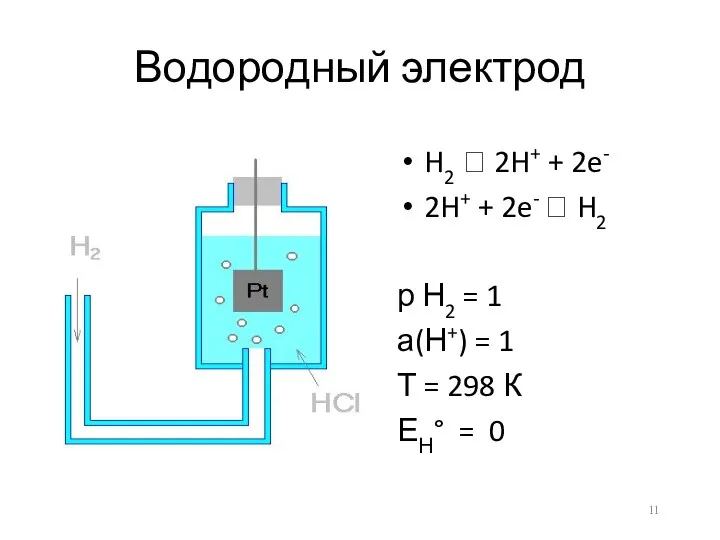
- 11. Водородный электрод H2 ⮀ 2H+ + 2e- 2H+ + 2e- ⮀ H2 р Н2 = 1
- 12. Недостатки стандартного водородного электрода Трудно изготавливать, сохранять и поддерживать в рабочем состоянии Водород должен быть химически
- 13. Названия электродов Анод – электрод, на котором протекает реакция окисления, т.е. отдача электронов; активный металл, заряд
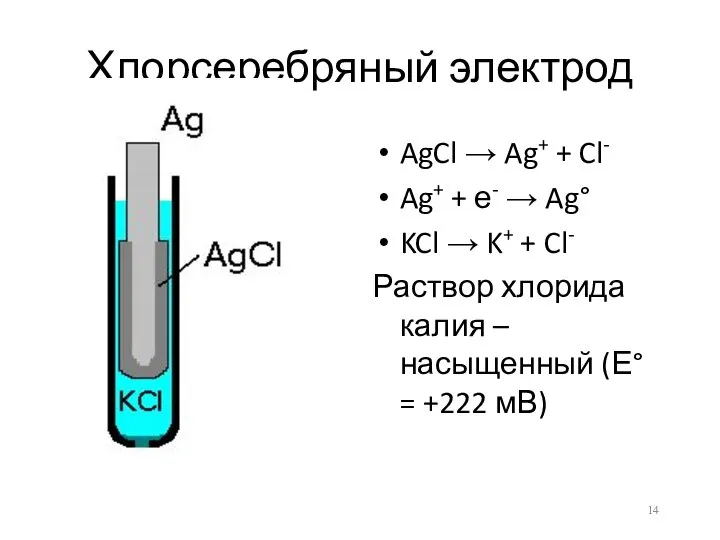
- 14. Хлорсеребряный электрод AgCl → Ag+ + Cl- Ag+ + е- → Ag° KCl → K+ +
- 15. Классификация электродов Электроды I типа Электродный потенциал создается на границе металл / раствор в результате окислительно-восстановительной
- 16. Ионометаллические электроды 1-го рода: электроды, обратимые относительно или катиона или аниона (цинковый, медный, газовые). Представляет собой
- 17. Окислительно-восстановительные электроды Электроды, в которых материал электрода в окислительно-восстановительном процессе не участвует; он является только переносчиком
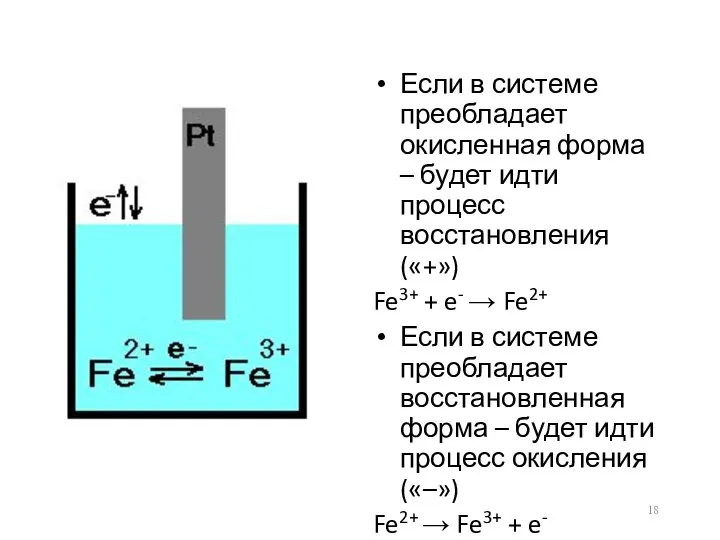
- 18. Если в системе преобладает окисленная форма – будет идти процесс восстановления («+») Fe3+ + e- →
- 19. Уравнение Нернста-Петерса 0,2Т [OX] Eо-в = Е°о-в + ---------- ⋅ lg----------- n [Red] n – количество
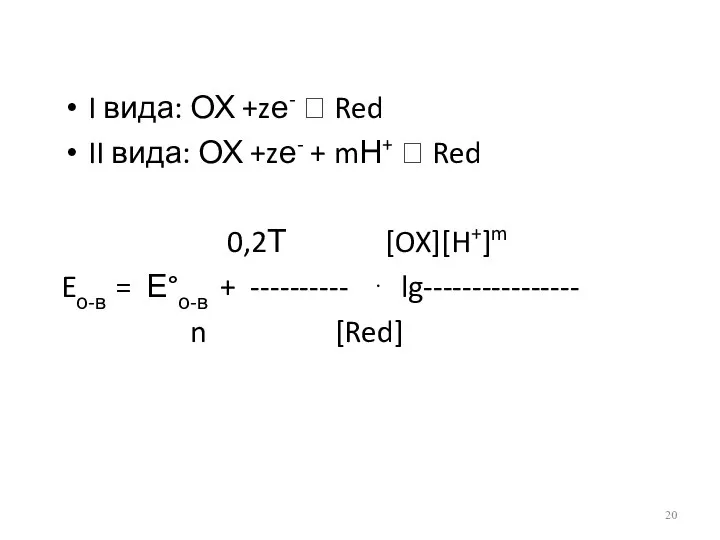
- 20. I вида: ОХ +zе- ⮀ Red II вида: ОХ +zе- + mН+ ⮀ Red 0,2Т [OX][H+]m
- 21. Электроды II типа Электродный потенциал возникает на границе раздела двух растворов, отделенных мембраной с избирательной проницаемостью
- 22. Стандартные О-В потенциалы Характеризуют способность системы функционировать в качестве окислителя или восстановителя
- 23. О-В системы в живых организмах 0,2Т [пируват][H+]2 Ео-в = Е°о-в + ----------- ⋅ lg------------------- 2 [лактат]
- 25. Скачать презентацию











![Уравнение Нернста-Петерса 0,2Т [OX] Eо-в = Е°о-в + ---------- ⋅ lg-----------](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1402913/slide-18.jpg)


![О-В системы в живых организмах 0,2Т [пируват][H+]2 Ео-в = Е°о-в +](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1402913/slide-22.jpg)
 Аттестационная работа. Выращивание кристаллов. Выявить условия, позволяющие из раствора медного купороса выращивать кристаллы
Аттестационная работа. Выращивание кристаллов. Выявить условия, позволяющие из раствора медного купороса выращивать кристаллы Ցեմենտի արտադրություն
Ցեմենտի արտադրություն Ученые – химики в годы Великой Отечественной войны
Ученые – химики в годы Великой Отечественной войны Кремний и его соединения
Кремний и его соединения Аллотропия. Аллотропные модификации
Аллотропия. Аллотропные модификации ЗОЛОТОЙ ВЕК ГОЛЛАНДСКОЙ ЖИВОПИСИ
ЗОЛОТОЙ ВЕК ГОЛЛАНДСКОЙ ЖИВОПИСИ  Кристаллдық және аморфтық күй
Кристаллдық және аморфтық күй Углерод. Металлы. 9 класс
Углерод. Металлы. 9 класс А.Д. Сахаров – выдающийся ученый и правозащитник современности МБОУ «Гимназия № 13», 9 «Б» класс. Выполнил: Артёмов Александр. На
А.Д. Сахаров – выдающийся ученый и правозащитник современности МБОУ «Гимназия № 13», 9 «Б» класс. Выполнил: Артёмов Александр. На Аналитическая химия. Качественный анализ
Аналитическая химия. Качественный анализ Окислительно-восстановительные реакции. Электролиз
Окислительно-восстановительные реакции. Электролиз Токсичность. Параметры токсичности
Токсичность. Параметры токсичности Электронное строение атома
Электронное строение атома Разработка технологии получения наноструктурированных катализаторов для гидрирования
Разработка технологии получения наноструктурированных катализаторов для гидрирования Синтетические моющие средства
Синтетические моющие средства Металловедение. Основные типы диаграмм состояния двойных сплавов. (Лекция 4)
Металловедение. Основные типы диаграмм состояния двойных сплавов. (Лекция 4) Строение и функции отдельных коферментов
Строение и функции отдельных коферментов Сравнительная характеристика бензольного кольца и олимпийских колец
Сравнительная характеристика бензольного кольца и олимпийских колец Щелочноземельные металлы
Щелочноземельные металлы Галогены: Хлор, бром, иод
Галогены: Хлор, бром, иод Путешествие по континенту Химия. Познавательная игра по химии, 8 класс
Путешествие по континенту Химия. Познавательная игра по химии, 8 класс Эластомеры (резины)
Эластомеры (резины) Презентация по Химии "«Щелочные металлы»" - скачать смотреть
Презентация по Химии "«Щелочные металлы»" - скачать смотреть  Химиялық элемент алюминий
Химиялық элемент алюминий Строение атома. Атомные орбитали. Типы связей. Основные органогенные элементы, их роль
Строение атома. Атомные орбитали. Типы связей. Основные органогенные элементы, их роль Аминокислоты и белки
Аминокислоты и белки λ-MnO2 as material with pseudocapacitive properties
λ-MnO2 as material with pseudocapacitive properties Галогены - друзья или враги?
Галогены - друзья или враги?