Содержание
- 2. Ранние модели строения атома «Пудинг с изюмом» (1902-1904 г. Дж. Томсон) «Планетарная» (1907 г. Э. Резерфорд)
- 3. Современная модель атома Атом – электронейтральная частица Ядро атома – положительно заряженное Электроны – отрицательно заряженные
- 4. Состав ядра атома Протоны. Масса = 1, заряд = +1 Нейтроны. Масса = 1, заряд =
- 5. Изотопы Изотопы – совокупность атомов, имеющих одинаковое число протонов, но различающихся количеством нейтронов в ядре атома.
- 6. Частицы микромира Корпускулярно-волновой дуализм Электрон – частица с массой m1= 9*10-28, скорость 108 см/сек, заряд -1
- 7. Важные понятия Электронное облако – пространство около ядра атома, где сосредоточены вся масса электрона и электронная
- 8. Квантовые числа Квантовые числа описывают состояние электрона в атоме n – главное квантовое число, хар-т общую
- 9. Квантовые числа l – побочное квантовое число; уточняет запас энергии электрона на энергетическом уровне, хар-т связь
- 11. Квантовые числа m1 – магнитное орбитальное квантовое число соответствует распределению АО в пространстве около ядра Определяет
- 12. Квантовые числа ms – магнитное спиновое квантовое число характеризует чисто квантовое свойство электрона Это собственный момент
- 13. Принципы заполнения электронных оболочек Принцип минимальной энергии: принцип Паули правило Хунда правило Клечковского
- 14. Несоблюдение принципа Паули При несоблюдении принципа Паули на АО в атоме были бы электроны с одинаковыми
- 15. Несоблюдение правила Хунда При несоблюдении правила Хунда суммарный спин не будет максимальным, а это соответствует большему
- 16. Правило Клечковского Заполнение электронами орбиталей в атоме происходит в порядке возрастания суммы главного и орбитального квантовых
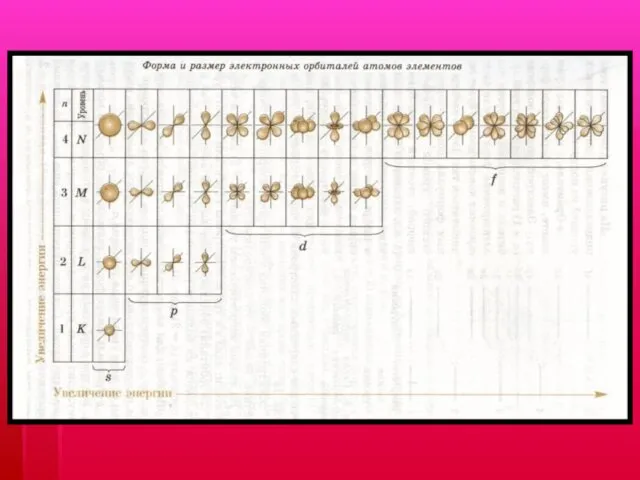
- 17. Электронные семейства s-элементы, если заполняется s-подуровень p-элементы, если заполняется p-подуровень d-элементы, если заполняется d-подуровень f-элементы, если
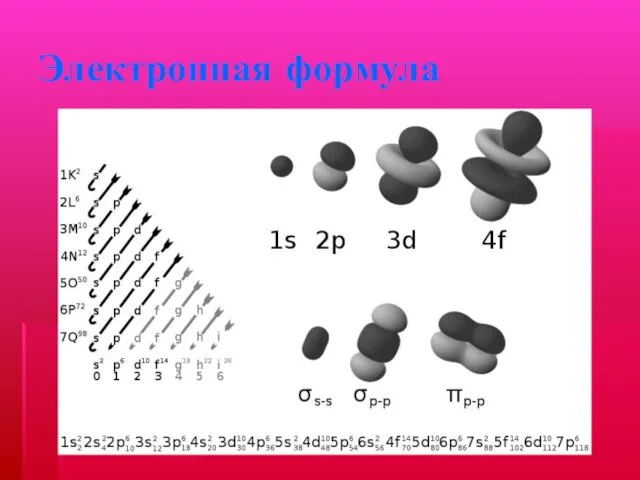
- 18. Электронная формула Электронная формула атома химического элемента показывает как распределяются электроны в атоме, учитывая их характеистику
- 19. Электронная формула
- 20. «Провал» электрона В атомах некоторых элементов электрон с s-подуровня внешнео энергетического уровня переходит на d-подуровень предвнешнего
- 21. Задание Определить элемент: Составить электронные и электронно-графические формулы элемента:
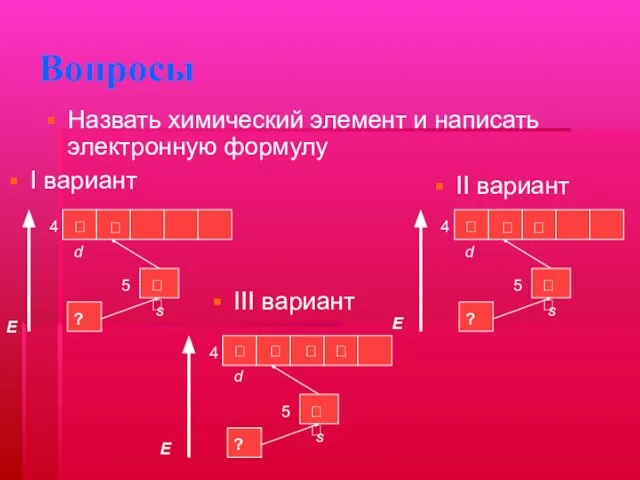
- 22. Вопросы I вариант Назвать химический элемент и написать электронную формулу III вариант
- 24. Скачать презентацию


















 Химическое строение рецепторов и лигандов. Агонисты и антогонисты, принцип структурной комплементарности
Химическое строение рецепторов и лигандов. Агонисты и антогонисты, принцип структурной комплементарности Депонирование и мобилизация жиров
Депонирование и мобилизация жиров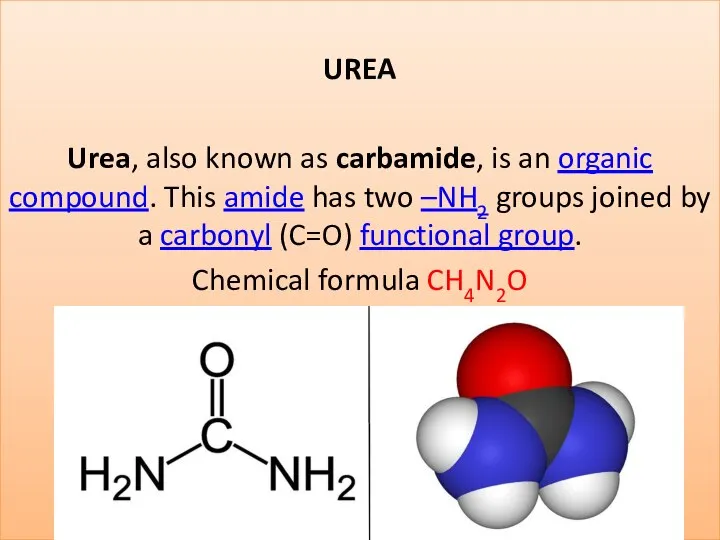 Urea (carbamide)
Urea (carbamide) Использование QR-кода в обучении химии
Использование QR-кода в обучении химии Введение в минералогию. Генезис минералов
Введение в минералогию. Генезис минералов Вплив радіонуклідів Радіоактивне випромінювання небезпечне тим, що воно невидиме, не має ні запаху, ні смаку, тому людина його нія
Вплив радіонуклідів Радіоактивне випромінювання небезпечне тим, що воно невидиме, не має ні запаху, ні смаку, тому людина його нія Аттестационная работа. Использование цифровой лаборатории «Архимед» во внеурочной деятельности по химии
Аттестационная работа. Использование цифровой лаборатории «Архимед» во внеурочной деятельности по химии Энергетика химических реакций. Элементы химической термодинамики
Энергетика химических реакций. Элементы химической термодинамики Третья группа ПС
Третья группа ПС Стратегия успеха 2 (ЕГЭ). Органическая химия
Стратегия успеха 2 (ЕГЭ). Органическая химия Кінетика хімічних реакцій і хімічна рівновага
Кінетика хімічних реакцій і хімічна рівновага Геология и геохимия нефти и газа
Геология и геохимия нефти и газа Презентация по Химии "Бинарные соединения" - скачать смотреть
Презентация по Химии "Бинарные соединения" - скачать смотреть  Конкурс интерактивных презентаций «Интерактивная мозаика» автор: Кудрявцева Ирина Александровна МОУ «Средняя общеобразова
Конкурс интерактивных презентаций «Интерактивная мозаика» автор: Кудрявцева Ирина Александровна МОУ «Средняя общеобразова Періодичний закон і система хімічних елементів Д.І.Менделєєва. Будова атома.
Періодичний закон і система хімічних елементів Д.І.Менделєєва. Будова атома. 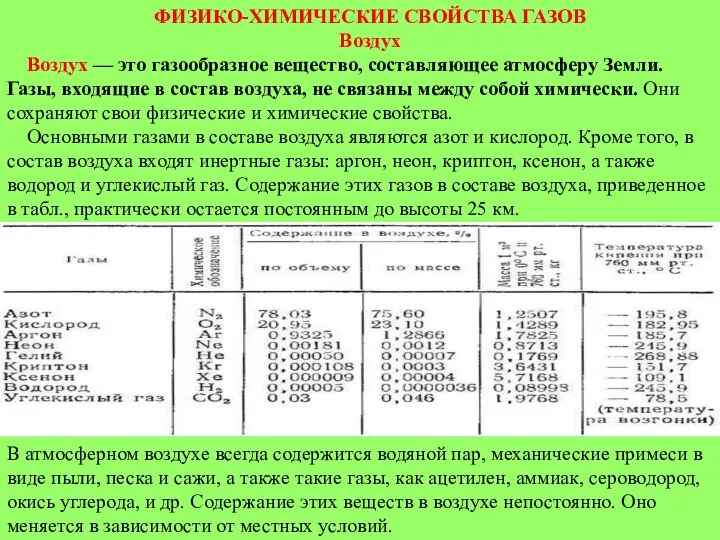 Физико-химические свойства газов
Физико-химические свойства газов Мягкие лекарственные формы. Мази, капсулы, суппозитории, пластыри
Мягкие лекарственные формы. Мази, капсулы, суппозитории, пластыри Химическое оружие
Химическое оружие Практическая работа №1 Признаки химических реакций
Практическая работа №1 Признаки химических реакций Важнейшие кислоты и кислотные остатки. (Леция 1)
Важнейшие кислоты и кислотные остатки. (Леция 1) Коллоидные ПАВ
Коллоидные ПАВ Введение в специальность. Химическая технология
Введение в специальность. Химическая технология Physical chemistry of nanostructured systems.( lecture no. 7)
Physical chemistry of nanostructured systems.( lecture no. 7) Природные источники углеводородов
Природные источники углеводородов Сабақтың тақырыбы: донорлыакцепторлы байланыс. Комплексті қосылыстар
Сабақтың тақырыбы: донорлыакцепторлы байланыс. Комплексті қосылыстар Строение вещества
Строение вещества Искусственные или технические битумы
Искусственные или технические битумы Тема урока: СЕРНАЯ КИСЛОТА И ЕЁ СВОЙСТВА
Тема урока: СЕРНАЯ КИСЛОТА И ЕЁ СВОЙСТВА