Содержание
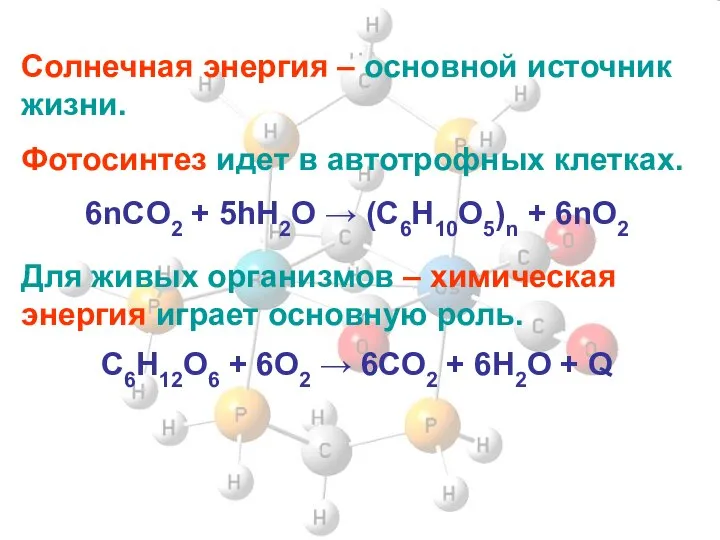
- 2. Солнечная энергия – основной источник жизни. Фотосинтез идет в автотрофных клетках. 6nCO2 + 5hH2O → (C6H10O5)n
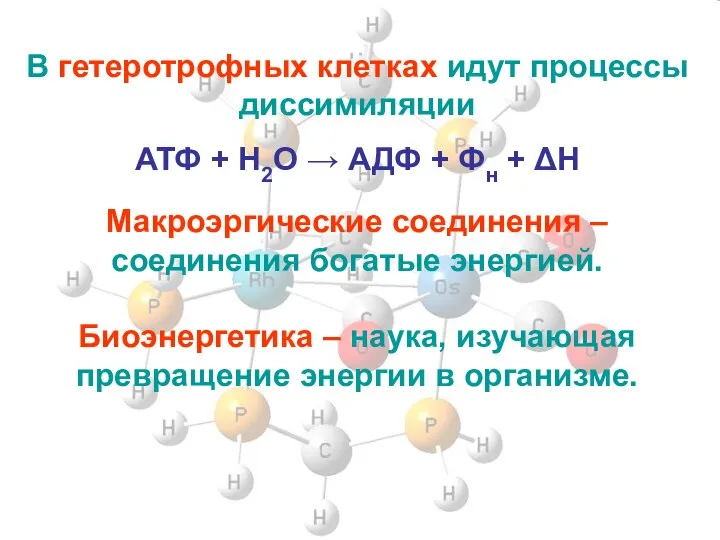
- 3. В гетеротрофных клетках идут процессы диссимиляции АТФ + H2O → АДФ + Фн + ΔH Макроэргические
- 4. Химическая термодинамика – наука о взаимопревращениях теплоты и энергии, в том числе энергии химических процессов (середина
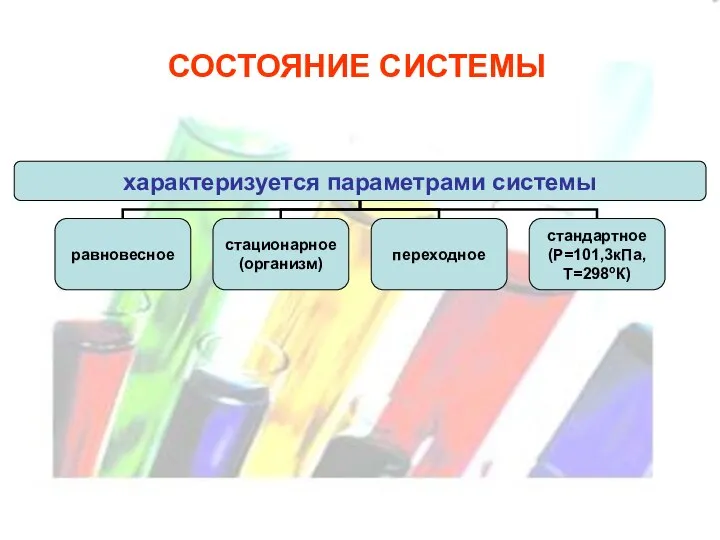
- 6. СОСТОЯНИЕ СИСТЕМЫ
- 8. Энергия – мера движения и взаимодействия материальных систем
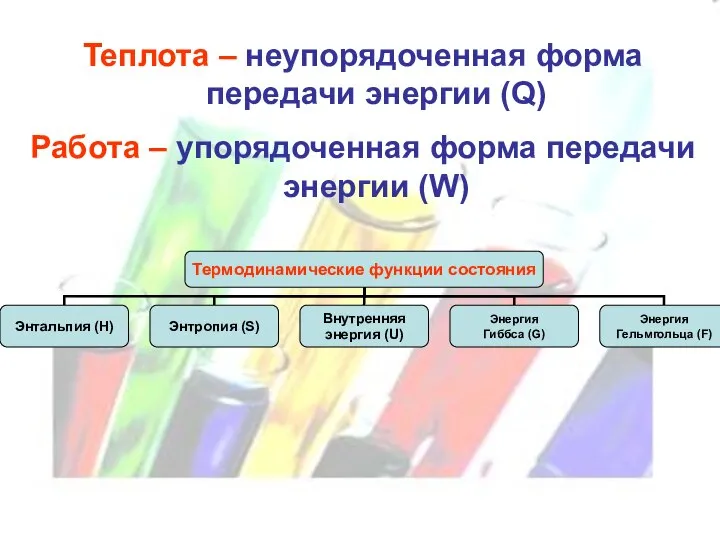
- 9. Теплота – неупорядоченная форма передачи энергии (Q) Работа – упорядоченная форма передачи энергии (W)
- 10. I начало (закон) термодинамики (Р. Майер, Д. Джоуль, Г.Л. Гельмгольц) Это закон сохранения энергии Энергия не
- 11. Q = ΔU + W Для изобарного процесса W = pΔV Qp = ΔU + pΔV
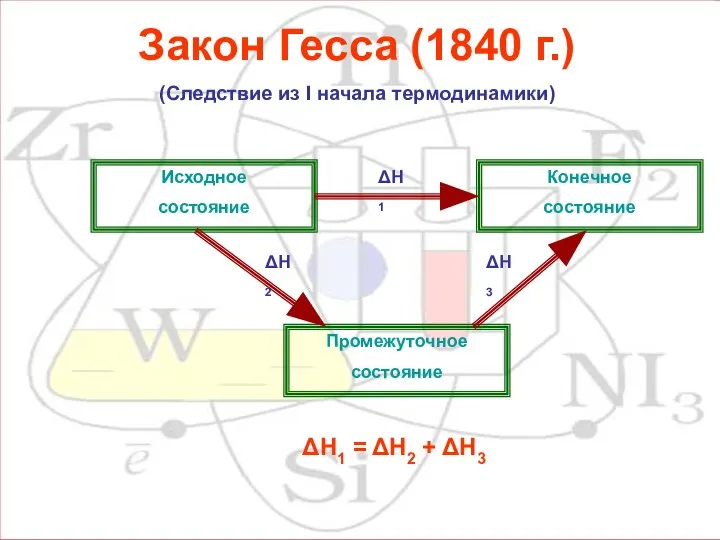
- 12. Закон Гесса (1840 г.) (Следствие из I начала термодинамики) Конечное состояние Исходное состояние Промежуточное состояние ΔН1
- 13. Следствие из закона Гесса (следствие из I начала термодинамики) ΔНор-ии = Σm⋅ΔНообр.(прод.) - Σn⋅ΔНообр.(исх.в-в) ΔНор-ии =
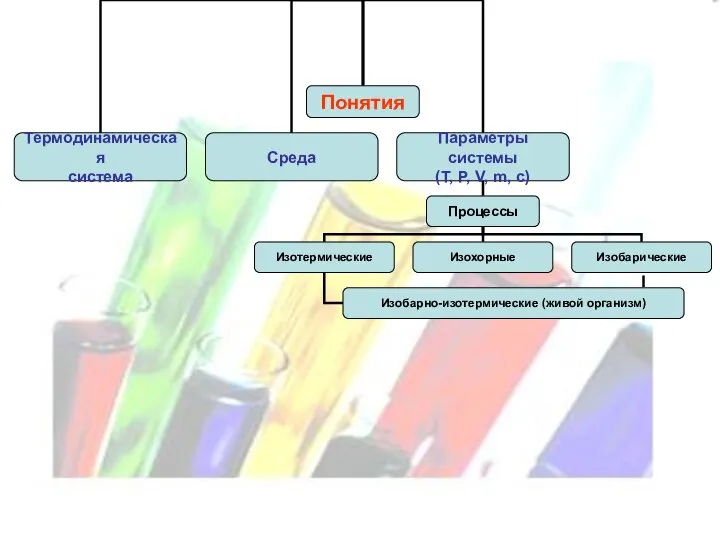
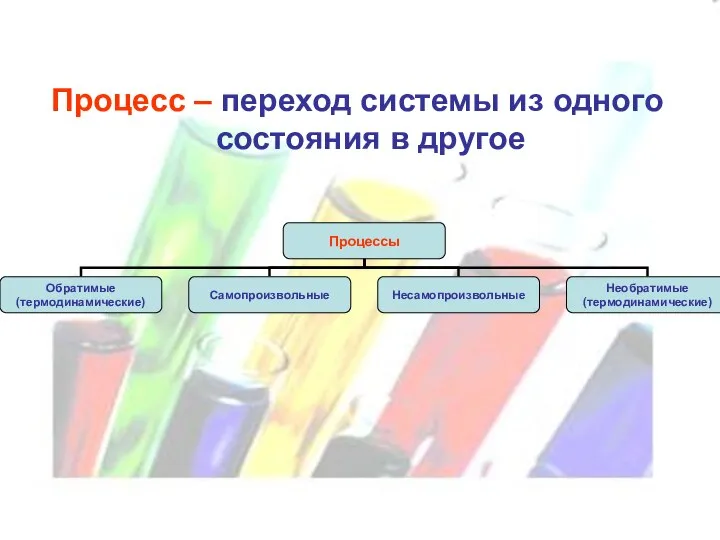
- 14. Процесс – переход системы из одного состояния в другое
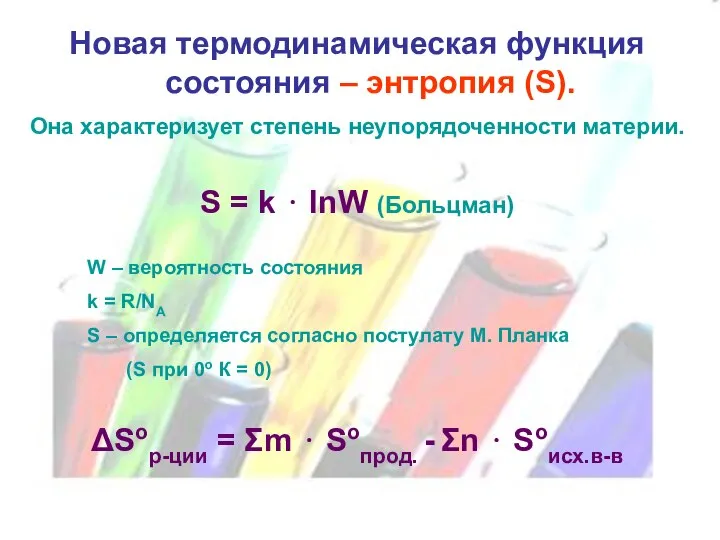
- 15. Новая термодинамическая функция состояния – энтропия (S). Она характеризует степень неупорядоченности материи. S = k ⋅
- 16. II начало (закон) термодинамики Невозможен самопроизвольный переход тепла от тела менее нагретого к телу более нагретому.
- 17. ∆Sобр = Qобр. / Т или в общем виде ∆S ≥ Q / T, т.е. ∆S
- 18. Д.У. Гиббс – новая функция состояния (G) – энергия Гиббса (изобарно-изотермический потенциал) ∆G = ∆H -
- 19. Для неизолированных систем самопроизвольное протекание процессов характеризуется: Энтальпийным фактором (∆Н) Энтропийным фактором (∆S)
- 20. Направленность протекания процессов
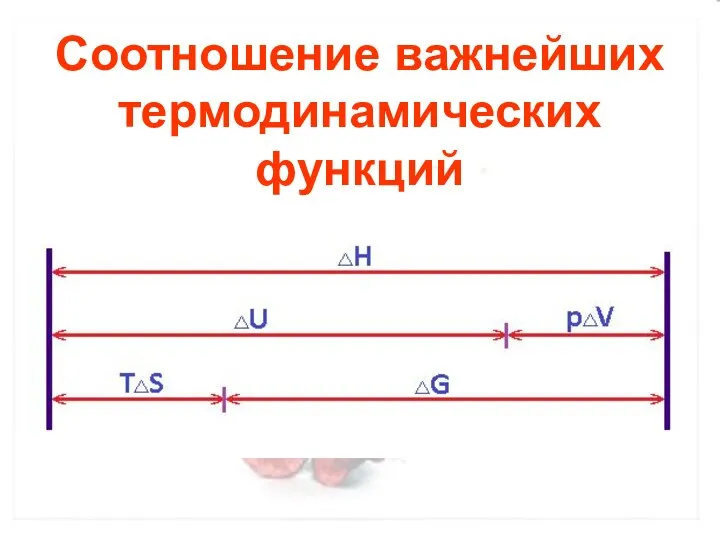
- 21. Соотношение важнейших термодинамических функций
- 22. Экзергонические реакции –∆G Эндергонические реакции –∆G > 0
- 23. Принцип энергетического сопряжения Энергия, необходимая для протекания эндергонических реакций, поступает за счет осуществления экзергонических реакций. Интермедиат
- 24. АТФ + Н2О ↔ АДФ + Н3РО4 ∆Gо = -29,2 кДж/моль Экзергоническая реакция С6Н12О6 + Н3РО4
- 25. Применение химической термодинамики к биологическим системам
- 26. Применение I начала термодинамики Термодинамические условия равновесия. Энергия Гиббса биологического окисления вещества Экзергонические и эндергонические реакции
- 28. Точность – 99% 1 г жира – 9,3 ккал 1 г углевода и белка – 4,2
- 29. Вывод: Организм не является источником энергии, а полностью подчиняется I началу термодинамики
- 30. 2-ое начало термодинамики: ΔS≥0 и ΔG≤0 Состояние равновесия: ΔS=0 и ΔG=0 Химический потенциал (Гиббс): (на 1
- 31. Может ли живой организм производить работу только за счет теплоты окружающей среды? Ответ: Прямых доказательств нет.
- 32. Играет ли увеличение энтропии определяющую роль в направлении химических процессов обмена в биосистемах? Ответ: Энтропия всей
- 33. Могут ли живые организмы использовать молекулярные отклонения в отношении уменьшения энтропии? Ответ: До сих пор известен
- 34. Применима ли к биосистемам обычная трактовка энтропии как меры упорядоченности? Ответ: Применительно к биосистемам различают: 1.
- 35. Итак, ответ на все вопросы отрицательный. Биосистема и биохимия имеют дело не с равновесными, а со
- 36. Окисление углеводов (аэробный распад) имеет большое значение в энергетическом балансе организма С6Н12О6 тв + 6О2 газ
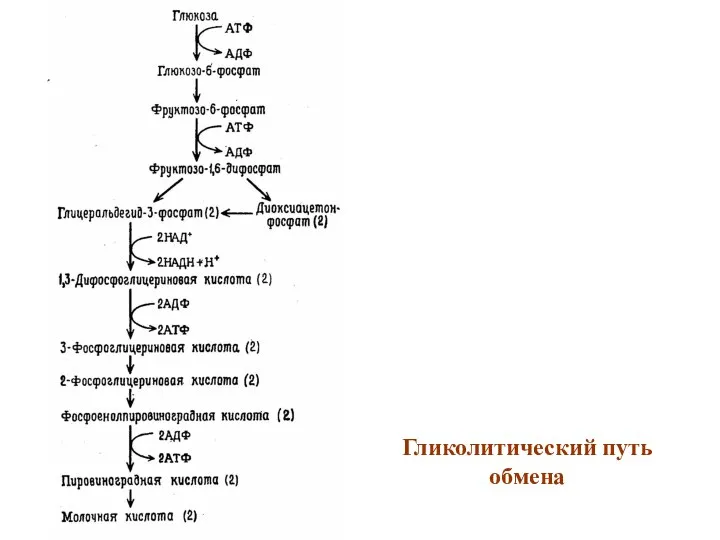
- 37. Гликолитический путь обмена
- 39. Окислительный распад жирных кислот – второй источник (после углеводов) энергии в организме. Этот процесс локализован в
- 40. В заключительной стадии под влиянием фермента кетотиолазы образуются ацетилкоэнзим и, новая молекула коэнзима А, вновь активированная
- 41. Рассмотрим образцы калориметров, используемых в разные века.
- 48. Вакуумный адиабатический калориметр
- 49. Дифференциальный сканирующий калориметр с программным управлением фирмы «СЕТАРАМ»
- 51. Скачать презентацию



















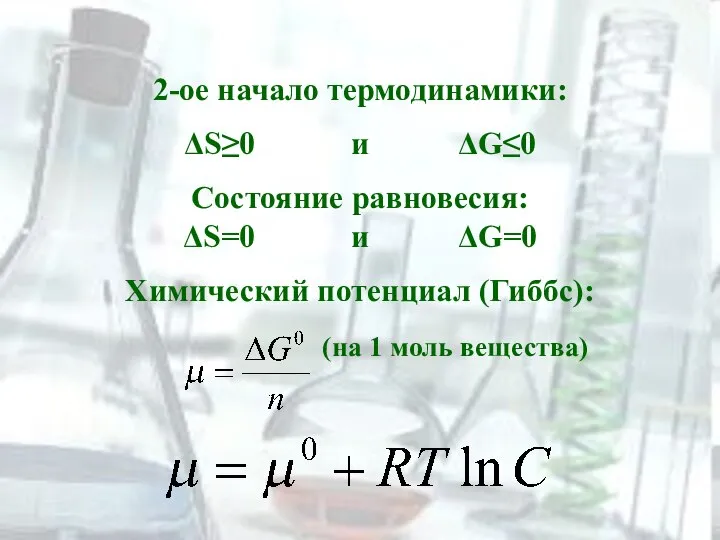


















 Классификация органических реакций в органической химии
Классификация органических реакций в органической химии Группа веществ, изолируемых из биологического материала экстракцией и сорбцией. (Лекция 6)
Группа веществ, изолируемых из биологического материала экстракцией и сорбцией. (Лекция 6) Выполнил ученик 11-б класса МОУ СОШ №41 Гандилян Армен Руководитель: Изместьева Н.Д. Красноярск
Выполнил ученик 11-б класса МОУ СОШ №41 Гандилян Армен Руководитель: Изместьева Н.Д. Красноярск  Методы диффузионной металлизации
Методы диффузионной металлизации Хлор
Хлор Антидиабеттік қауынқұрттың реологиялық қасиетін анықтау
Антидиабеттік қауынқұрттың реологиялық қасиетін анықтау Галогены
Галогены Введение в термические процессы вторичной переработки нефти
Введение в термические процессы вторичной переработки нефти Химия элементов VIA группы. Сера
Химия элементов VIA группы. Сера Физические свойства фтороводорода
Физические свойства фтороводорода Окисно-відновні реакції та їхнє значення
Окисно-відновні реакції та їхнє значення Презентация по Химии "Путешествие по стране карбонатов" - скачать смотреть
Презентация по Химии "Путешествие по стране карбонатов" - скачать смотреть  Химическая промышленность
Химическая промышленность Белки, протеины, полипептиды
Белки, протеины, полипептиды Оценка срока службы для полимерных материалов методами термического анализа
Оценка срока службы для полимерных материалов методами термического анализа Модельные представления силикатных структур
Модельные представления силикатных структур Structural revision of (+)-uprolide F diacetate confirmed by asymmetric total synthesis
Structural revision of (+)-uprolide F diacetate confirmed by asymmetric total synthesis Азот. Соединения азота
Азот. Соединения азота Охорона навколишнього середовища від забруднень при переробці вуглеводневої сировини та використання продуктів її переробки
Охорона навколишнього середовища від забруднень при переробці вуглеводневої сировини та використання продуктів її переробки  Растворы электролитов
Растворы электролитов Предельные углеводороды. Алканы
Предельные углеводороды. Алканы Предельные углеводороды
Предельные углеводороды Химическое загрязнение атмосферы
Химическое загрязнение атмосферы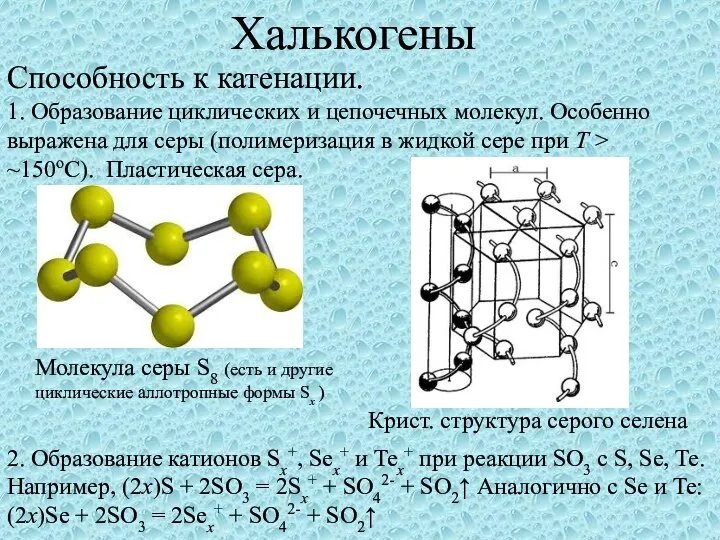 Халькогены. Способность к катенации
Халькогены. Способность к катенации Алюминиевые сплавы
Алюминиевые сплавы Алкины. Физические и химические свойства
Алкины. Физические и химические свойства Кислоты, их состав, свойства и применение
Кислоты, их состав, свойства и применение Презентация к уроку по теме: «Алканы» Учитель химии Колесникова Г.Т.
Презентация к уроку по теме: «Алканы» Учитель химии Колесникова Г.Т.