Содержание
- 2. Энзимология Основу всех жизненных процессов составляют тысячи химических реакций, катализируемых ферментами (энзимами). Нарушения в работе ферментов
- 3. Суть действия ферментов По своей функции ферменты являются биологическими катализаторами. Сущность действия ферментов, так же как
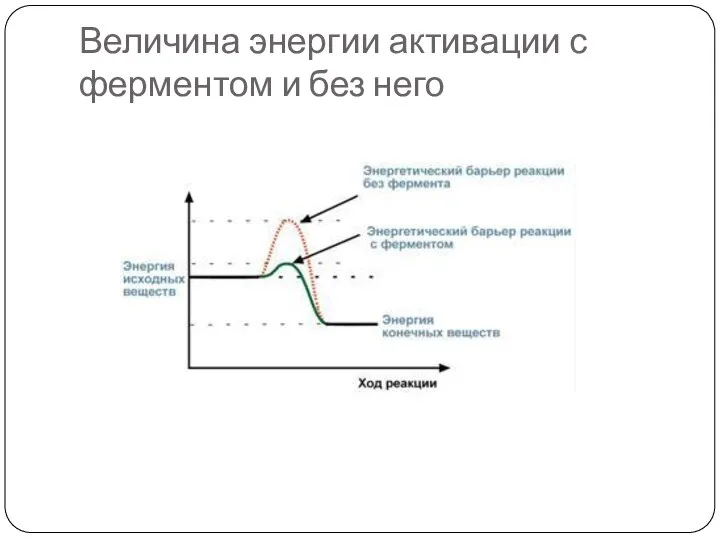
- 4. Величина энергии активации с ферментом и без него
- 5. Сходство и отличия ферментов и неорганических катализаторов Сходство 1. Катализируют только энергетически возможные реакции. 2. Не
- 6. Этапы катализа В ферментативной реакции можно выделить следующие этапы: 1. Присоединение субстрата (S) к ферменту (E)
- 7. Механизмы катализа 1. Кислотно-основной катализ – в активном центре фермента находятся группы специфичных аминокислотных остатков, которые
- 9. Типы ферментативных реакций 1. Тип "пинг-понг" – фермент сначала взаимодействует с субстратом А, отбирая у него
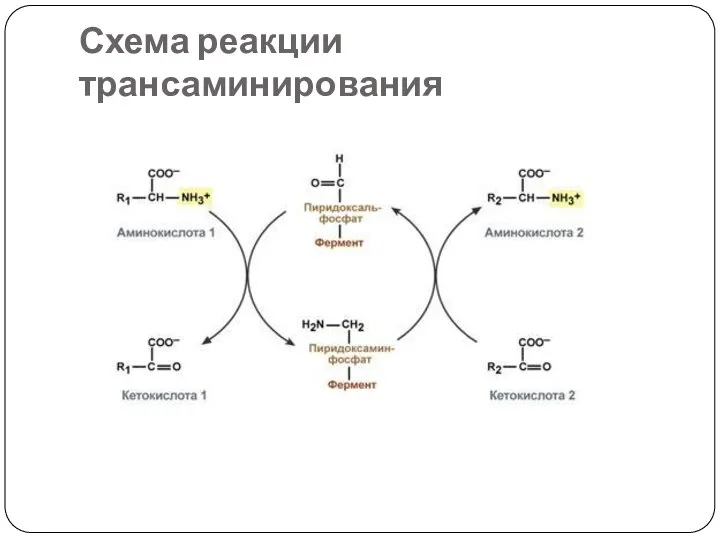
- 10. Схема реакции трансаминирования
- 11. 2. Тип последовательных реакций – к ферменту последовательно присоединяются субстраты А и В, образуя "тройной комплекс",
- 12. 3. Тип случайных взаимодействий – субстраты А и В присоединяются к ферменту в любом порядке, неупорядоченно,
- 13. Ферменты как белки Все ферменты являются белками и обладают всеми свойствами белков. Поэтому подобно белкам ферменты
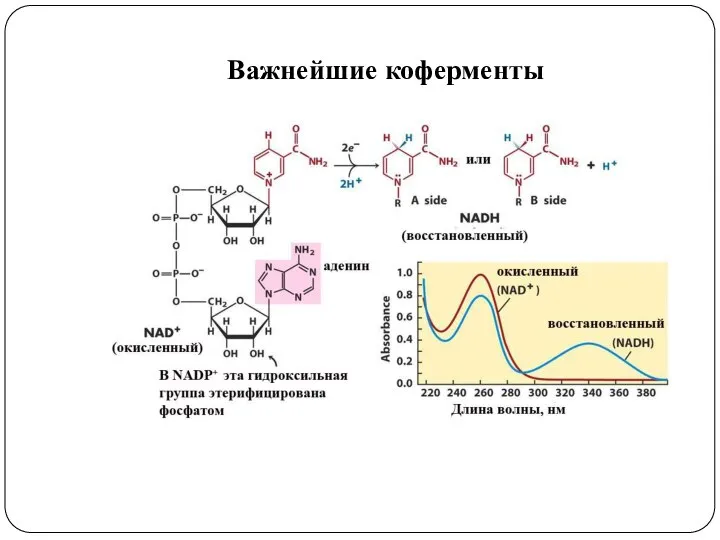
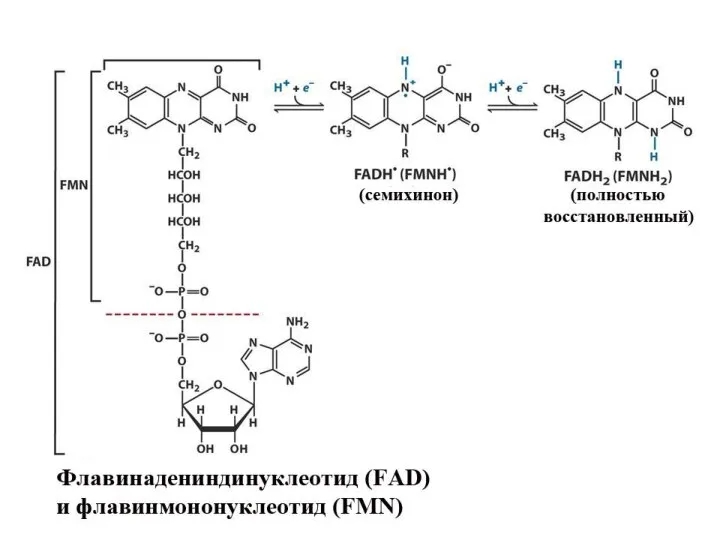
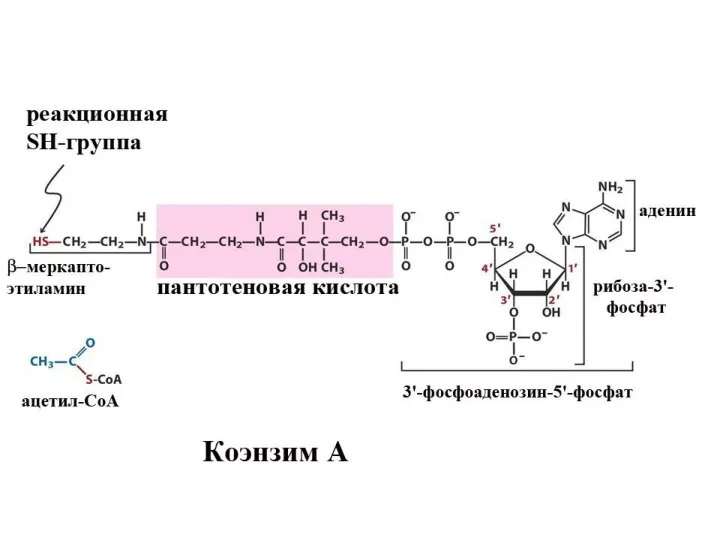
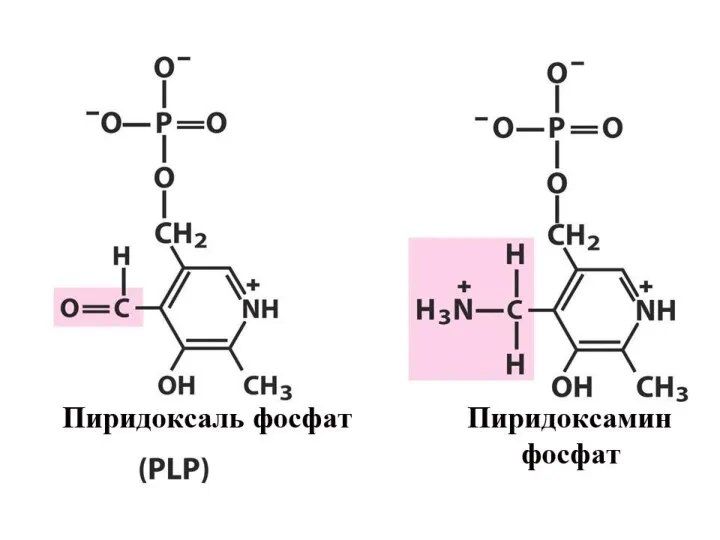
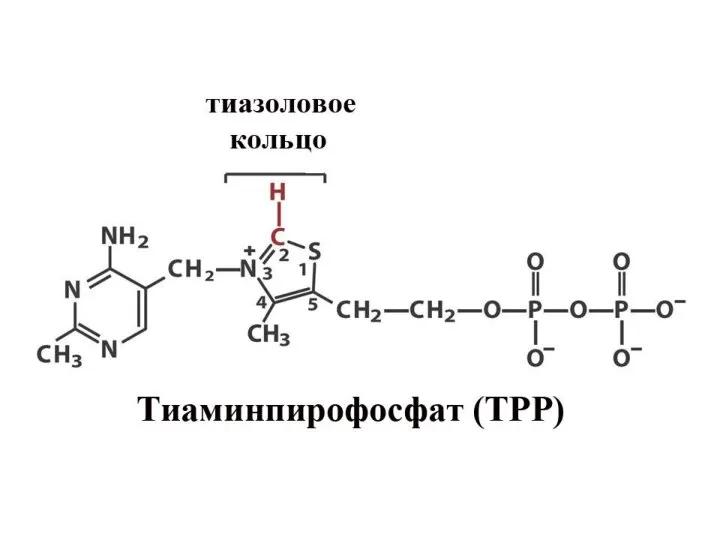
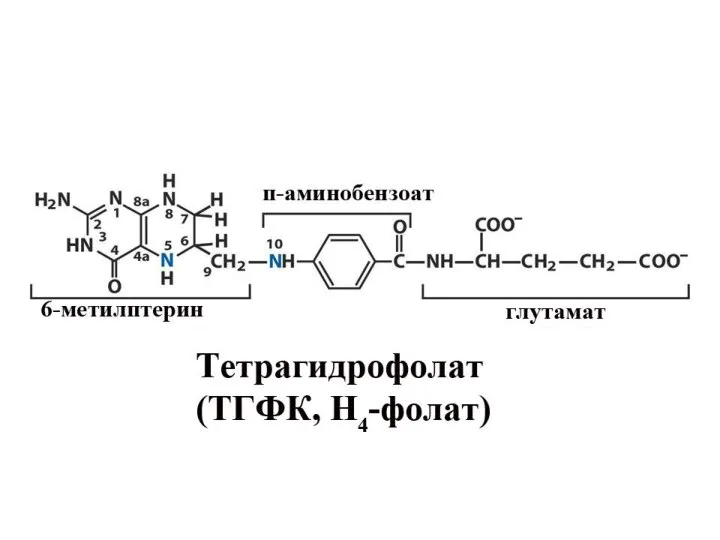
- 14. Важнейшие коферменты
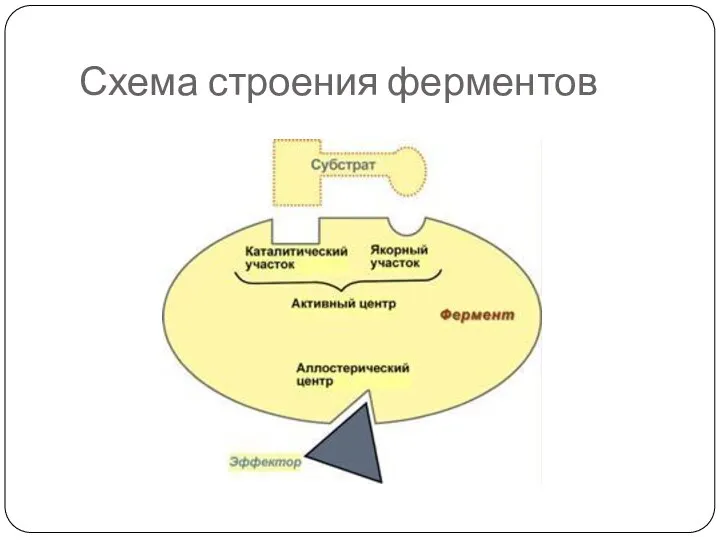
- 23. Структурно-функциональная организация ферментов В составе фермента выделяют области, выполняющие различную функцию: 1. Активный центр – комбинация
- 24. Схема строения ферментов
- 25. 2. Аллостерический центр (allos – чужой) – центр регуляции активности фермента, который пространственно отделен от активного
- 26. Изоферменты Изоферменты – это молекулярные формы одного и того же фермента, возникшие в результате небольших генетических
- 27. ЛДГ Также существует пять изоферментов лактатдегидрогеназы (ЛДГ) – фермента, участвующего в обмене глюкозы. Отличия между ними
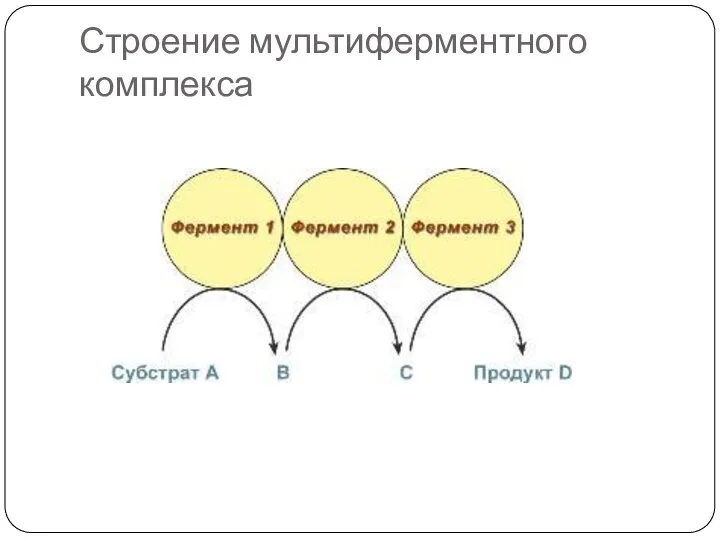
- 28. Мультиферментные комплексы В мультиферментном комплексе несколько ферментов прочно связаны между собой в единый комплекс и осуществляют
- 29. Строение мультиферментного комплекса
- 30. Активность ферментов В повседневной биохимической практике практически не оценивается количество фермента, а только его активность. Активность
- 31. Основы количественного определения активности ферментов Активность фермента выражается в скорости накопления продукта или скорости убыли субстрата
- 32. Единицы активности ферментов В практике обычно используют: единицы количества вещества – моль (и его производные ммоль,
- 33. 2. Создание стандартных условий, чтобы можно было сравнивать результаты, полученные в разных лабораториях – оптимальная рН
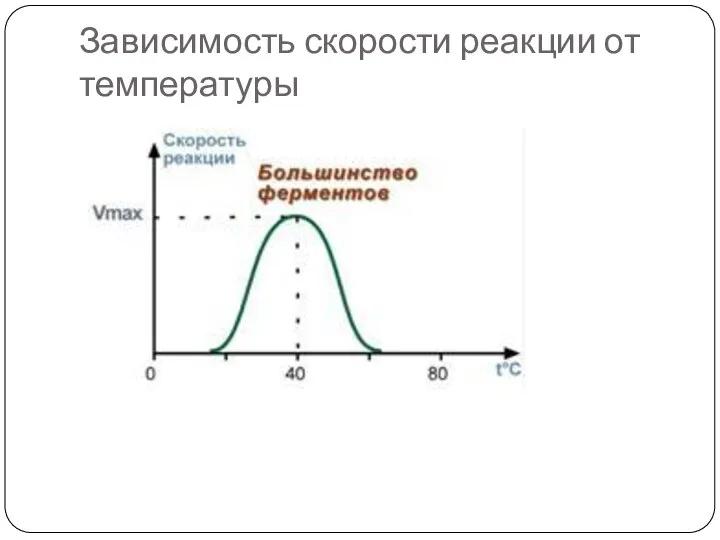
- 34. Свойства ферментов 1. Зависимость скорости реакции от температуры Зависимость активности ферментов (скорости реакции) от температуры описывается
- 35. Зависимость скорости реакции от температуры
- 36. 2. Зависимость скорости реакции от рН Зависимость также описывается колоколообразной кривой с максимумом скорости при оптимальном
- 37. Зависимость скорости реакции от величины pH
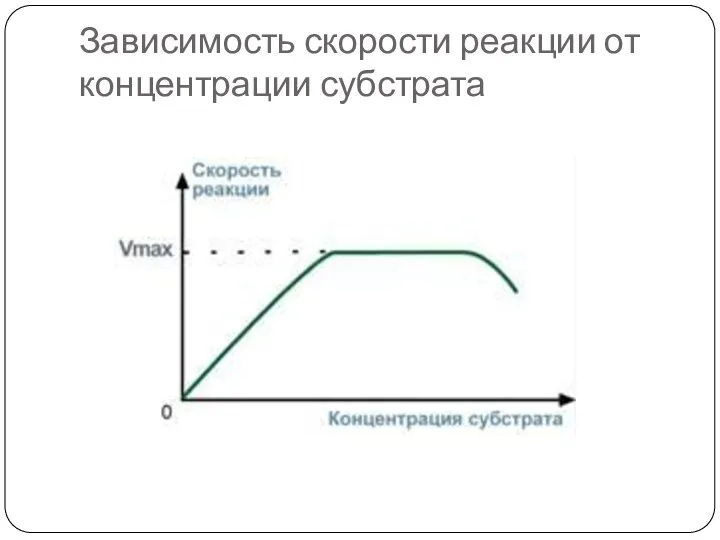
- 38. 3. Зависимость скорости реакции от концентрации субстрата При увеличении концентрации субстрата скорость реакции сначала возрастает соответственно
- 39. Зависимость скорости реакции от концентрации субстрата
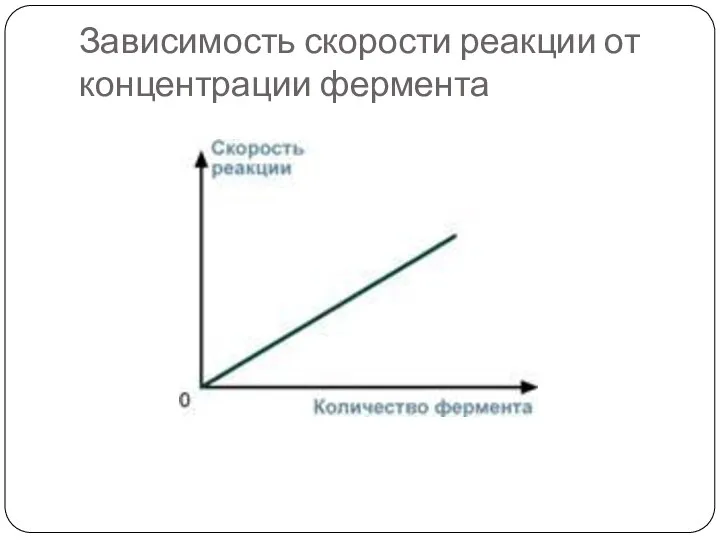
- 40. 4. Зависимость от концентрации фермента При увеличении количества молекул фермента скорость реакции возрастает непрерывно и прямо
- 41. Зависимость скорости реакции от концентрации фермента
- 42. Специфичность ферментов Специфичность, т.е. высокая избирательность действия ферментов, основана на комплементарности структуры субстрата и активного центра
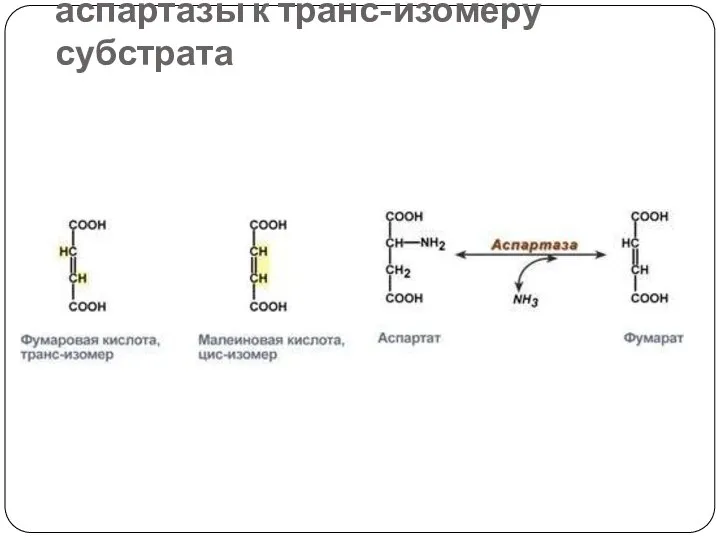
- 43. Стереоспецифичность аспартазы к транс-изомеру субстрата
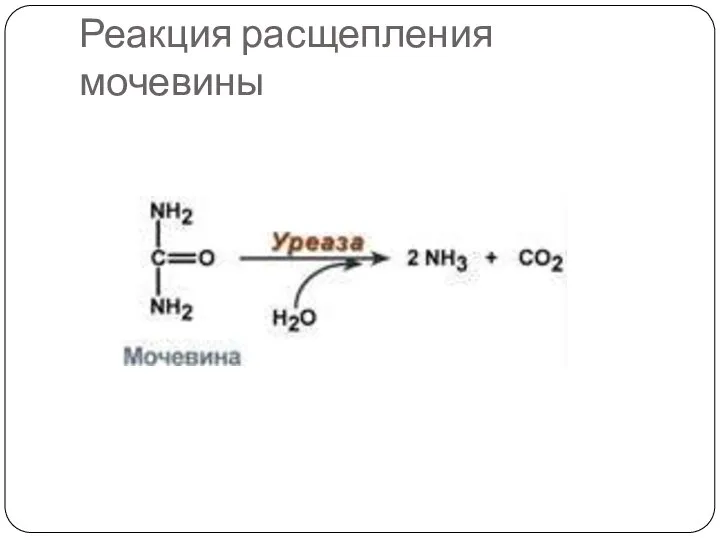
- 44. Реакция расщепления мочевины
- 45. Групповая специфичность 3. Групповая специфичность – катализ субстратов с общими структурными особенностями, т.е. при наличии определенной
- 46. Регуляция активности ферментов Активность ферментов в клетке непостоянна во времени. Ферменты чутко реагируют на ситуацию, в
- 47. 1. Доступность субстрата или кофермента Здесь работает закон действия масс – фундаментальный закон химической кинетики: при
- 48. 2. Компартментализация Компартментализация – это сосредоточение ферментов и их субстратов в одном компартменте (одной органелле) –
- 49. 3. Изменение количества фермента Изменение количества фермента может происходить в результате увеличения или снижения его синтеза.
- 50. 4. Ограниченный (частичный) протеолиз проферментов Ограниченный (частичный) протеолиз проферментов подразумевает, что синтез некоторых ферментов осуществляется в
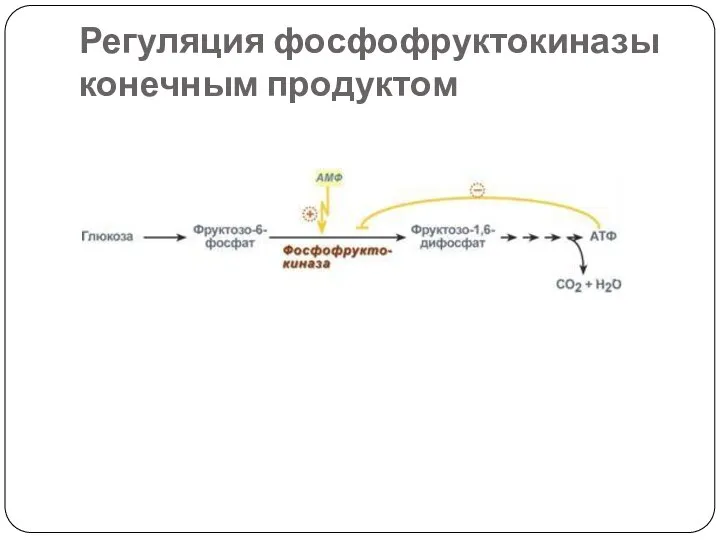
- 51. 5. Аллостерическая регуляция Аллостерические ферменты построены из двух и более субъединиц: одни субъединицы содержат каталитический центр,
- 52. Регуляция фосфофруктокиназы конечным продуктом
- 53. 6. Белок-белковое взаимодействие Термин белок-белковое взаимодействие обозначает ситуацию, когда в качестве регулятора выступают не метаболиты биохимических
- 54. 7. Ковалентная (химическая) модификация Ковалентная модификация заключается в обратимом присоединении или отщеплении определенной группы, благодаря чему
- 55. Ингибирование ферментов В медицине активно разрабатываются и используются соединения, изменяющие активность ферментов с целью регуляции скорости
- 56. Необратимое ингибирование При необратимом ингибировании происходит связывание или разрушение функциональных групп фермента, необходимых для проявления его
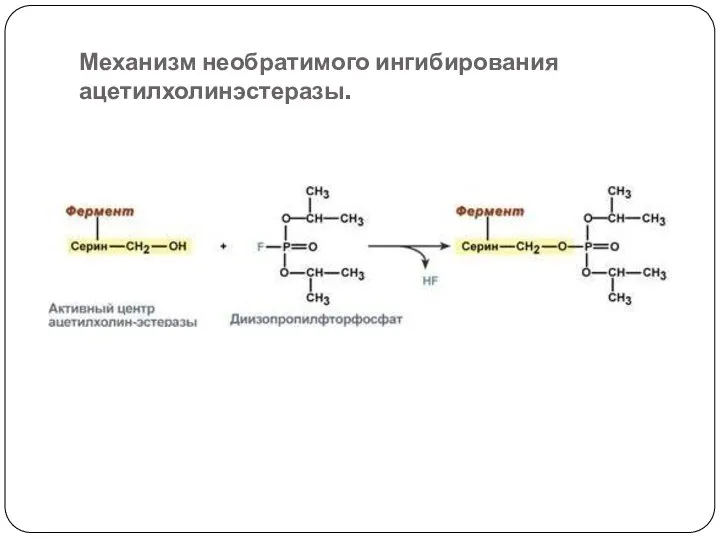
- 57. Механизм необратимого ингибирования ацетилхолинэстеразы.
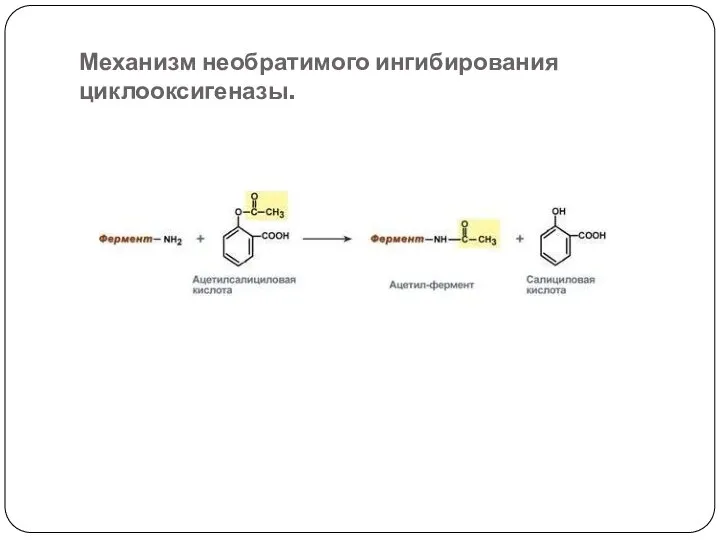
- 58. Механизм необратимого ингибирования циклооксигеназы.
- 59. Обратимое ингибирование При обратимом ингибировании происходит непрочное связывание ингибитора с функциональными группами фермента, вследствие чего активность
- 60. Конкурентное ингибирование При таком виде ингибирования ингибитор по своей структуре похож на субстрат фермента. Поэтому он
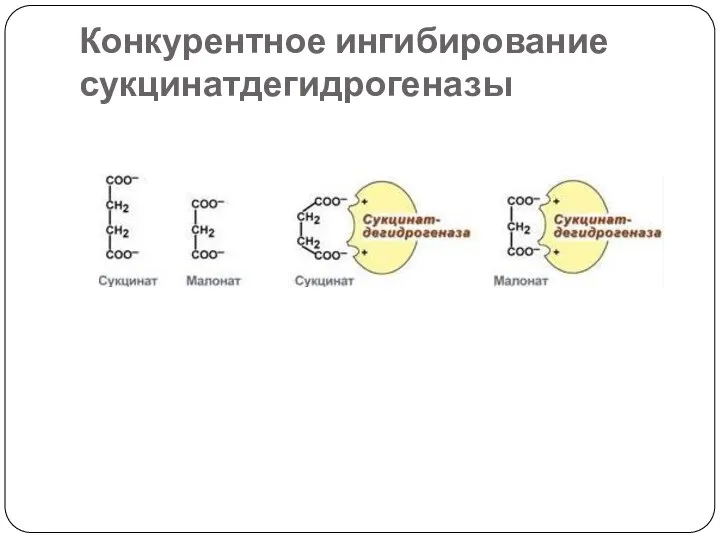
- 61. Конкурентное ингибирование сукцинатдегидрогеназы
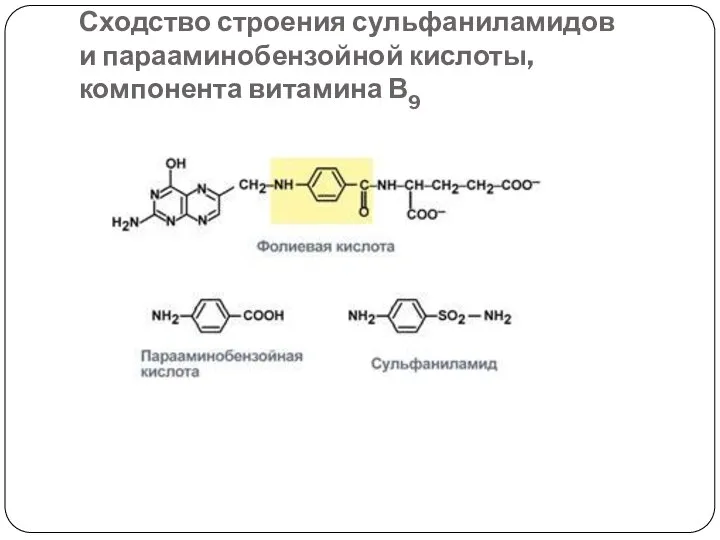
- 62. Сходство строения сульфаниламидов и парааминобензойной кислоты, компонента витамина В9
- 64. Скачать презентацию









































 Химические средства защиты растений
Химические средства защиты растений Каталитический крекинг. Промышленные установки
Каталитический крекинг. Промышленные установки Предельные углеводороды
Предельные углеводороды Алюминий және оның қосылыстары
Алюминий және оның қосылыстары Роль хімії в сучасному житті
Роль хімії в сучасному житті Презентация по Химии "Кислотные дожди"
Презентация по Химии "Кислотные дожди" Простые вещества - металлы
Простые вещества - металлы Минерал чароит. Месторождения
Минерал чароит. Месторождения Валериановая кислота
Валериановая кислота Индикатор pH
Индикатор pH Химические реакции
Химические реакции Физические и химические явления
Физические и химические явления Занимательная химия
Занимательная химия Оксид металлов
Оксид металлов Вазелин и вазелиновое масло
Вазелин и вазелиновое масло Щелочноземельные металлы
Щелочноземельные металлы Презентация Химический состав мороженного
Презентация Химический состав мороженного Спирты, фенолы, простые эфиры
Спирты, фенолы, простые эфиры Электролитическая диссоциация уксусной и муравьиной кислоты
Электролитическая диссоциация уксусной и муравьиной кислоты Методы выделения и очистки продуктов биотехнологических производств
Методы выделения и очистки продуктов биотехнологических производств Интересные факты из жизни Дмитрия Ивановича Менделеева
Интересные факты из жизни Дмитрия Ивановича Менделеева  Personal сare. Akypo Foam Rl 40
Personal сare. Akypo Foam Rl 40 Азотная кислота и нитраты
Азотная кислота и нитраты ,1
,1 Катионы І - ІІІ аналитических групп
Катионы І - ІІІ аналитических групп Щавелевая кислота
Щавелевая кислота Установка кристаллов
Установка кристаллов Тугоплавкие металлы и их сплавы
Тугоплавкие металлы и их сплавы