Содержание
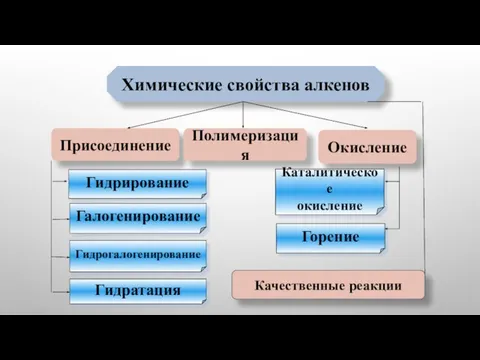
- 2. Химические свойства алкенов Присоединение Окисление Полимеризация Гидрирование Галогенирование Гидрогалогенирование Гидратация Горение Каталитическое окисление Качественные реакции
- 3. ГИДРИРОВАНИЕ T, NI СН2=СН2 + Н2 → СН2 – СН2 L L Н Н
- 4. ГАЛОГЕНИРОВАНИЕ СН2=СН2 + CI2 (ВОДНЫЙ РАСТВОР) → СН2 – СН2 L L CI CI ДИХЛОРЭТАН
- 5. ГИДРОГАЛОГЕНИРОВАНИЕ СН3–СН=СН2 + Н:CI→ СН3–СН–СН2 L L Н CI 1-ХЛОРПРОПАН ПРАВИЛО МАРКОВНИКОВА ПРИСОЕДИНЕНИЕ ВОДОРОДА ПРОИСХОДИТ К
- 6. ГИДРАТАЦИЯ T, H3PO4 СН2=СН2 + НОН → СН2 – СН2 L L Н ОН ПРАВИЛО МАРКОВНИКОВА
- 7. РЕАКЦИЯ ПОЛИМЕРИЗАЦИИ n(СН2 = СН2) → (- СН2 – СН2 -)n кat,t,p этилен полиэтилен мономер структурное
- 8. КАТАЛИТИЧЕСКОЕ ОКИСЛЕНИЕ 1. В ПРИСУТСТВИИ ХЛОРИДОВ МЕДИ И ПАЛЛАДИЯ: КАТ. 2 СН2=СН2 + О2 → 2
- 9. РЕАКЦИЯ ВАГНЕРА 3СН2=СН2 + 4Н2О + 2KMNO4 3СН2OH-СН2OH +2MNO2 + 2KOH ЭТИЛЕНГЛИКОЛЬ КАЧЕСТВЕННАЯ РЕАКЦИЯ НА КРАТНУЮ
- 10. СН2=СН2 + BR2 → СН2–СН2 L L BR BR ДИБРОМЭТАН БРОМНАЯ ВОДА, ИМЕЮЩАЯ ЖЕЛТУЮ ОКРАСКУ ОБЕСЦВЕЧИВАЕТСЯ
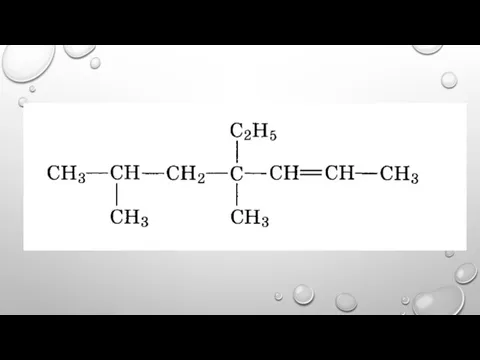
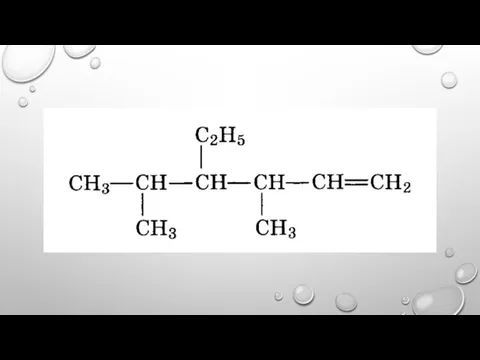
- 12. 3,3- ДИМЕТИЛПЕНТЕН-1 2,4-ДИМЕТИЛГЕКСЕН-2 2,4,4-ТРИМЕТИЛПЕНТЕН-2
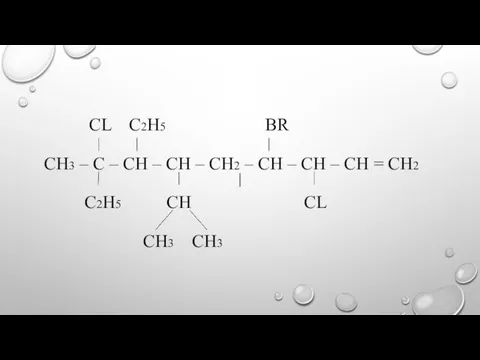
- 15. 2,3,4,6-ТЕТРАМЕТИЛ-2,7-ДИХЛОР-5,6-ДИЭТИЛОКТЕН-4 2,8,8-ТРИБРОМ-3,9,9-ТРИМЕТИЛ-5-ИЗОПРОПИЛ-6-ХЛОРДЕЦЕН-1
- 16. CL C2H5 BR СH3 – С – СH – СH – СH2 – СH – СH
- 18. Скачать презентацию











 Валентность
Валентность Тепловой эффект химических реакций 8 класс
Тепловой эффект химических реакций 8 класс Методы снижения уровня учебного стресса у обучающихся 9-х классов на уроках химии
Методы снижения уровня учебного стресса у обучающихся 9-х классов на уроках химии Органикалық қосылыстардың жіктелуі
Органикалық қосылыстардың жіктелуі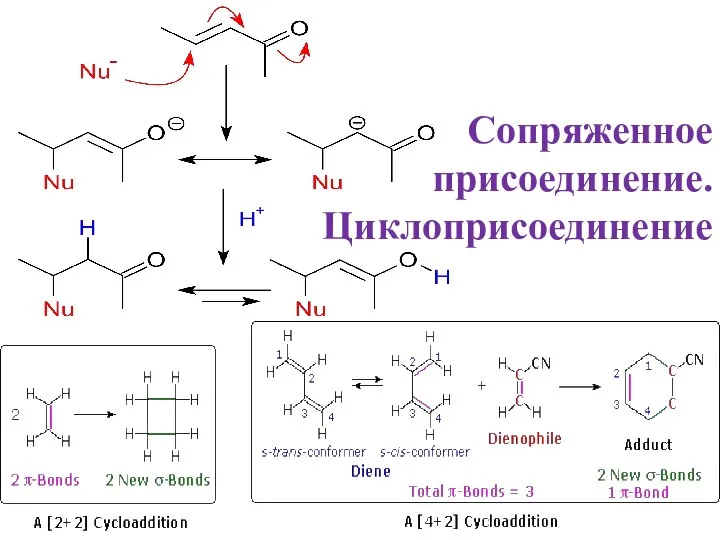 Сопряженное присоединение. Циклоприсоединениеie
Сопряженное присоединение. Циклоприсоединениеie Номенклатура органических соединений
Номенклатура органических соединений Конструкционные функциональные волокнистые композиты
Конструкционные функциональные волокнистые композиты Применение солей
Применение солей  Классы неорганических соединений. Индивидуальные задания
Классы неорганических соединений. Индивидуальные задания Углеводороды. Свойства алканов
Углеводороды. Свойства алканов Ртуть. Нахождение в природе. Применение
Ртуть. Нахождение в природе. Применение Химические компоненты клетки. Неорганические компоненты
Химические компоненты клетки. Неорганические компоненты Презентация по Химии "Синтетические материалы" - скачать смотреть
Презентация по Химии "Синтетические материалы" - скачать смотреть  Мило. Мийні засоби
Мило. Мийні засоби  Презентация по Химии "Группа веществ, изолируемых из биологического материала дистилляцией («Летучие яды»)" - скачать смотрет
Презентация по Химии "Группа веществ, изолируемых из биологического материала дистилляцией («Летучие яды»)" - скачать смотрет Горные породы: гранит, базальт
Горные породы: гранит, базальт Хочу хорошо сдать ЕГЭ
Хочу хорошо сдать ЕГЭ Презентация по Химии "Особенности строения атома карбона в основном и возбужденном состояниях. Образование ковалентных связей
Презентация по Химии "Особенности строения атома карбона в основном и возбужденном состояниях. Образование ковалентных связей  Подготовка к лабораторной работе
Подготовка к лабораторной работе Фосфор, фосфор оксидтері
Фосфор, фосфор оксидтері Биохимия печени
Биохимия печени Презентація на тему : Застосування Сполук Алюмінію Підготував : Учень 10 класу Кійко Едуард
Презентація на тему : Застосування Сполук Алюмінію Підготував : Учень 10 класу Кійко Едуард  Классификация минералов
Классификация минералов Конкурс проектных работ "Химия наука о чудесах!" Выполнила: ученица 8 класса МОУ гимназии № 91 имени М.В.Ломоносова Пожид
Конкурс проектных работ "Химия наука о чудесах!" Выполнила: ученица 8 класса МОУ гимназии № 91 имени М.В.Ломоносова Пожид Силикатная промышленность Подготовила ученица 9 А класса Семёнова Екатерина
Силикатная промышленность Подготовила ученица 9 А класса Семёнова Екатерина Сульфиды и им подобные соединения
Сульфиды и им подобные соединения Текстуры метаморфических пород
Текстуры метаморфических пород Превращения в нашей жизни: физические и химические
Превращения в нашей жизни: физические и химические