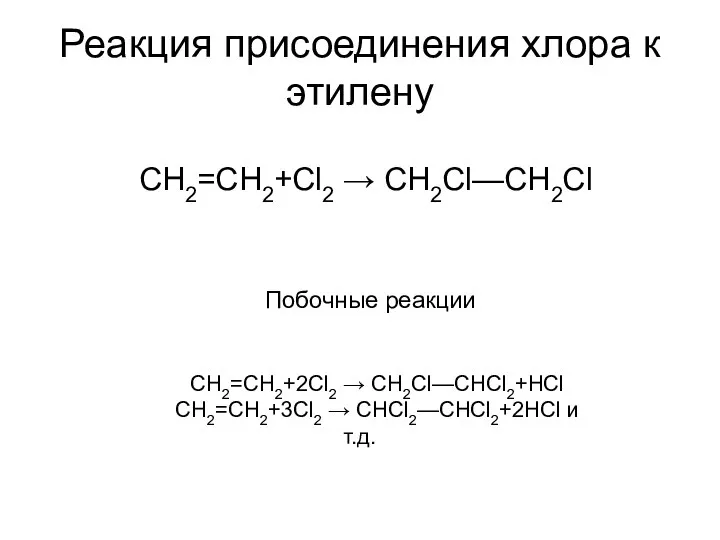
Основные свойства
Этилен СН2 = СН2.
– молекулярная масса – 28
– плотность –
1,261 кг/м3
– растворимость в воде при н. у. – 0,281г/дм3
– температура кипения – минус 103,710 С
– температура плавления – минус 169,50 С
Хлор СL2
– молекулярная масса – 35
– плотность – 3,214 кг/м3
– растворимость в воде при н. у. – 7,4г/дм3
– температура кипения – минус 34,050 С
– температура плавления – минус 101,60 С
1,2-Дихлорэтан СН2Сl – CН2Cl.
– молекулярная масса – 98
– плотность – 1282 кг/м3
– температура кипения – 83,47 0С
– температура плавления – минус 35,36 0С

![Выход продуктов реакции Условия процесса:[6] Температура – 265 0С; Давление –](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1394783/slide-2.jpg)



 Неорганические вещества
Неорганические вещества Аттестационная работа. Программа элективного курса химия и военное дело. (8-9 класс)
Аттестационная работа. Программа элективного курса химия и военное дело. (8-9 класс) ПРОЕКТ по химии «Значение химии в жизни человека» Выполнила ученица 8 А класса МОУ «Ленинская СОШ №3» Кальнова Дарья
ПРОЕКТ по химии «Значение химии в жизни человека» Выполнила ученица 8 А класса МОУ «Ленинская СОШ №3» Кальнова Дарья Краткая история химии
Краткая история химии Процессы комплексообразования
Процессы комплексообразования Воздух, которым мы дышим
Воздух, которым мы дышим Хлороводород. Соляная кислота.
Хлороводород. Соляная кислота.  Химический элемент - бром
Химический элемент - бром Шампунь для волосся
Шампунь для волосся  Химия элементов VIIA-группы
Химия элементов VIIA-группы Конструкционные функциональные волокнистые композиты. Полимерные матричные материалы
Конструкционные функциональные волокнистые композиты. Полимерные матричные материалы Мило та його склад
Мило та його склад  Фiзико-хімічні основи розвитку пожеж. Тепломасообмін, температурний режим пожежі в огородженні. (Розділ 4.13.5)
Фiзико-хімічні основи розвитку пожеж. Тепломасообмін, температурний режим пожежі в огородженні. (Розділ 4.13.5) Характеристика и технология производства основных катализаторов нефтепереработки
Характеристика и технология производства основных катализаторов нефтепереработки Геохимия магматического процесса
Геохимия магматического процесса Химия в сельском хозяйстве
Химия в сельском хозяйстве Поверхностные и массовые силы. Вывод уравнения неразрывности сплошной однокомпонентной среды
Поверхностные и массовые силы. Вывод уравнения неразрывности сплошной однокомпонентной среды Бензол қатарындағы гетерофункционалды туындылары дәрі-дәрмек ретінде
Бензол қатарындағы гетерофункционалды туындылары дәрі-дәрмек ретінде Основы химической термодинамики и кинетики химических реакций
Основы химической термодинамики и кинетики химических реакций Бораттарды алу
Бораттарды алу Глюкоза. Будова глюкози та її властивості
Глюкоза. Будова глюкози та її властивості Автор: Васильева Е.Д. Учитель физики МОУ гимназия г.Советский
Автор: Васильева Е.Д. Учитель физики МОУ гимназия г.Советский Глобальні екологічні проблеми повязані з добуванням та переробкою вуглеводної сировини Підготувала учениця 11-А класу Гребі
Глобальні екологічні проблеми повязані з добуванням та переробкою вуглеводної сировини Підготувала учениця 11-А класу Гребі Основные понятия химической термодинамики. Первый закон термодинамики Физическая и коллоидная химия и ее значение для фармации
Основные понятия химической термодинамики. Первый закон термодинамики Физическая и коллоидная химия и ее значение для фармации Каталитические превращения углеводородов и других компонентов нефти
Каталитические превращения углеводородов и других компонентов нефти Синтез метилового эфира цинкофорина
Синтез метилового эфира цинкофорина Количество вещества. Моль. Молярная масса
Количество вещества. Моль. Молярная масса Крахмал. Строение вещества
Крахмал. Строение вещества