Основные понятия химической термодинамики. Первый закон термодинамики Физическая и коллоидная химия и ее значение для фармации
Содержание
- 2. 1. Физколлоидная химия и ее значение для фармации Физическая химия - одна из пограничных наук, изучающая
- 3. 1.Физколлоидная химия и ее значение для фармации Основные разделы физколлоидной химии и их значение для фармации:
- 4. 1. Физколлоидная химия и ее значение для фармации 2. Учение о фазовых равновесиях позволяет осознанно выбирать
- 5. 1. Физколлоидная химия и ее значение для фармации 4. Химическая кинетика изучает скорости химических реакций и
- 6. 1. Физколлоидная химия и ее значение для фармации 5. Электрохимия, изучает взаимосвязь химических и физических процессов
- 7. 1. Физколлоидная химия и ее значение для фармации 6. Коллоидная химия занимается изучением коллоидных систем, может
- 8. 1. Физколлоидная химия и ее значение для фармации На основе сведений о молекулярно-кинетических, реологических и оптических
- 9. 1. Физколлоидная химия и ее значение для фармации Физическая химия составляет теоретическую основу различных наук фармации:
- 10. 1. Физколлоидная химия и ее значение для фармации Основные методы физической химии: Термодинамический метод - метод,
- 11. 1. Физколлоидная химия и ее значение для фармации В истории физической химии выделяют три основных периода:
- 12. 1. Физколлоидная химия и ее значение для фармации Второй период — оформление физической химии в самостоятельную
- 13. 1. Физколлоидная химия и ее значение для фармации В этот период были сформированы новые разделы физической
- 14. 1. Физколлоидная химия и ее значение для фармации Началом третьего современного периода развития физической химии принято
- 15. 1. Физколлоидная химия и ее значение для фармации Широко применяются экспериментальные методы современной физики - ультрафиолетовая
- 16. 1. Физколлоидная химия и ее значение для фармации В настоящее время физическая химия приобретает все большее
- 17. 2. Основные понятия химической термодинамики Химическая термодинамика изучает закономерности превращения энергии в химических реакциях и при
- 18. 2. Основные понятия химической термодинамики Для удобства иллюстрации закономерностей термодинамики в качестве простейшей термодинамической системы будем
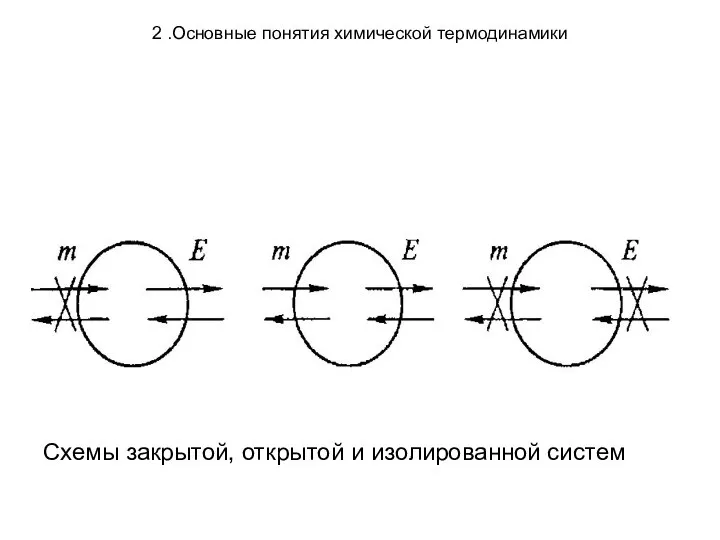
- 19. 2. Основные понятия химической термодинамики По характеру обмена энергией и веществом с внешней средой системы разделяют
- 20. 2 .Основные понятия химической термодинамики Схемы закрытой, открытой и изолированной систем
- 21. 2. Основные понятия химической термодинамики Термодинамическое состояние системы - совокупность всех физических и химических свойств системы.
- 22. 2.Основные понятия химической термодинамики Термодинамические параметры - это совокупность физических величин, определяющих состояние системы. Если их
- 23. 2. Основные понятия химической термодинамики Термодинамический процесс - переход системы из одного равновесного состояния в другое,
- 24. 2. Основные понятия химической термодинамики Термодинамические параметры, которые не зависят от пути перехода называются функциями состояния
- 25. 2. Основные понятия химической термодинамики В зависимости от того, какой из параметров состояния при протекании термодинамического
- 26. 2. Основные понятия химической термодинамики На практике часто протекают процессы, когда и р = const, и
- 27. 3. 1 з-н термодинамики. Внутр. энергия. Теплота. Работа. Первый закон термодинамики является постулатом: он не может
- 28. 3. 1 з-н термодинамики. Внутр. энергия. Теплота. Работа. Формулировки первого закона термодинамики вечный двигатель первого рода
- 29. 3. 1 з-н термодинамики. Внутр. энергия. Теплота. Работа. Внутренняя энергия (U) - термодинамическая функция состояния системы,
- 30. 3. 1 з-н термодинамики. Внутр. энергия. Теплота. Работа. Теплота (Q) - форма передачи энергии, посредством хаотического
- 31. 3. 1 з-н термодинамики. Внутр. энергия. Теплота. Работа. Работа (А) - форма передачи энергии от системы
- 32. 3. 1 з-н термодинамики. Внутр. энергия. Теплота. Работа. В зависимости от условий проведения процесса работа может
- 33. 3. 1 з-н термодинамики. Внутр. энергия. Теплота. Работа. Все разновидности работы кроме работы расширения-сжатия, называют полезными
- 34. 4. Модификация 1 з-на терм-ки для разл. процессов. Энтальпия. 1. Изохорный процесс (V = const) проводят
- 35. 4. Модификация 1 з-на терм-ки для разл. процессов. Энтальпия. Тогда уравнение первого закона термодинамики принимает следующий
- 36. 4. Модификация 1 з-на терм-ки для разл. процессов. Энтальпия. 2. Изобарный процесс (р = const). Если
- 37. 4. Модификация 1 з-на терм-ки для разл. процессов. Энтальпия. Согласно первому закону термодинамики теплота, направленная в
- 38. 4. Модификация 1 з-на терм-ки для разл. процессов. Энтальпия. Из уравнений следует, что теплота изобарного процесса
- 39. 4. Модификация 1 з-на терм-ки для разл. процессов. Энтальпия. В настоящее время нет возможности определить абсолютную
- 41. Скачать презентацию





































 Микроколичественное определение 2,3-бутандиола для анализа антирадикальной активности фенольных соединений
Микроколичественное определение 2,3-бутандиола для анализа антирадикальной активности фенольных соединений Пятичленные гетероциклы с двумя гетероатомами - азолы
Пятичленные гетероциклы с двумя гетероатомами - азолы Общая характеристика углерода
Общая характеристика углерода Химический элемент фосфор. Фосфор в составе ДНК и РНК
Химический элемент фосфор. Фосфор в составе ДНК и РНК Акварельные краски. Их состав и изготовление
Акварельные краски. Их состав и изготовление Начальные стадии растворения смектита при кислотной обработке
Начальные стадии растворения смектита при кислотной обработке Фосфор. Функции фосфора в организме
Фосфор. Функции фосфора в организме Загальні способи добування основ і солей
Загальні способи добування основ і солей Неорганическая химия Сероводород
Неорганическая химия Сероводород  Введение в химию. Теоретические основы химии
Введение в химию. Теоретические основы химии Пленки нитрида галлия
Пленки нитрида галлия Соли. Названия и классификация солей
Соли. Названия и классификация солей Енергетичний стан поверхні. Сорбційні явища. Мезопористі матеріали
Енергетичний стан поверхні. Сорбційні явища. Мезопористі матеріали Геохимия редкоземельных элементов
Геохимия редкоземельных элементов Алкены. Строение. Изомерия. Химические свойства. Получение. Учитель химии ГОУ СОШ №277 Кировского района г. Санкт-Петербурга Елен
Алкены. Строение. Изомерия. Химические свойства. Получение. Учитель химии ГОУ СОШ №277 Кировского района г. Санкт-Петербурга Елен Научные принципы химического производства. Производство аммиака
Научные принципы химического производства. Производство аммиака Фотолабораторный процесс. Основные этапы фото обработки. Рентгеновского изображения
Фотолабораторный процесс. Основные этапы фото обработки. Рентгеновского изображения Решение задач на нахождение молекулярной формулы органических веществ
Решение задач на нахождение молекулярной формулы органических веществ Презентация по Химии "Производство аммиака цианамидным методом" - скачать смотреть
Презентация по Химии "Производство аммиака цианамидным методом" - скачать смотреть  Металдар мен бейметалдардың табиғатта таралуы. ҚР-дағы кен орындары
Металдар мен бейметалдардың табиғатта таралуы. ҚР-дағы кен орындары Өндірістік улар
Өндірістік улар Неметаллы 9 класс
Неметаллы 9 класс Кристаллические решетки
Кристаллические решетки Хиральные производные тиомочевины и скуарамидов в асимметрическом катализе
Хиральные производные тиомочевины и скуарамидов в асимметрическом катализе Ерітінділер түрлері. Идеал ертітінділер және реал ерітінділер. Ерітіндінің пайыздық концентрациясына eсептер
Ерітінділер түрлері. Идеал ертітінділер және реал ерітінділер. Ерітіндінің пайыздық концентрациясына eсептер Твердое тело и его характеристики. Закон Гука. Плавление и кристаллизация. Лекция №26
Твердое тело и его характеристики. Закон Гука. Плавление и кристаллизация. Лекция №26 Gas hydrates
Gas hydrates Химический элемент V группы: сурьма
Химический элемент V группы: сурьма