Содержание
- 2. А Л Ь Д Е Г И Д Ы - органические вещества, молекулы которых содержат карбонильную
- 3. Классификация. 1. По характеру углеводородного радикала: предельные, непредельные, ароматические. 2. По числу альдегидных групп: моно-, диальдегиды
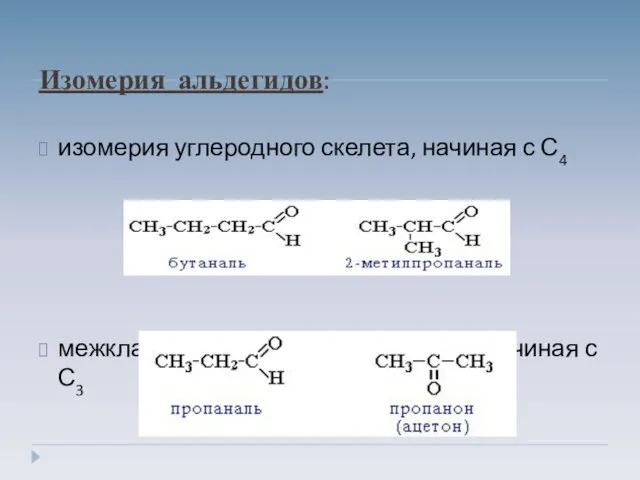
- 4. Изомерия альдегидов: изомерия углеродного скелета, начиная с С4 межклассовая изомерия с кетонами, начиная с С3
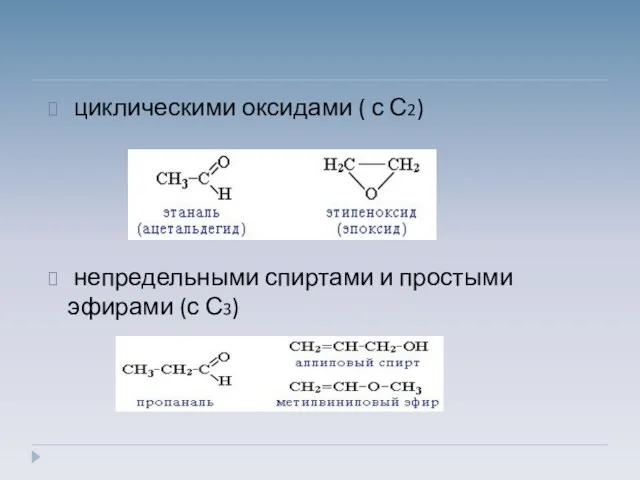
- 5. циклическими оксидами ( с С2) непредельными спиртами и простыми эфирами (с С3)
- 6. Физические свойства. Метаналь (формальдегид) – газ, альдегиды С2-C5 – жидкости, высшие – твердые вещества. Низшие гомологи
- 7. Физически свойства некоторых альдегидов. Формальдегид – газ, с резким запахом, раздражает слизистые ткани и оказывает действие
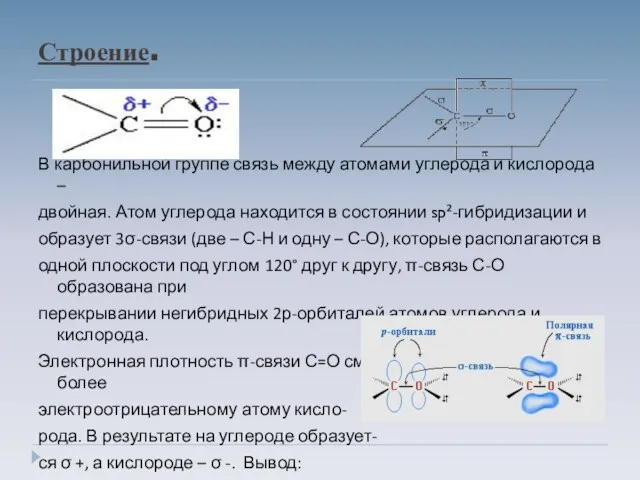
- 8. Строение. В карбонильной группе связь между атомами углерода и кислорода – двойная. Атом углерода находится в
- 9. Химические свойства. Наличие альдегидной группы в молекуле определяет характерные свойства альдегидов. Реакции присоединения. Гидрирование – реакции
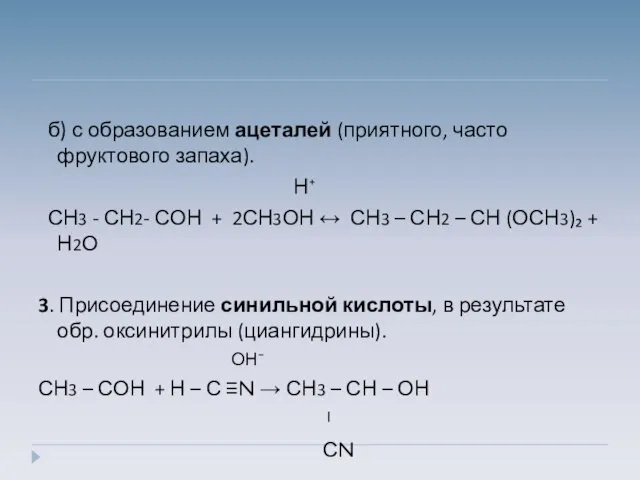
- 10. б) с образованием ацеталей (приятного, часто фруктового запаха). Н⁺ СН3 - СН2- СОН + 2СН3ОН ↔
- 11. 4. Присоединение гидросульфита натрия (это качественная реакция на карбонильную группу), в результате образ. гидросульфит натрия. СН3
- 12. Химические свойства II. Реакции полимеризации: а) линейная n СН2 = О → [ - СН2 –
- 13. Химические свойства III. Реакции окисления: 1. аммиачным раствором оксида серебра (реакция «серебряного зеркала»). Это качественная реакция
- 14. 2. гидроксидом меди (II), в результате обр. осадок кирпично-красного цвета (качественная реакция). t° СН3 – СОН
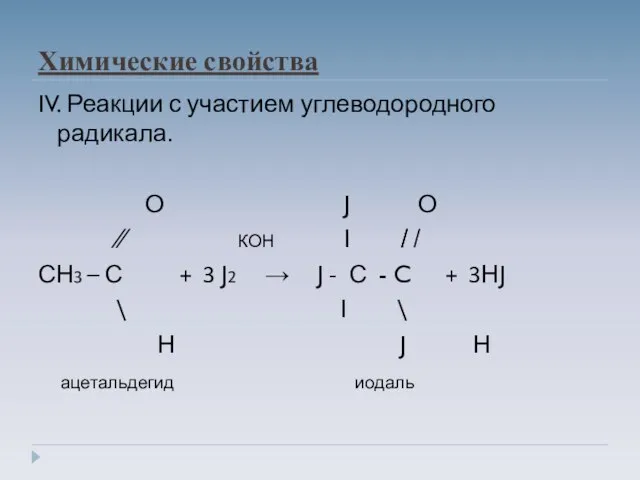
- 15. Химические свойства IV. Реакции с участием углеводородного радикала. О J О ∕∕ КОН Ι ̸̸ ̸
- 16. Химические свойства. V. Реакции с магнийорганическими соединениями. О ОМgBr первичный ΙΙ Ι Н2О спирт С +
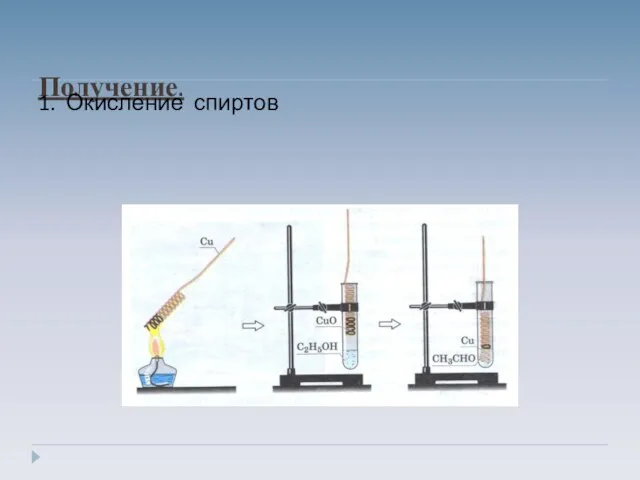
- 17. Получение. 1. Окисление спиртов
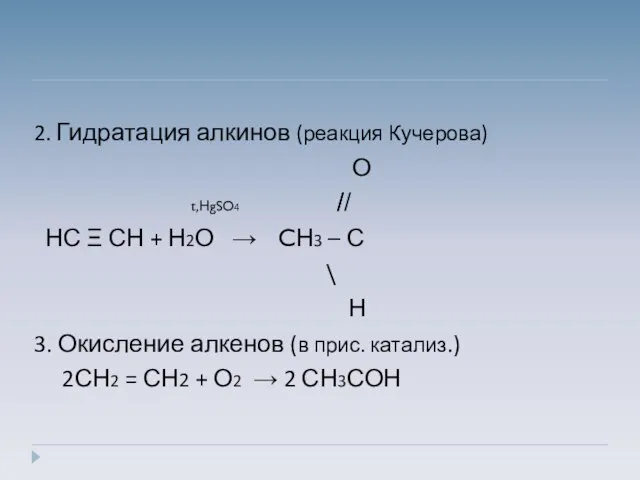
- 18. 2. Гидратация алкинов (реакция Кучерова) О t,НgSO4 ̸̸̸ ̸ НС Ξ СН + Н2О → CН3
- 20. Скачать презентацию










 Скорость химической реакции
Скорость химической реакции Урок-сказка Приключение серной кислоты
Урок-сказка Приключение серной кислоты Презентация по Химии "Детонаційна стійкість бензину" - скачать смотреть бесплатно
Презентация по Химии "Детонаційна стійкість бензину" - скачать смотреть бесплатно Железо и его соединения
Железо и его соединения Металлы
Металлы Неорганические вещества. Оксиды, кислоты, соли, основания
Неорганические вещества. Оксиды, кислоты, соли, основания Функциональные производные с простой связью C-“Э". Галогенпроизводные. (Лекция 5)
Функциональные производные с простой связью C-“Э". Галогенпроизводные. (Лекция 5) Окислительно–восстановительные реакции (ОВР)
Окислительно–восстановительные реакции (ОВР) Аминокислоты. Белки
Аминокислоты. Белки Polivinilpirrolidon-limon turşusunun Na duzu-su ikifazalı sisteminin fizikikimyəvi xassələri
Polivinilpirrolidon-limon turşusunun Na duzu-su ikifazalı sisteminin fizikikimyəvi xassələri Подготовка к ЕГЭ: КИСЛОРОДСОДЕРЖАЩИЕ. УГЛЕВОДЫ. Муниципальное бюджетное общеобразовательное учреждение «Средняя общеобразоват
Подготовка к ЕГЭ: КИСЛОРОДСОДЕРЖАЩИЕ. УГЛЕВОДЫ. Муниципальное бюджетное общеобразовательное учреждение «Средняя общеобразоват Шлиховые минералы
Шлиховые минералы Предмет органической химии. Особенности органических веществ
Предмет органической химии. Особенности органических веществ Презентация по Химии "Классификация реакций в неорганической химии." - скачать смотреть бесплатно_
Презентация по Химии "Классификация реакций в неорганической химии." - скачать смотреть бесплатно_ Аттестационная работа. Программа внеурочной деятельности по химии “Занимательная химия”. (8 класс)
Аттестационная работа. Программа внеурочной деятельности по химии “Занимательная химия”. (8 класс) Кольорові метали
Кольорові метали  Пути обмена глюкозо-6 фосфата в тканях. Анаэробное расщепление глюкозы. Спиртовое брожение. Метаболизм этанола. (Тема 2)
Пути обмена глюкозо-6 фосфата в тканях. Анаэробное расщепление глюкозы. Спиртовое брожение. Метаболизм этанола. (Тема 2) Основания. Гидроксид лития
Основания. Гидроксид лития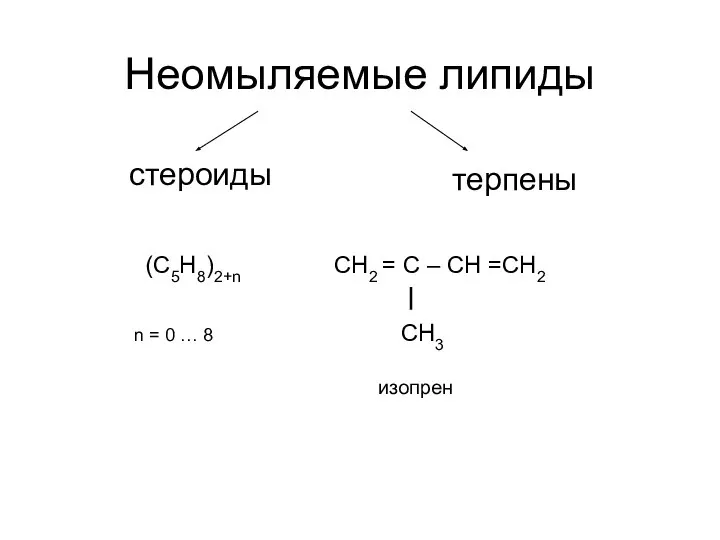 Неомыляемые липиды. Стероиды
Неомыляемые липиды. Стероиды Одержання нанопорошків з гідроксидів
Одержання нанопорошків з гідроксидів Решение задач на Углеводороды
Решение задач на Углеводороды План выполнения домашней работы по теме «Алкадиены»
План выполнения домашней работы по теме «Алкадиены» Олигонуклеотидный синтез
Олигонуклеотидный синтез Фосфор и его соединения
Фосфор и его соединения Этанол (этиловый спирт)
Этанол (этиловый спирт) Цеоліти як адсорбенти та основа сучасних каталізаторів. Структура, здатність до модифікування
Цеоліти як адсорбенти та основа сучасних каталізаторів. Структура, здатність до модифікування Кремнийорганические модификаторы
Кремнийорганические модификаторы Colloid chemistry
Colloid chemistry