Содержание
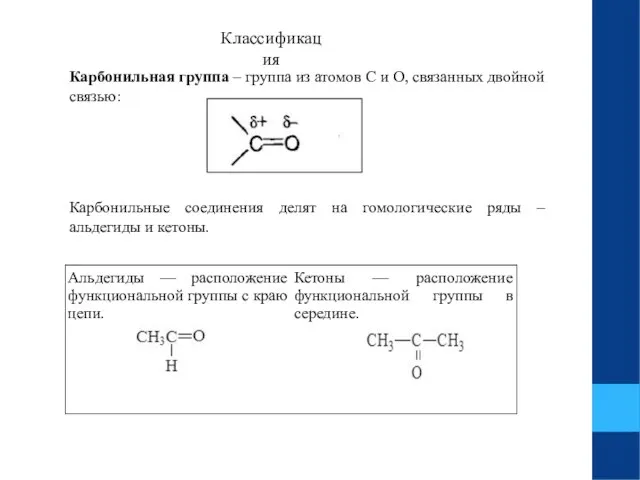
- 2. Карбонильная группа – группа из атомов С и О, связанных двойной связью: Карбонильные соединения делят на
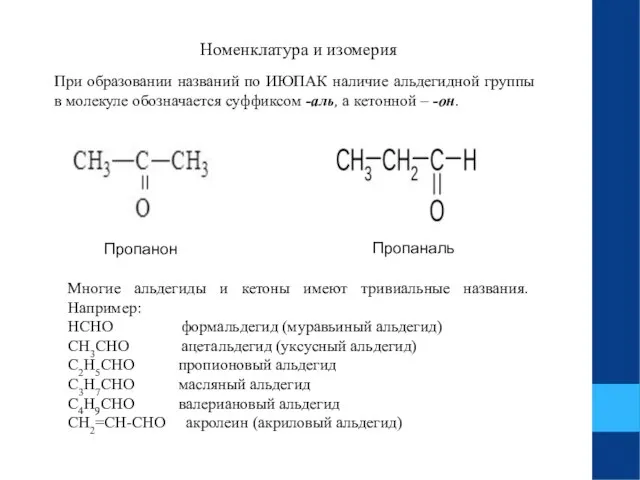
- 3. Номенклатура и изомерия При образовании названий по ИЮПАК наличие альдегидной группы в молекуле обозначается суффиксом -аль,
- 4. Изомерия альдегидов и кетонов 1. Изомерия углеродного скелета, у кетонов начиная с c C5, у альдегидов
- 5. 2. Изомерия положения карбонильной группы (c C5):
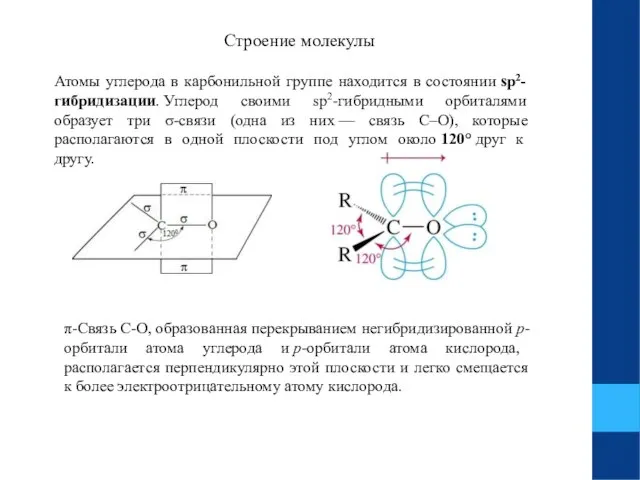
- 6. Строение молекулы Атомы углерода в карбонильной группе находится в состоянии sp2-гибридизации. Углерод своими sp2-гибридными орбиталями образует
- 7. Связь С=О сильно поляризована. Электроны кратной связи С=О, особенно более подвижные π-электроны, смещены к более электроотрицательному
- 8. Физические свойства соединений Нет водородных связей. Температура плавления и кипения немного ниже, чем у спиртов. Хорошо
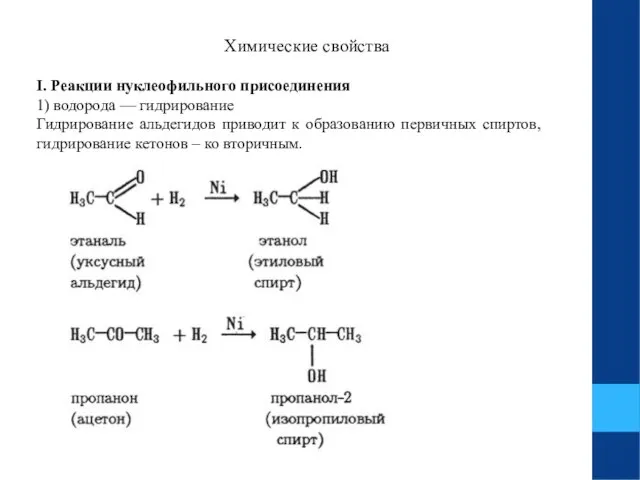
- 9. Химические свойства I. Реакции нуклеофильного присоединения 1) водорода — гидрирование Гидрирование альдегидов приводит к образованию первичных
- 10. 2) Воды Формальдегид Хлоральгидрат — бесцветные кристаллы, хорошо растворимые в воде, ацетоне, этаноле и диэтиловом эфире,
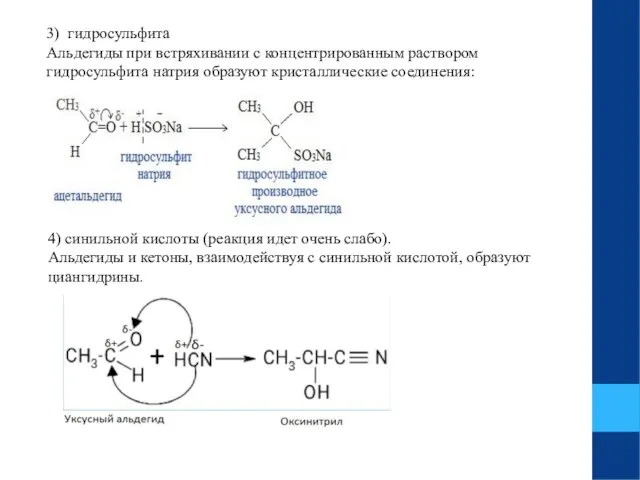
- 11. 3) гидросульфита Альдегиды при встряхивании с концентрированным раствором гидросульфита натрия образуют кристаллические соединения: 4) синильной кислоты
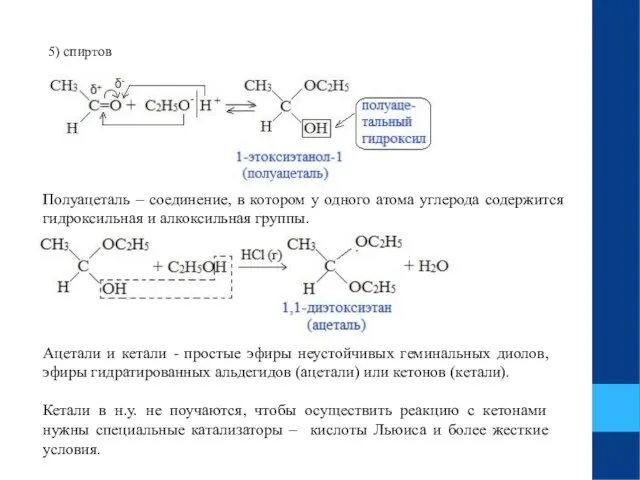
- 12. 5) спиртов Полуацеталь – соединение, в котором у одного атома углерода содержится гидроксильная и алкоксильная группы.
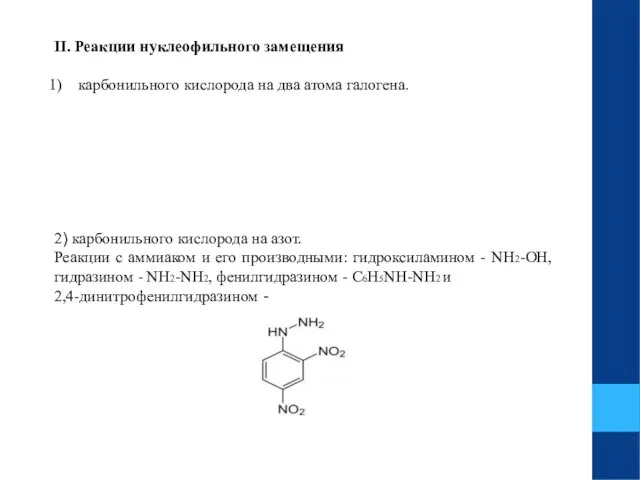
- 13. II. Реакции нуклеофильного замещения карбонильного кислорода на два атома галогена. 2) карбонильного кислорода на азот. Реакции
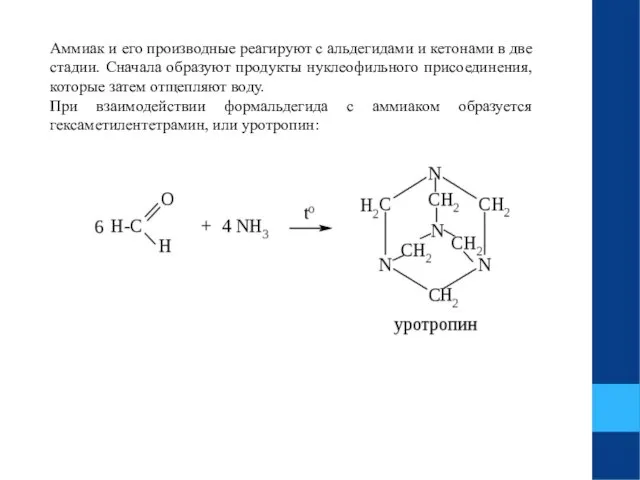
- 14. Аммиак и его производные реагируют с альдегидами и кетонами в две стадии. Сначала образуют продукты нуклеофильного
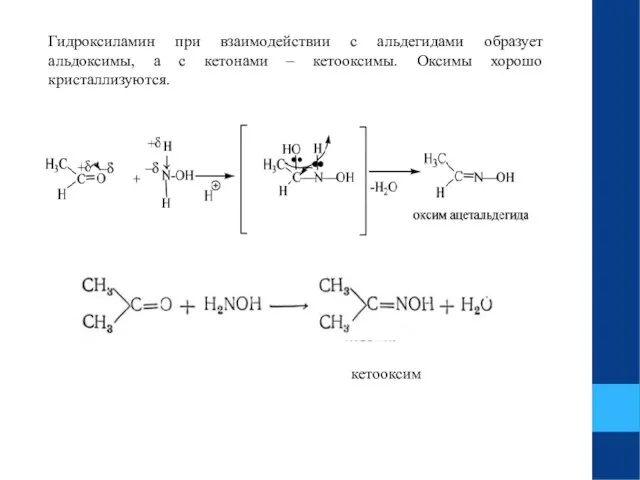
- 15. Гидроксиламин при взаимодействии с альдегидами образует альдоксимы, а с кетонами – кетооксимы. Оксимы хорошо кристаллизуются. кетооксим
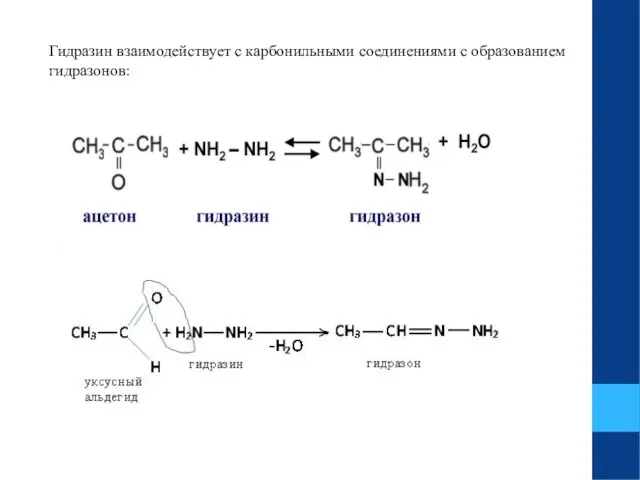
- 16. Гидразин взаимодействует с карбонильными соединениями с образованием гидразонов:
- 17. Альдегиды и кетоны, взаимодействуя с фенилгидразином или его производными, образует фенилгидразоны: Реакции хорошо идут и с
- 18. III. Реакция окисления Альдегиды окисляются легко как сильными, так и слабыми окислителями до соответствующих карбоновых кислот.
- 19. Окисление гидроксидом меди (II) (реакция «медного зеркала») Качественная реакция на альдегидную группу! Альдегид окисляется до соответствующей
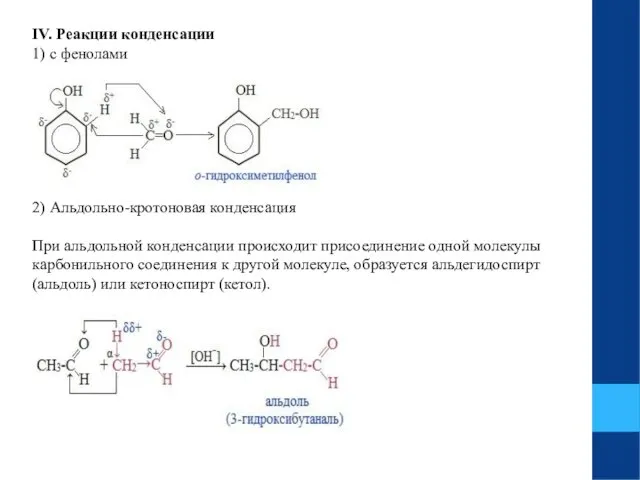
- 20. IV. Реакции конденсации 1) с фенолами 2) Альдольно-кротоновая конденсация При альдольной конденсации происходит присоединение одной молекулы
- 21. При кротоновой конденсации образуется молекула непредельного альдегида или кетона. Химическая реакция сопровождается выделением молекулы воды.
- 22. Вывод: Альдегиды более реакционно-способные, чем кетоны, т.к. 1. Для альдегидов легче идут реакции присоединения. 2. Альдегиды
- 23. Способы получения Окисление спиртов При окислении первичных спиртов образуются альдегиды, при окислении вторичных спиртов – кетоны.
- 24. 3. Гидратация алкинов (реакция Кучерова). Так как это реакция присоединение воды к непредельным углеводородам, то выполняется
- 25. 4. Каталитическое окисление алкенов кислородом воздуха Этим экономичным способом получают низшие альдегиды и кетоны. Этот промышленный
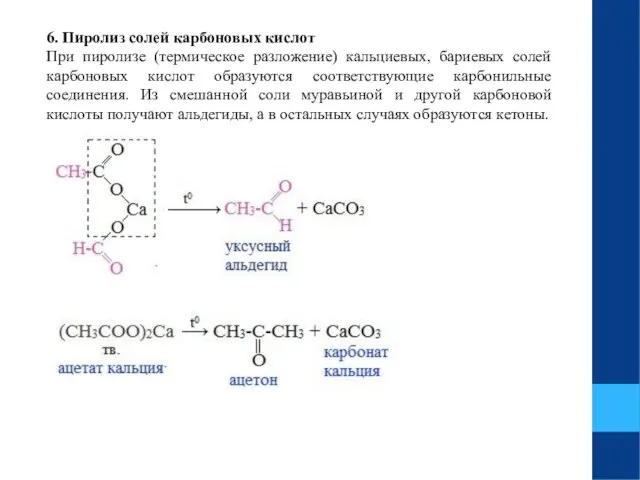
- 26. 6. Пиролиз солей карбоновых кислот При пиролизе (термическое разложение) кальциевых, бариевых солей карбоновых кислот образуются соответствующие
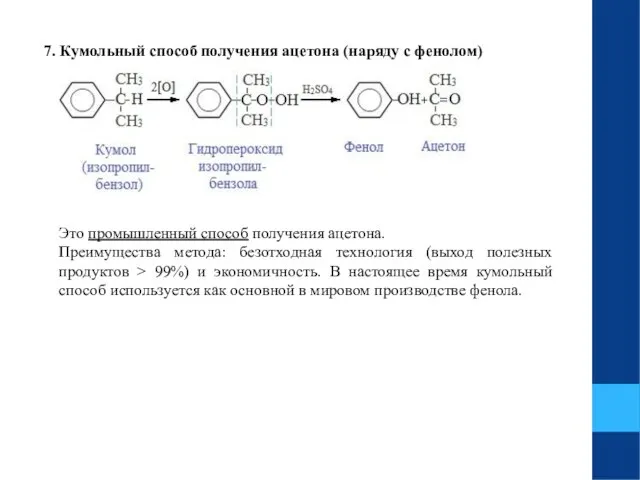
- 27. 7. Кумольный способ получения ацетона (наряду с фенолом) Это промышленный способ получения ацетона. Преимущества метода: безотходная
- 29. Скачать презентацию













 Сравнительный анализ Фармакопейных статей для субстанций, представленных в мировых Фармакопеях
Сравнительный анализ Фармакопейных статей для субстанций, представленных в мировых Фармакопеях Заполни электронные уровни элементов
Заполни электронные уровни элементов Свойства щелочных металлов
Свойства щелочных металлов Майда еритін витаминдер. А,D,E,K витаминдері
Майда еритін витаминдер. А,D,E,K витаминдері Презентация Типы изомерий 10 класс
Презентация Типы изомерий 10 класс Стиральные порошки и средства для стирки 2016
Стиральные порошки и средства для стирки 2016 Аттестационная работа. Проект по химии: Определение качества кисломолочных продуктов на примере сметаны
Аттестационная работа. Проект по химии: Определение качества кисломолочных продуктов на примере сметаны Презентация по Химии "Химия и пища" - скачать смотреть
Презентация по Химии "Химия и пища" - скачать смотреть  Особенности строения соединений органической химии. 10 класс
Особенности строения соединений органической химии. 10 класс Кислород. Характеристика и применение
Кислород. Характеристика и применение Группа веществ, требующих особых методов изолирования. Характеристика соединений. Токсикологическое значение
Группа веществ, требующих особых методов изолирования. Характеристика соединений. Токсикологическое значение Алюминий, его физические и химические свойства
Алюминий, его физические и химические свойства Водорастворимые витамины. (Лекция 13)
Водорастворимые витамины. (Лекция 13) Материаловедение
Материаловедение Хімія у створенні нових матеріалів та побуті
Хімія у створенні нових матеріалів та побуті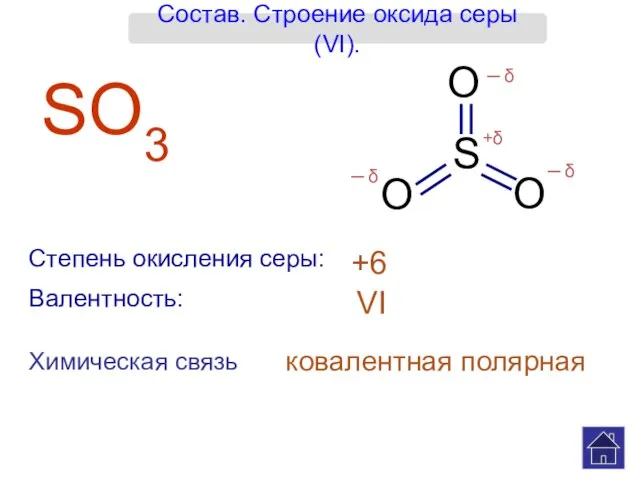 Оксид серы
Оксид серы Типы ингибирования и их характерные черты
Типы ингибирования и их характерные черты Вода. Особливості молекулярної води. Роль води в життєдіяльності організмів Палієнко Яна 10 – Б клас Вчитель: Громова Тетяна В
Вода. Особливості молекулярної води. Роль води в життєдіяльності організмів Палієнко Яна 10 – Б клас Вчитель: Громова Тетяна В Правила безопасности в кабинете химии. Приёмы обращения с лабораторным оборудованием
Правила безопасности в кабинете химии. Приёмы обращения с лабораторным оборудованием Бытовая химия в квартире
Бытовая химия в квартире Презентация по Химии "Химия и проблема охраны окружающей среды" - скачать смотреть бесплатно
Презентация по Химии "Химия и проблема охраны окружающей среды" - скачать смотреть бесплатно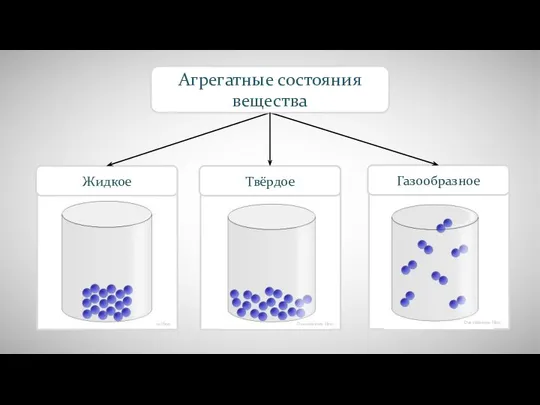 Агрегатные состояния вещества
Агрегатные состояния вещества Разработка проектных решений по переводу паровых котлов электростанций в конденсационный режим с целью увеличения кпд котла
Разработка проектных решений по переводу паровых котлов электростанций в конденсационный режим с целью увеличения кпд котла Диаграммы состояния сплавов, компоненты которых имеют полиморфное превращение
Диаграммы состояния сплавов, компоненты которых имеют полиморфное превращение Химия гетероциклических соединений
Химия гетероциклических соединений Тренажер Знаки Хэ
Тренажер Знаки Хэ Алмазы. Бриллианты
Алмазы. Бриллианты Переработка тяжелых нефтей, битумов и нефтяных остатков
Переработка тяжелых нефтей, битумов и нефтяных остатков