Содержание
- 2. Задание: 1. Изучить теоретический материал 2. Выписать названия и буквенные обозначения основных линий диаграмм 3.Начертить диаграммы
- 3. Диаграмма состояния 1 типа Компоненты не растворимы друг в друге в твердом состоянии Основные линии диаграммы:
- 4. Диаграмма состояния 2 типа Компоненты неограниченно растворимы друг в друге в твердом состоянии. Компоненты имеют близкие
- 5. Диаграмма состояния 3 типа Компоненты ограниченно растворимы друг в друге.
- 6. abc – линия ликвидус; Xb – химический состав эвтектики. adec – линия солидус. df, eg –
- 7. Диаграмма состояния IV типа Компоненты образуют в твердом состоянии химические соединения. Диаграммы для компонентов, образующих химические
- 8. Правило отрезков для диаграмм I типа. Для линий abd, bce и части диаграммы ниже линии de
- 9. Правило отрезков для диаграммы II типа Для a1b2 работает правило отрезков: ; Химический состав фаз для
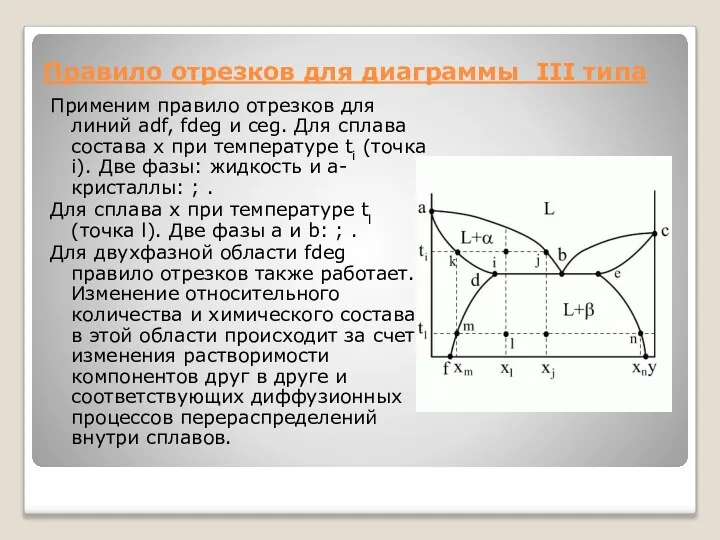
- 10. Правило отрезков для диаграммы III типа Применим правило отрезков для линий adf, fdeg и ceg. Для
- 11. Тестирование № 1. Какой вид имеет уравнение правила фаз? А) С = К + F –
- 12. № 6. Диаграмма состояния какого типа представлена на рис. 27? А) С неограниченной растворимостью компонентов в
- 13. № 10. При каких температурных условиях кристаллизуются чистые металлы? А) В зависимости от природы металла температура
- 14. № 15. Какому сплаву (каким сплавам) принадлежит кривая охлаждения В (рис.31)? d. В) а и d.
- 15. № 18. На рис. 34 представлена диаграмма состояния с полиморфным превращением компонента А. Какое из суждений
- 17. Скачать презентацию
Задание:
1. Изучить теоретический материал
2. Выписать названия и буквенные обозначения основных линий
Задание:
1. Изучить теоретический материал
2. Выписать названия и буквенные обозначения основных линий
4. Изучить правило отрезков
5. Пройти тест
Диаграмма состояния 1 типа
Компоненты не растворимы друг в друге в твердом
Диаграмма состояния 1 типа Компоненты не растворимы друг в друге в твердом
Основные линии диаграммы:
abc – линия ликвидус – геометрическое место точек начала кристаллизации сплавов различного химического состава: Выше этой линии все сплавы находятся в жидком состоянии. L – liquid.
dbe – линия солидус – геометрическое место точек конца процесса кристаллизации; Ниже этой линии все сплавы находятся в твердом состоянии.
abd и bce – двухфазное состояние сплавов – происходит процесс кристаллизации.
Точка b – точка эвтектики;
xb – эвтектический состав для данной пары компонентов.
Анализ превращений на диаграмме состояния каждого сплава необходимо вести вдоль вертикальной линии, проходящей через точку на оси химического состава, определяющую суммарный химический состав сплава. То есть состав сплава определяется точкой на диаграмме с координатами температура–химический состав.Структура и фазовый состав будет определяться областью, в которую попадет эта точка. Сплав (3) – эвтектический сплав, включающий в себя оба компонента; кристаллизуется аналогично чистым компонентам при постоянной температуре.
Диаграмма состояния 2 типа
Компоненты неограниченно растворимы друг в друге в твердом
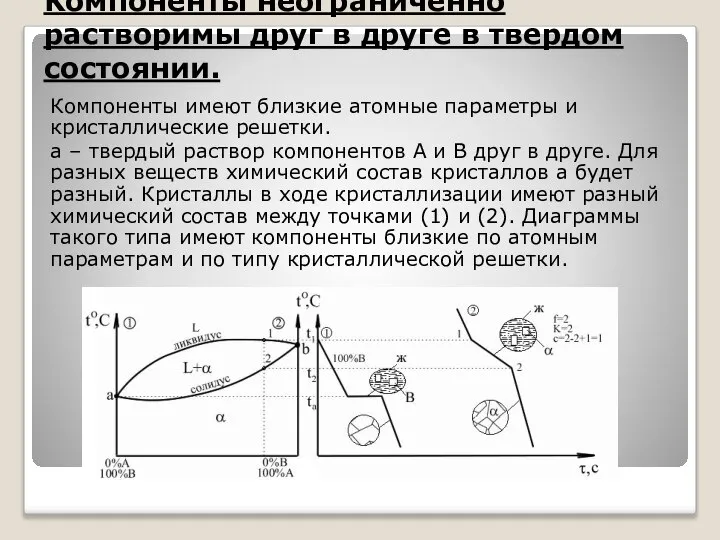
Диаграмма состояния 2 типа Компоненты неограниченно растворимы друг в друге в твердом
Компоненты имеют близкие атомные параметры и кристаллические решетки.
a – твердый раствор компонентов А и В друг в друге. Для разных веществ химический состав кристаллов a будет разный. Кристаллы в ходе кристаллизации имеют разный химический состав между точками (1) и (2). Диаграммы такого типа имеют компоненты близкие по атомным параметрам и по типу кристаллической решетки.
Диаграмма состояния 3 типа
Компоненты ограниченно растворимы друг в друге.
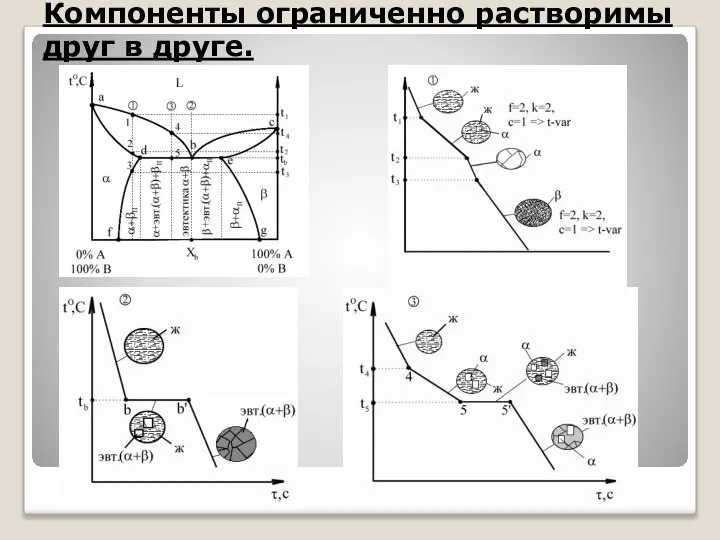
Диаграмма состояния 3 типа
Компоненты ограниченно растворимы друг в друге.
abc – линия ликвидус; Xb – химический состав эвтектики.
adec – линия
abc – линия ликвидус; Xb – химический состав эвтектики.
adec – линия
df, eg – линии предельной растворимости в твердом состоянии.
a – ограниченный твердый раствор компонента А в компоненте В.
b – ограниченный твердый раствор компонента B в компоненте А.
Сплав (1): Выше t1 – охлаждение с высокой скоростью, зависящее от внешних условий. 1-2 – первичная кристаллизация, образование a твердого раствора. Вследствие низкого содержания компонента А в исходном сплаве при достижении t2 весь компонент А расходуется на образование a-кристаллов, следовательно в точке 2 – однофазный твердый сплав. 2-3 – остывание сплава; превращений нет. Ниже температуры t3 – точка 3 соответствует достижению a-кристаллического состояния насыщенности, дальнейшее понижение температуры приводит к выделению избыточного компонента А за счет диффузии в небольшие зоны на границе кристаллов. Эти зоны превращаются в мелкие кристаллы b, то есть происходит вторичная кристаллизация внутри твердой фазы.
Сплав (2): Процесс аналогичен образованию эвтектики, толь ко вместо чистых компонентов А и В – a- и b-твердые растворы.
Сплав (3): Выше температуры t4 – охлаждение сплава – превращений нет. t4 – t5 – первичная кристаллизация a-кристаллов, при этом содержание компонента А в жидкости уменьшается и состав жидкости постепенно приближается к эвтектическому (при t5). 5–5' – состав жидкости соответствует эвтектическому, идет образование эвтектики (температура постоянна). Температура ниже t5 – охлаждение сплава, вторичная кристаллизация с образованием bII-вторичных кристаллов. Для заэвтектической области процессы и кривые охлаждения сплавов аналогичны, только a- и b-кристаллы меняются местами.
Диаграмма состояния IV типа
Компоненты образуют в твердом состоянии химические соединения.
Диаграммы для
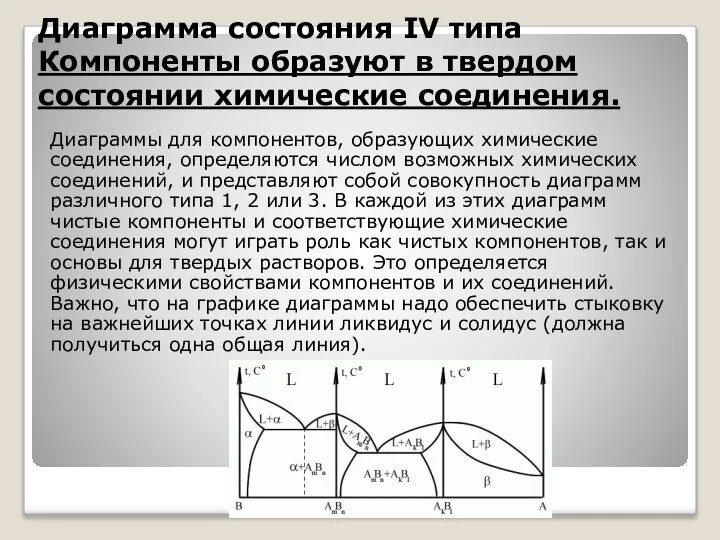
Диаграмма состояния IV типа
Компоненты образуют в твердом состоянии химические соединения.
Диаграммы для
Правило отрезков для диаграмм I типа.
Для линий abd, bce и части
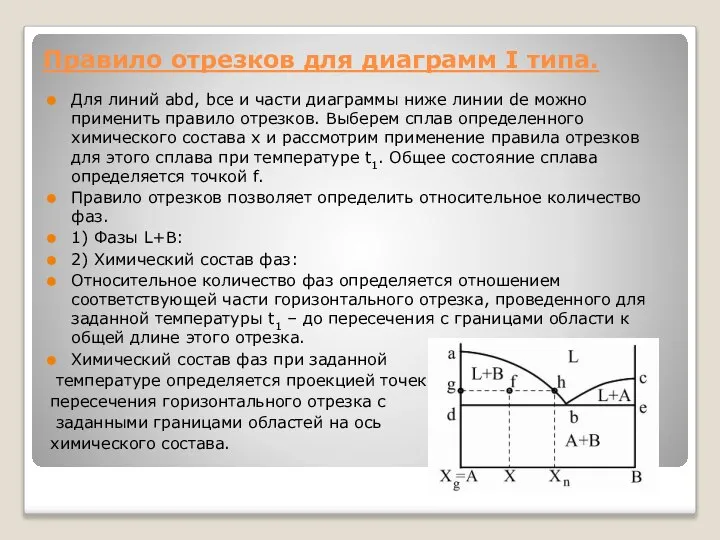
Правило отрезков для диаграмм I типа.
Для линий abd, bce и части
Правило отрезков позволяет определить относительное количество фаз.
1) Фазы L+B:
2) Химический состав фаз:
Относительное количество фаз определяется отношением соответствующей части горизонтального отрезка, проведенного для заданной температуры t1 – до пересечения с границами области к общей длине этого отрезка.
Химический состав фаз при заданной
температуре определяется проекцией точек
пересечения горизонтального отрезка с
заданными границами областей на ось
химического состава.
Правило отрезков для диаграммы II типа
Для a1b2 работает правило отрезков: ;
Правило отрезков для диаграммы II типа
Для a1b2 работает правило отрезков: ;
Химический состав фаз для рассматриваемой области определяется проекциями точек, попадающих на границу с областью, занимаемой соответствующей фазой, то есть в донном случае точка g на границе с областью a – определяет химический состав a-кристаллов, точка h на границе с областью L – определяет химический состав жидкости.
Применим правило отрезков для точек 1, f и 2 сплава x. При этом химический состав образующихся a-кристаллов будет меняться от x, через xg до исходного состава x в соответствии с правилом отрезков, то есть при кристаллизации a-кристаллы, образующиеся на разных этапах кристаллизации имеют разный химический состав.
Это противоречие связано с тем, что рассматриваемая нами диаграмма состояния является равновесной, то есть:
а) Процесс фазового превращения происходит бесконечно медленно;
б) Происходит диффузионное выравнивание химических составов каждой фазы;
В действительности:
а) Скорость кристаллизации конечна;
б) Полного выравнивания химического состава твердой фазы не происходит, то есть в составе образовавшейся твердой структуры остаются a-кристаллы с отличающимся от среднего химическим составом. Это явление носит название химической ликвации.
Ликвация – процесс, при котором часть структуры
сплава отличается по своему химическому строению от
Основного состава. В реальных сплавах всегда происходит
процесс ликвации.
Правило отрезков для диаграммы III типа
Применим правило отрезков для линий adf,
Правило отрезков для диаграммы III типа
Применим правило отрезков для линий adf,
Для сплава x при температуре tl (точка l). Две фазы a и b: ; .
Для двухфазной области fdeg правило отрезков также работает. Изменение относительного количества и химического состава в этой области происходит за счет изменения растворимости компонентов друг в друге и соответствующих диффузионных процессов перераспределений внутри сплавов.
Тестирование
№ 1. Какой вид имеет уравнение правила фаз?
А) С = К
Тестирование
№ 1. Какой вид имеет уравнение правила фаз?
А) С = К
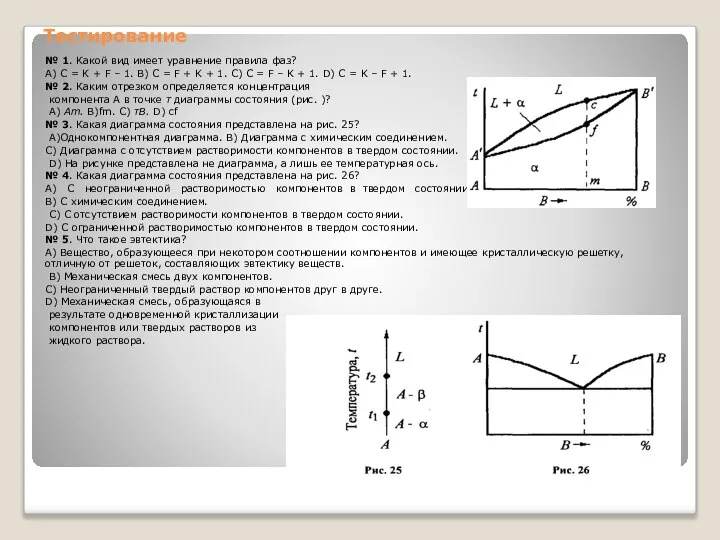
№ 2. Каким отрезком определяется концентрация
компонента А в точке т диаграммы состояния (рис. )?
A) Am. B)fm. С) тВ. D) сf
№ 3. Какая диаграмма состояния представлена на рис. 25?
А)Однокомпонентная диаграмма. В) Диаграмма с химическим соединением.
С) Диаграмма с отсутствием растворимости компонентов в твердом состоянии.
D) На рисунке представлена не диаграмма, а лишь ее температурная ось.
№ 4. Какая диаграмма состояния представлена на рис. 26?
A) С неограниченной растворимостью компонентов в твердом состоянии.
B) С химическим соединением.
С) С отсутствием растворимости компонентов в твердом состоянии.
D) С ограниченной растворимостью компонентов в твердом состоянии.
№ 5. Что такое эвтектика?
А) Вещество, образующееся при некотором соотношении компонентов и имеющее кристаллическую решетку, отличную от решеток, составляющих эвтектику веществ.
В) Механическая смесь двух компонентов.
С) Неограниченный твердый раствор компонентов друг в друге.
D) Механическая смесь, образующаяся в
результате одновременной кристаллизации
компонентов или твердых растворов из
жидкого раствора.
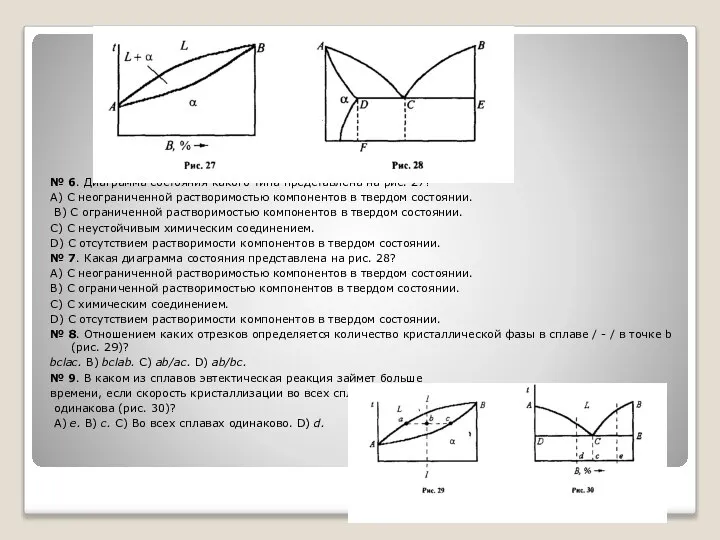
№ 6. Диаграмма состояния какого типа представлена на рис. 27?
А) С
№ 6. Диаграмма состояния какого типа представлена на рис. 27?
А) С
В) С ограниченной растворимостью компонентов в твердом состоянии.
С) С неустойчивым химическим соединением.
D) С отсутствием растворимости компонентов в твердом состоянии.
№ 7. Какая диаграмма состояния представлена на рис. 28?
А) С неограниченной растворимостью компонентов в твердом состоянии.
В) С ограниченной растворимостью компонентов в твердом состоянии.
С) С химическим соединением.
D) С отсутствием растворимости компонентов в твердом состоянии.
№ 8. Отношением каких отрезков определяется количество кристаллической фазы в сплаве / - / в точке b (рис. 29)?
bclac. В) bclab. С) ab/ас. D) аb/bс.
№ 9. В каком из сплавов эвтектическая реакция займет больше
времени, если скорость кристаллизации во всех сплавах
одинакова (рис. 30)?
А) е. В) с. С) Во всех сплавах одинаково. D) d.
№ 10. При каких температурных условиях кристаллизуются чистые металлы?
А) В зависимости
№ 10. При каких температурных условиях кристаллизуются чистые металлы?
А) В зависимости
№ 11. При каких температурных условиях кристаллизуются сплавы в системе с неограниченной растворимостью компонентов в твердом состоянии?
А) Все сплавы кристаллизуются при снижающейся температуре.
В) Кристаллизация сплавов протекает при снижающейся температуре, завершается -при постоянной.
С) Все сплавы кристаллизуются при постоянной температуре.
D) Сплавы кристаллизуются при растущей температуре (из-за выделения скрытой теплоты кристаллизации).
№ 12. При каких температурных условиях кристаллизуются эвтектики в двухкомпонентных сплавах?
А) При снижающейся температуре. В) В зависимости от вида сплава температура может расти в одних случаях, снижаться в других и оставаться постоянной в третьих.
С) При постоянной температуре. D) При растущей температуре.
№ 13. Как меняется температура сплавов системы с отсутствием растворимости компонентов в твердом состоянии в процессе кристаллизации?
А) Снижается (кроме эвтектического сплава), завершается кристаллизация всех сплавов при постоянной температуре. В) Остается постоянной. С) Снижается.
D) Снижается (кроме эвтектического сплава), завершается кристаллизация некоторых сплавов при постоянной температуре.
№ 14. В чем состоит отличие эвтектоидного превращения от эвтектического?
А) При эвтектоидном превращении возникают промежуточные фазы, при эвтектическом - механические смеси. В) Принципиальных отличий нет. Это однотипные превращения.
С) При эвтектоидном превращении распадается твердый раствор, при эвтектическом - жидкий. D) При эвтектоидном превращении из твердых растворов выделяются вторичные кристаллы, при эвтектическом - из жидкости - первичные.
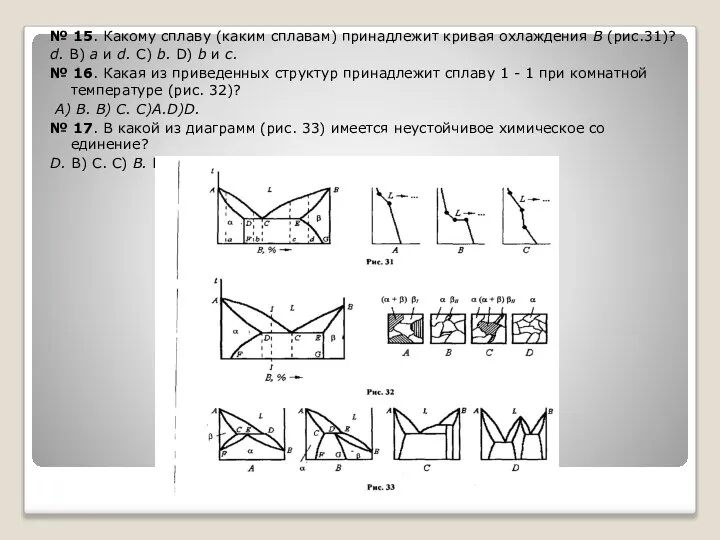
№ 15. Какому сплаву (каким сплавам) принадлежит кривая охлаждения В (рис.31)?
d.
№ 15. Какому сплаву (каким сплавам) принадлежит кривая охлаждения В (рис.31)?
d.
№ 16. Какая из приведенных структур принадлежит сплаву 1 - 1 при комнатной температуре (рис. 32)?
А) В. В) С. C)A.D)D.
№ 17. В какой из диаграмм (рис. 33) имеется неустойчивое химическое соединение?
D. В) С. С) В. D) А.
№ 18. На рис. 34 представлена диаграмма состояния с полиморфным превращением
№ 18. На рис. 34 представлена диаграмма состояния с полиморфным превращением
А) Высокотемпературная модификация компонента А изоморфна В.
В) Тип кристаллической решетки компонента А отличен от В.
С) Низкотемпературная модификация А изоморфна компоненту В.
D) Компонент А имеет кристаллическую решетку того же типа, что и компонент В.
№ 19. Какое из суждений относительно приведенной на рис. 35 диаграммы справедливо?
На рис. 35 приведена диаграмма...
А) А - В. Компоненты А и В неограниченно растворяются друг в друге.
B) с полиморфным превращением. Обе модификации А изоморфны компоненту В.
C) с эвтектикой. Низкотемпературная модификация А и компонент В имеют однотипные решетки.
D)c перитектикой. Компонент А имеет полиморфное превращение. Низкотемпературная модификация А изоморфна В.
№ 20. В какой диаграмме (каких диаграммах) состояния есть полиморфное превращение (рис. 36)?
A)D. B)A.C)C. D)B И C.






 Инсектициды на основе бакуловирусов
Инсектициды на основе бакуловирусов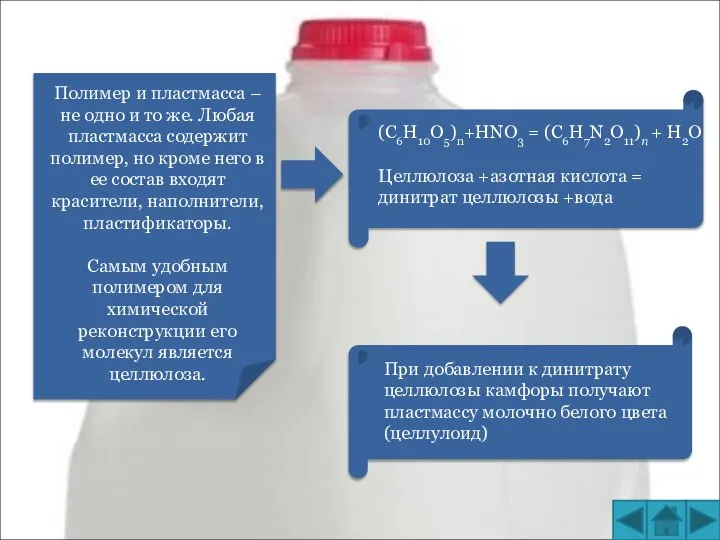 Полимер и пластмасса
Полимер и пластмасса Металлы в нашей жизни
Металлы в нашей жизни Сложные эфиры
Сложные эфиры Металлы и их соединения
Металлы и их соединения Властивості етанової (оцтової) кислоти
Властивості етанової (оцтової) кислоти Елементарний склад живих організмів
Елементарний склад живих організмів Структурно-механические свойства дисперсных систем
Структурно-механические свойства дисперсных систем Протеины: плюсы и минусы
Протеины: плюсы и минусы Излучение и поглощение света атомами. Виды спектров, спектральный анализ
Излучение и поглощение света атомами. Виды спектров, спектральный анализ Относительная атомная масса
Относительная атомная масса Биодизельное топливо
Биодизельное топливо Неметалічні елементи
Неметалічні елементи Бромды метил буының концентрациясын анықтау тәсілдемесі
Бромды метил буының концентрациясын анықтау тәсілдемесі Металлдардың кристалдық құрылымы
Металлдардың кристалдық құрылымы Поняття про лікарські препарати Підготували Стебко Марія, Бондар Аліна 11-Ф
Поняття про лікарські препарати Підготували Стебко Марія, Бондар Аліна 11-Ф  Закон постоянства состава веществ
Закон постоянства состава веществ Аргентум (Срібло)
Аргентум (Срібло) Мило. Синтетичні миючі засоби.
Мило. Синтетичні миючі засоби.  Растворы электролитов. Буферные растворы. Лекция 4
Растворы электролитов. Буферные растворы. Лекция 4 Аммиак. Физические и химические свойства. Получение и применение
Аммиак. Физические и химические свойства. Получение и применение Обмен железа и его нарушения
Обмен железа и его нарушения Презентация по Химии "Окислительно-восстановительные реакции" - скачать смотреть бесплатно
Презентация по Химии "Окислительно-восстановительные реакции" - скачать смотреть бесплатно Кетоны
Кетоны Альдегиды. Строение молекулы
Альдегиды. Строение молекулы Элементы третьего периода, периодической системы Д. И. Менделеева
Элементы третьего периода, периодической системы Д. И. Менделеева Нанохімія та нанотехнології
Нанохімія та нанотехнології Allgemeine Chemie für PharmazeutInnen
Allgemeine Chemie für PharmazeutInnen