Содержание
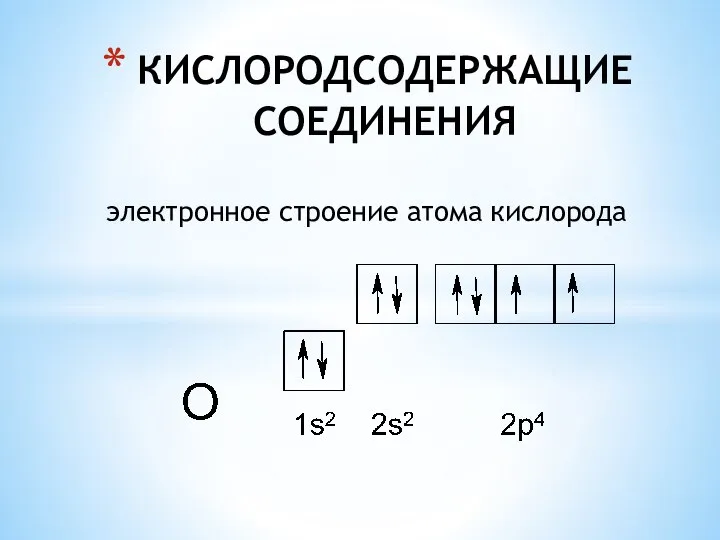
- 2. КИСЛОРОДСОДЕРЖАЩИЕ СОЕДИНЕНИЯ электронное строение атома кислорода
- 3. КИСЛОРОДСОДЕРЖАЩИЕ СОЕДИНЕНИЯ электронное строение атома кислорода 25.03.2011 Нижник Я.П. http://norgchem.professorjournal.ru
- 4. 25.03.2011 Нижник Я.П. http://norgchem.professorjournal.ru
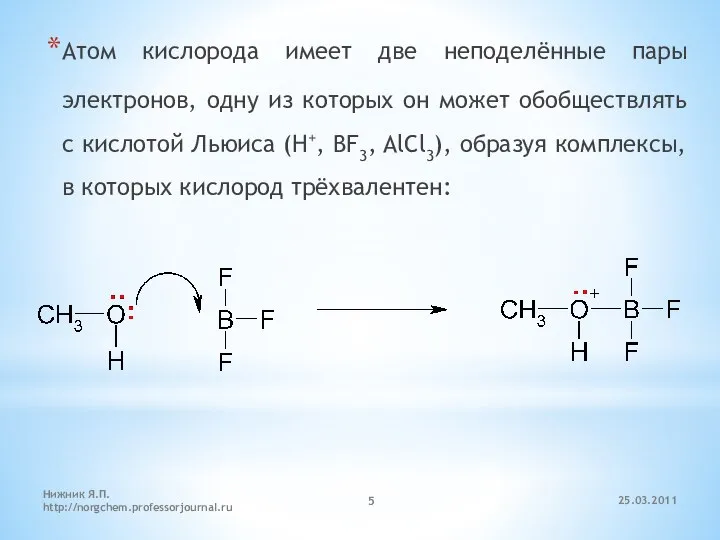
- 5. Атом кислорода имеет две неподелённые пары электронов, одну из которых он может обобществлять с кислотой Льюиса
- 6. СПИРТЫ и ФЕНОЛЫ этанол этенол фенол β-нафтол (этиловый спирт) (виниловый спирт) спирты фенолы 25.03.2011 Нижник Я.П.
- 7. 1. Строение и классификация Две конформации этанола в кристаллическом состоянии P.-G. Jonsson // Acta Crystallogr.,Sect.B, 1976,
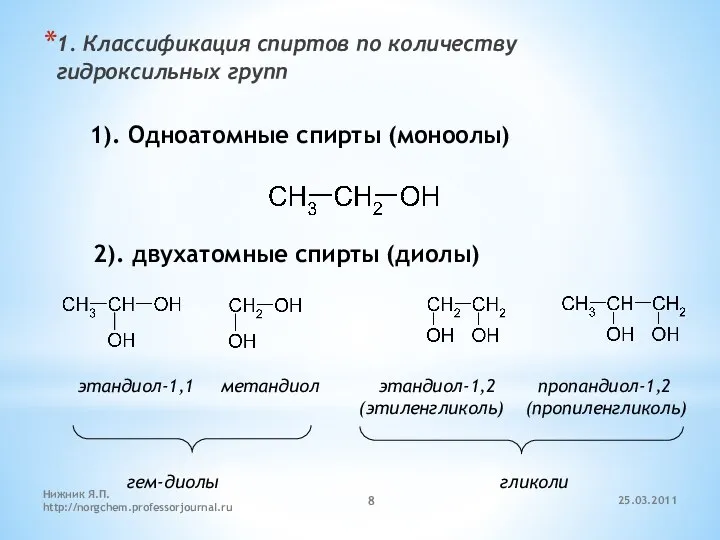
- 8. 1. Классификация спиртов по количеству гидроксильных групп 1). Одноатомные спирты (моноолы) 2). двухатомные спирты (диолы) этандиол-1,1
- 9. 3). Многоатомные спирты пропантриол-1,2,3 бутантетраол-1,2,3,4 (глицерин) (эритрит) 25.03.2011 Нижник Я.П. http://norgchem.professorjournal.ru
- 10. 2. Классификация по типу спиртового атома углерода 1). Первичные спирты. первичный бутиловый спирт (бутанол-1) 2). Вторичные
- 11. 2. Номенклатура 25.03.2011 Нижник Я.П. http://norgchem.professorjournal.ru
- 12. 3-метилбутанол-1 бутен-3-ол-1 2-гидроксипропановая кислота 2-оксипропановая кислота 25.03.2011 Нижник Я.П. http://norgchem.professorjournal.ru
- 13. 3. Изомерия 3.1. Cтруктурная изомерия 3.1. 1. Изомерия положения заместителей пентанол-1 пентанол-2 пентанол-3 3.1. 2. Изомерия
- 14. 3.1. 3. Межклассовая изомерия этанол диметиловый эфир 3.2. Пространственная изомерия 25.03.2011 Нижник Я.П. http://norgchem.professorjournal.ru
- 15. 4. Физические и биологические свойства Гидроксигруппа является сильно полярной группой, поэтому низшие спирты растворяются в воде
- 16. Низшие члены гомологического ряда спиртов являются жидкостями и, начиная с C12 (т.пл. додеканола-1 24оС), одноатомные спирты
- 17. Температуры кипения спиртов являются аномально высокими по сравнению с температурами кипения изомерных им простых эфиров. Таблица
- 18. P.-G. Jonsson // Acta Crystallogr.,Sect.B, 1976, Vol.32, P.232. 25.03.2011 Нижник Я.П. http://norgchem.professorjournal.ru
- 19. Метиловый спирт считается самым ядовитым спиртом. Вызывает слепоту или смерть. http://photofile.ru/users/pratezgalavy/2175396/37069795/ 25.03.2011 Нижник Я.П. http://norgchem.professorjournal.ru
- 20. Токсическое действие метанола связано с угнетением центральной нервной системы, развитием тяжелого метаболического ацидоза, поражением сетчатки глаза
- 21. Этиловый спирт оказывает опьяняющее действие. “вино веселит сердце человека” (Псалом103:15) В высоких концентрациях этанол оказывает анестезирующее
- 22. 25.03.2011 Нижник Я.П. http://norgchem.professorjournal.ru
- 23. 5. Химические свойства 5.1. Кислотные свойства спиртов этоксид натрия 25.03.2011 Нижник Я.П. http://norgchem.professorjournal.ru
- 24. 5.2. Реакции нуклеофильного замещения 5.2.1. Образование галогенопроизводных 25.03.2011 Нижник Я.П. http://norgchem.professorjournal.ru
- 25. 5.2.2. Образование простых эфиров этанол диэтилововый эфир 25.03.2011 Нижник Я.П. http://norgchem.professorjournal.ru
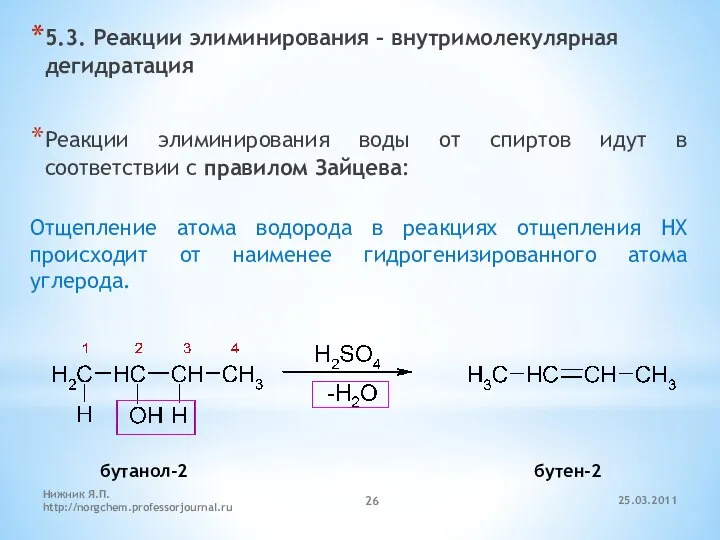
- 26. 5.3. Реакции элиминирования – внутримолекулярная дегидратация Реакции элиминирования воды от спиртов идут в соответствии с правилом
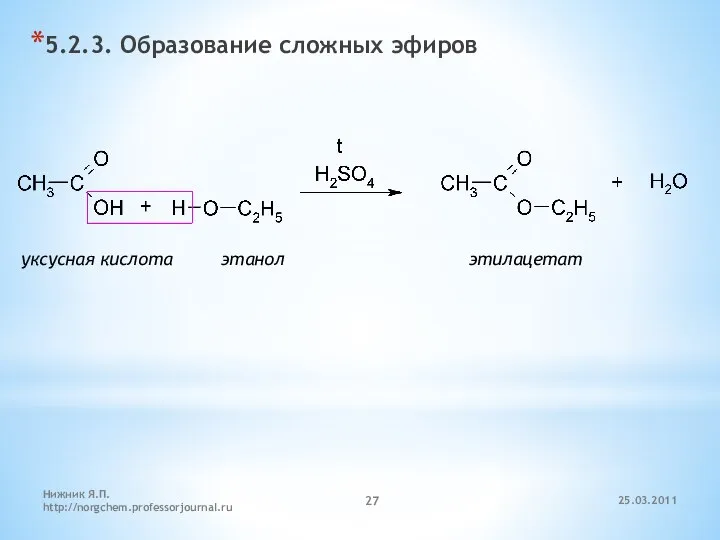
- 27. 5.2.3. Образование сложных эфиров уксусная кислота этанол этилацетат 25.03.2011 Нижник Я.П. http://norgchem.professorjournal.ru
- 28. 5.3. Реакции окисления спиртов Мягкие окислители окисляют первичные спирты в альдегиды, а вторичные спирты в кетоны.
- 29. ретинол (витамин А) ретиналь первичный спирт альдегид карбоновая кислота вторичный спирт кетон 25.03.2011 Нижник Я.П. http://norgchem.professorjournal.ru
- 30. 25.03.2011 Нижник Я.П. http://norgchem.professorjournal.ru
- 31. 6. Получение спиртов 6.1. Гидратация алкенов 6.2. Гидролиз алкилгалогенидов этилен этанол (этиловый спирт) 25.03.2011 Нижник Я.П.
- 32. 6.3. Восстановление альдегидов и кетонов 6.4. Взаимодействие металлоорганических соединений с карбонильными соединениями 25.03.2011 Нижник Я.П. http://norgchem.professorjournal.ru
- 33. 6.5. Промышленное получение спиртов До 1925 года метанол получали пиролизом древесины. В настоящее время его получают
- 34. Saccharomyces cerevisiae 25.03.2011 Нижник Я.П. http://norgchem.professorjournal.ru
- 35. Бутиловый спирт используется как растворитель, топливо и для получения пластификаторов (дибутилфталата) и т.д. Бутиловый спирт получают
- 36. МНОГОАТОМНЫЕ СПИРТЫ 1. Изомерия и номенклатура этиленгликоль глицерин эритрит 25.03.2011 Нижник Я.П. http://norgchem.professorjournal.ru
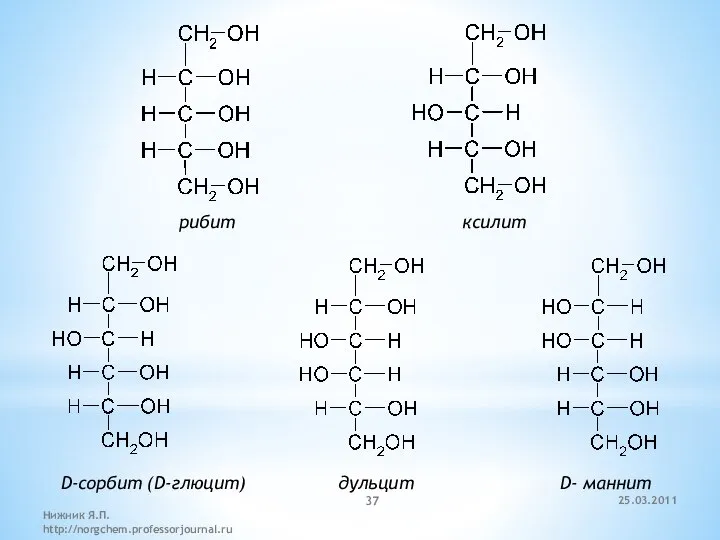
- 37. рибит ксилит D-сорбит (D-глюцит) дульцит D- маннит 25.03.2011 Нижник Я.П. http://norgchem.professorjournal.ru
- 38. 2. Физические и биологические свойства Этиленгликоль и пропиленгликоль являются высококипящими жидкостями, глицерин представляет собой очень вязкую
- 39. 3. Химические свойства 3.1. Кислотные свойства. 3.2. Нуклеофильное замещение. глицерин стеариновая кислота тристеароилглицерин (тристеарин) 25.03.2011 Нижник
- 40. Нитроглицерин используется во взрывчатых веществах - динамитах и бездымных порохах - баллиститах. Динамит и баллистит были
- 41. этиленгликоль диоксан 3.3. Реакции элиминирования – внутримолекулярная дегидратация. глицерин пропадиенол акролеин 25.03.2011 Нижник Я.П. http://norgchem.professorjournal.ru
- 42. 3.4. Окисление глицеральдегид дигидроксиацетон При действии мягких окислителей (H2O2/Fe2+, O2/Pt, Br2/сода) окисляется только одна спиртовая группа
- 43. периодатное окисление – окисление йодной кислотой 25.03.2011 Нижник Я.П. http://norgchem.professorjournal.ru
- 44. 4. Получение этан этилен этиленоксид этиленгликоль Этиленгликоль – бесцветная вязкая жидкость, tкип 197,6 °С. Применяется как
- 45. жир (тристеароилглицерин) глицерин стеариновая кислота 25.03.2011 Нижник Я.П. http://norgchem.professorjournal.ru
- 46. ксилоза ксилит Многоатомные спирты часто встречаются в природе. Сорбит содержится в плодах рябины (лат. sorbus –
- 48. Скачать презентацию







































 Кремнийорганические модификаторы
Кремнийорганические модификаторы Рибозимы. Строение
Рибозимы. Строение Кислотные и основные свойства органических соединений
Кислотные и основные свойства органических соединений Аэрозоли – аэродисперсии действие на организм
Аэрозоли – аэродисперсии действие на организм Способы разделения смесей
Способы разделения смесей Презентация по Химии "Жевательная резинка: польза или вред?" - скачать смотреть
Презентация по Химии "Жевательная резинка: польза или вред?" - скачать смотреть  Ковалентная связь
Ковалентная связь Технология кварцевого стекла
Технология кварцевого стекла Электронное строение атома
Электронное строение атома Химические реакции
Химические реакции 27 февраля 2013
27 февраля 2013 Растворение как физико-химический процесс. Растворимость. Типы растворов
Растворение как физико-химический процесс. Растворимость. Типы растворов Химический элемент кремний
Химический элемент кремний МБОУ Луховицкая средняя общеобразовательная школа №9 Бинарный урок география – химия 9 класс Минеральные удобре
МБОУ Луховицкая средняя общеобразовательная школа №9 Бинарный урок география – химия 9 класс Минеральные удобре Презентация по Химии "Раціональне використання добрив та проблеми охорони природи" - скачать смотреть бесплатно
Презентация по Химии "Раціональне використання добрив та проблеми охорони природи" - скачать смотреть бесплатно Количество вещества. Молярная масса
Количество вещества. Молярная масса Вторичное квантование. Применение оболочечной модели. Метод Хартри - Фока
Вторичное квантование. Применение оболочечной модели. Метод Хартри - Фока Тема проекта: «Влияние культуры знаний на отношение к курению» Выполнил: Братым Артур, Васильев Андрей Руководитель: Бобр
Тема проекта: «Влияние культуры знаний на отношение к курению» Выполнил: Братым Артур, Васильев Андрей Руководитель: Бобр Введение в количественный анализ
Введение в количественный анализ Миючі засоби Виконала учениця 9-А класу, Велітченко Юлія
Миючі засоби Виконала учениця 9-А класу, Велітченко Юлія  Презентация Химическая связь
Презентация Химическая связь  Сорбционные процессы
Сорбционные процессы Основные характеристики ковалентной связи
Основные характеристики ковалентной связи Анализ стабильности экологических характеристик товарных дизельных топлив после перекачки
Анализ стабильности экологических характеристик товарных дизельных топлив после перекачки Приготовление основного и рабочих растворов хлорной извести
Приготовление основного и рабочих растворов хлорной извести Sample Kit Kemira 3f. External
Sample Kit Kemira 3f. External Титан. Нахождение в природе
Титан. Нахождение в природе Презентация Оксиды
Презентация Оксиды